Clear Sky Science · ru
Эффективное превращение метанола в этиленгликоль и глиоксаль посредством дивергентного синтеза с C−C связями
Превращение простого топлива в полезные строительные блоки
Метанол, простой спирт, который можно получать из углекислого газа, природного газа, угля или биомассы, уже является важным топливом и химикатом. В этом исследовании показано, как потоки света и тщательно спроектированные наноматериалы могут трансформировать метанол в более сложные, более ценные молекулы — при этом одновременно выделяя водородный газ как чистый энергоноситель. Работа раскрывает новый способ направлять один исходный материал в два разных полезных продукта простым изменением того, как отдельные атомы металла расположены на крошечной поверхности катализатора. 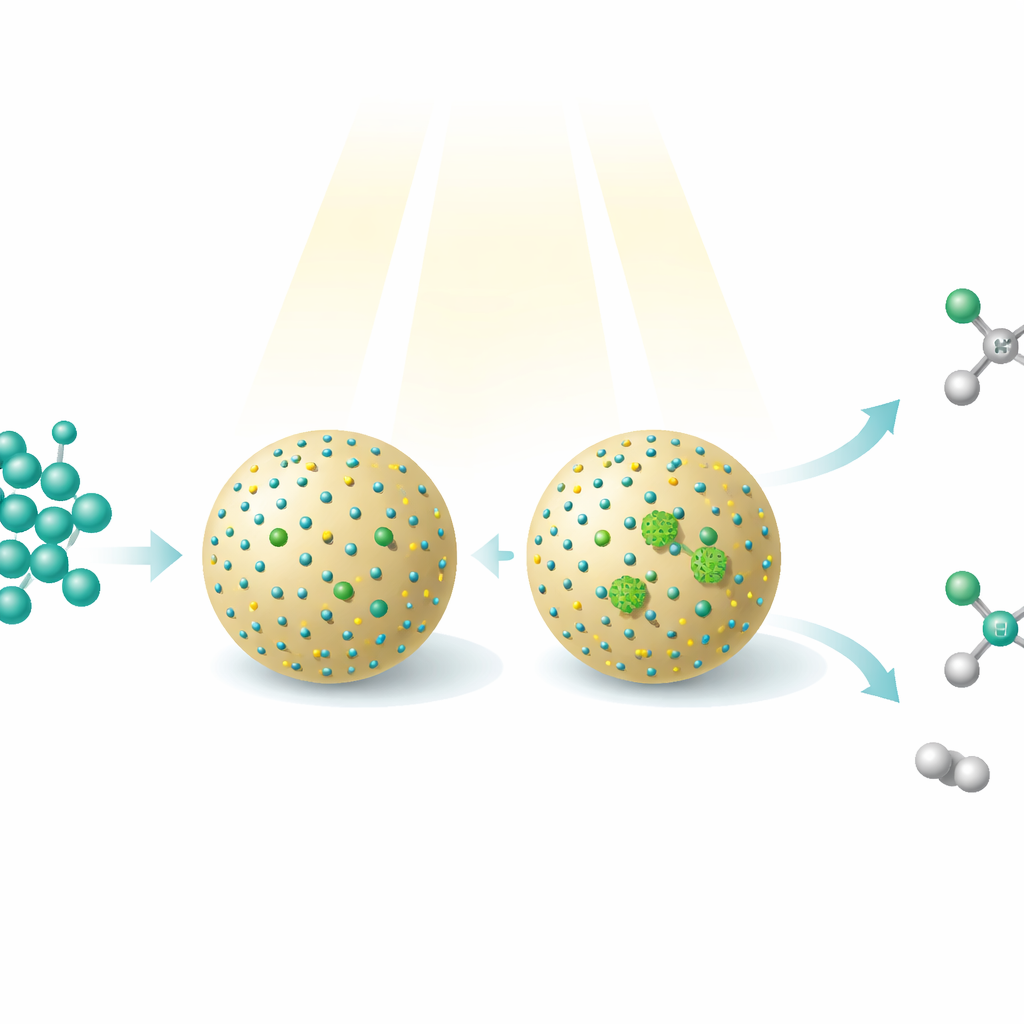
Почему важно улучшать метанол
В условиях поиска альтернатив нефти метанол стал привлекательным жидким носителем энергии и углерода. Однако большинство промышленных процессов превращения метанола в более крупные молекулы — грубые инструменты: они требуют высоких температур, зависят от ископаемых источников и часто дают множество нежелательных побочных продуктов. Химики стремятся с высокой точностью сцеплять молекулы метанола, чтобы селективно получать лишь желаемые соединения. Выполнение этого при мягких условиях с использованием света вместо тепла упростило бы интеграцию химического производства с возобновляемыми источниками энергии.
Работу выполняют светоактивные нановезикули
Исследователи создали фотокатализатор — буквально светоуправляемый катализатор — нанеся крошечные квантовые точки сульфида кадмия на шарообразные частицы диоксида кремния. Эти квантовые точки поглощают свет и создают возбужденные электроны и дырки, которые могут отрывать атомы водорода от метанола, формируя высокореакционноспособные фрагменты. На квантовые точки затем наносили атомы никеля двумя различными способами. В одном материале никель существовал преимущественно в виде изолированных одиночных атомов; в другом — формировал очень маленькие кластеры из нескольких атомов. Хотя общий состав почти не менялся, это тонкое различие в расположении никеля кардинально меняло реакции на поверхности.
Два дизайна никеля — два чистых продукта
Когда катализатор с одиночными атомами никеля облучали в метаноле, он предпочитал соединять два одинаковых фрагмента, происходящих от метанола, что приводило в основном к этиленгликолю — двухуглеродному диолу, широко используемому в антифризах и пластиках. Этот путь достиг примерно 90% селективности, то есть почти весь превращённый метанол образовывал именно этот продукт, а водородный газ выделялся в сопоставимых количествах из удалённых атомов водорода. Напротив, катализатор с никелевыми кластерами направлял те же фрагменты метанола по другой траектории. Здесь одна часть метанола подвергалась дальнейшему окислению до короткоживущего интермедиата, похожего на формальдегид, который затем соединялся с другим фрагментом, образуя глиоксаль — ещё одно двухуглеродное соединение с широким применением в тонкой химии и потенциально в биоориентированных процессах. Этот путь давал глиоксаль с 96% селективностью, также сопровождаясь выделением водорода. Кремнезёмная опора помогала квантовым точкам эффективнее собирать свет и делала частицы более устойчивыми при многократном использовании. 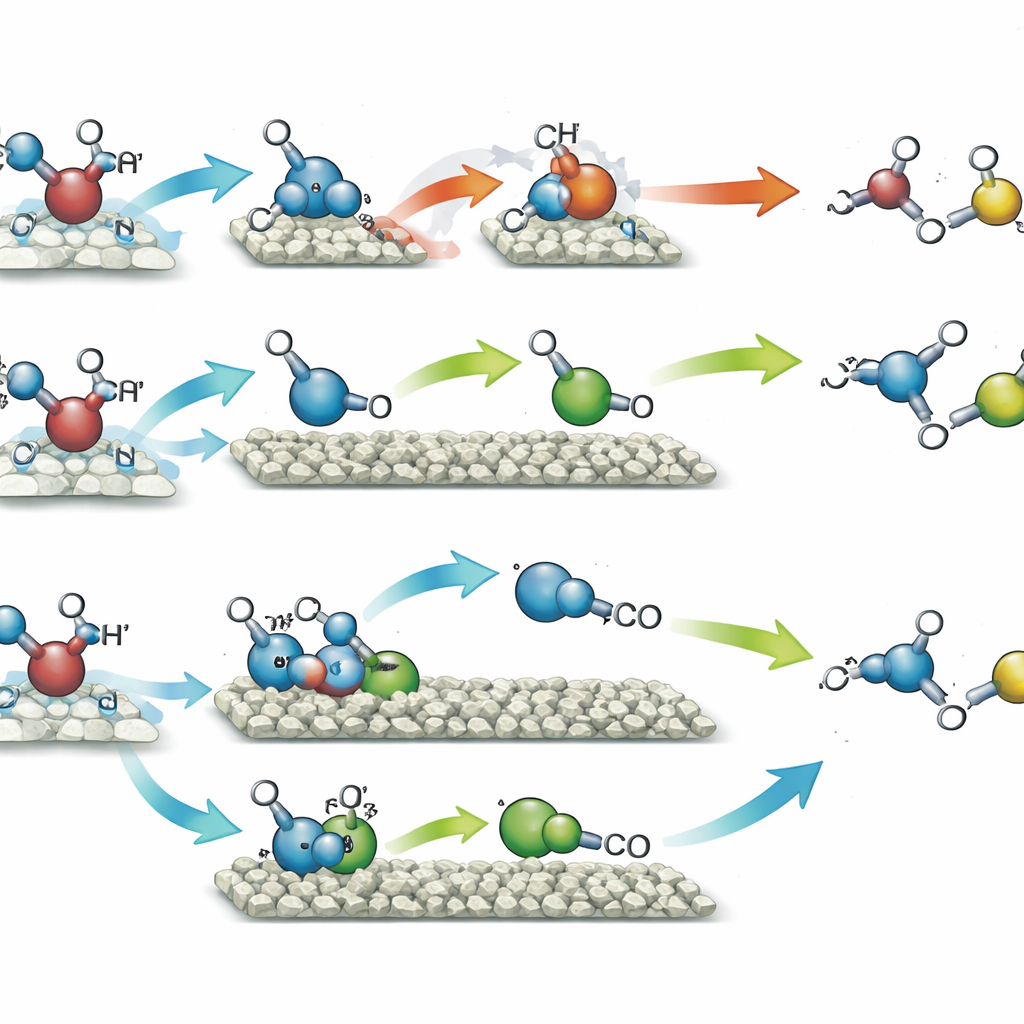
Заглядывая в механизм реакции
Чтобы понять, почему два варианта расположения никеля вели себя столь по-разному, команда совместила ряд передовых измерений с компьютерным моделированием. Эксперименты электронного парамагнитного резонанса показали, что оба катализатора генерируют радикалы на основе метанола под светом, но катализатор с кластерами также способствовал разрыву связи кислород–водород, что вело к более разнообразным реакционным фрагментам и к интермедиату типа формальдегида. Временнóй анализ подтвердил, что концентрация этого интермедиата сначала возрастала, а затем падала по мере его превращения в глиоксаль. Квантово-химические расчёты проложили энергетические траектории каждого шага. На одиночных атомах никеля прямое объединение двух одинаковых радикалов в этиленгликоль было самым лёгким пути. На никелевых кластерах та же связь продукта с поверхностью оказывалась слишком сильной, затрудняя его отделение, тогда как путь, в котором сначала образуется асимметричный интермедиат, а затем глиоксаль, становился энергетически предпочтительным.
Новый рычаг для более чистого химического производства
Проще говоря, эта работа показывает: «где» расположен каждый атом никеля на наноуровне может определять, «во что» превратится метанол при облучении светом. Переключаясь между одиночными атомами и малыми кластерами никеля, исследователи могут менять основной продукт с этиленгликоля на глиоксаль, при этом оба получаются эффективно и чисто вместе с водородным топливом. Эта стратегия проектирования катализаторов «атом за атомом» предлагает перспективный путь для апгрейда простых возобновляемых исходных материалов, таких как метанол, в ряд полезных химикатов без опоры на нефть, суровые условия или расточительные побочные реакции.
Цитирование: Qi, MY., Tan, CL., Tang, ZR. et al. Efficient methanol upcycling to ethylene glycol and glycolaldehyde via divergent C−C coupling synthesis. Nat Commun 17, 2835 (2026). https://doi.org/10.1038/s41467-026-69656-x
Ключевые слова: апсайклинг метанола, фотокатализ, одиночные атомы никеля, этиленгликоль, глиоксаль