Clear Sky Science · ru
Подписи включения экзонов позволяют точно оценивать активность факторов сплайсинга
Чтение скрытых меток редактирования клетки
Каждая клетка в нашем организме постоянно редактирует свои РНК-сообщения перед тем, как превращать их в белки. Это редактирование, называемое сплайсингом, помогает определить, останется ли клетка здоровой или превратится в раковую. Исследование, лежащее в основе этой статьи, показывает, что при внимательном анализе того, какие участки РНК сохраняются или пропускаются — так называемых подписей включения экзонов — учёные могут с высокой точностью восстановить активность молекулярных «редакторов», контролирующих сплайсинг, даже в сложных заболеваниях, таких как рак.
Как клетки вырезают и склеивают свои сообщения
Гены считываются не одним непрерывным фрагментом. Клетки удаляют некодирующие участки и соединяют кодирующие куски, известные как экзоны, чтобы получить окончательные РНК-сообщения. Специализированные белки — факторы сплайсинга — направляют этот процесс вырезания и склейки, решая, какие экзоны будут включены. Их поведение регулируется множеством уровней: сколько их собственной РНК и белка производится, какие химические модификации они несут, где они расположены в клетке и как взаимодействуют с другими белками. Поскольку на поведение факторов сплайсинга влияет так много рычагов, простое измерение одного типа данных — например экспрессии генов — часто не отражает их реальной активности.
Преобразование паттернов экзонов в показатели активности
Вдохновлённые предыдущими работами по факторам транскрипции, авторы предлагают иной подход: вместо прямого измерения факторов сплайсинга считывать их активность по эффектам. Когда активность фактора меняется, включение его таргетных экзонов смещается по узнаваемым шаблонам. Команда собрала сотни экспериментов, в которых отдельные факторы сплайсинга были вытеснены, выведены из строя или сверхэкспрессированы, и использовала эти данные для построения «эмпирических сетей», связывающих каждый фактор с экзонами, на которые он явно влияет. Затем они адаптировали вычислительную схему под названием VIPER, чтобы прочитать новую подпись включения экзонов и оценить, какая активность каждого фактора необходима для объяснения наблюдаемой картины.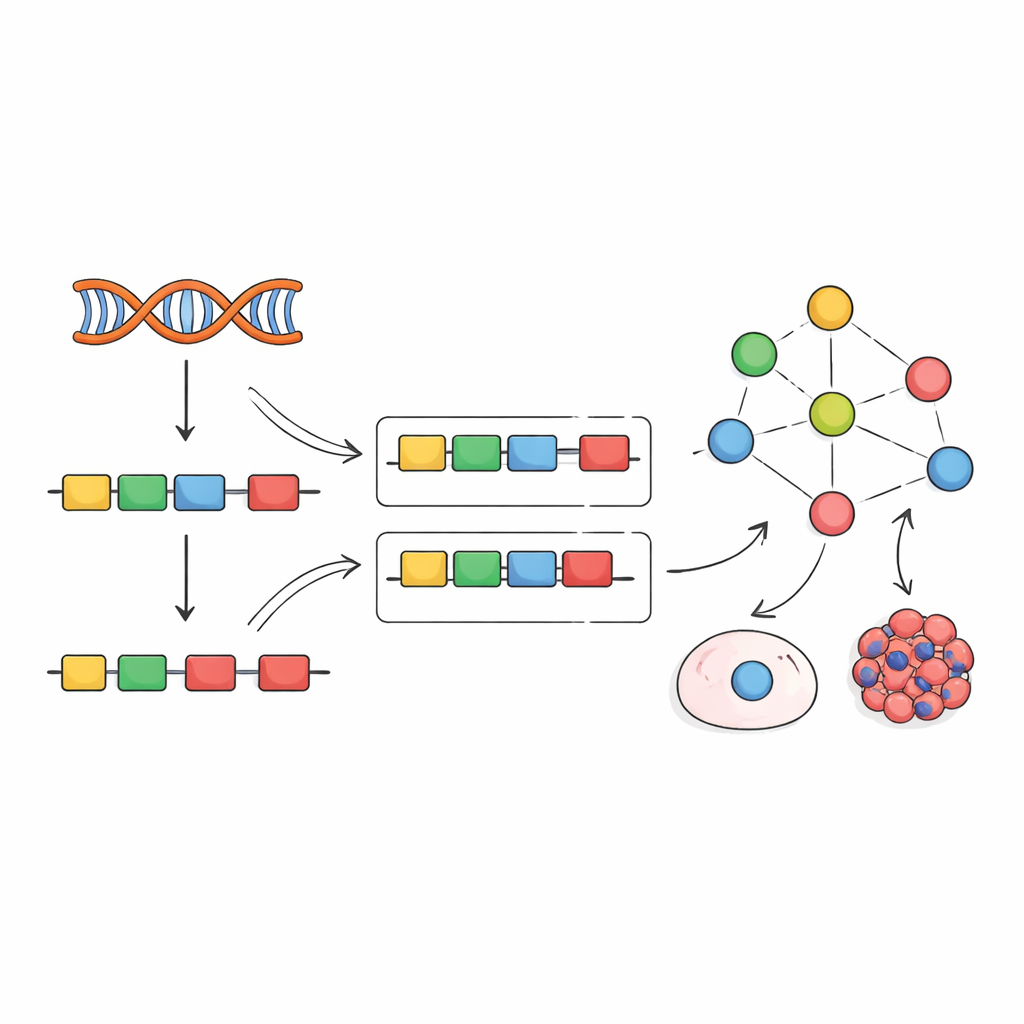
Тестирование метода на реальных возмущениях
Чтобы проверить работоспособность подхода, исследователи сравнили несколько способов построения сетей и вычисления показателей активности. Эмпирические сети, выведенные напрямую из экспериментов с возмущениями в сочетании с анализом обогащения VIPER, явно превосходили альтернативы, основанные только на статистическом выводе. Метод в большинстве тестов правильно идентифицировал экспериментально возмущённый фактор сплайсинга, даже при переходе между разными типами клеток и исследованиями. Он также захватил более тонкие механизмы регуляции. Например, противораковый препарат Индисулем вызывает деградацию белка фактора сплайсинга RBM39, в то время как уровни его РНК растут, что похоже на попытку компенсации. Традиционный анализ экспрессии вводил бы в заблуждение, показывая повышенную активность RBM39, тогда как оценка на основе экзонов корректно выявила сильную потерю функции, соответствующую известному действию препарата.
Выявление скрытых программ сплайсинга в раке
Вооружившись этим инструментом, авторы обратились к проекту The Cancer Genome Atlas, проанализировав данные на уровне экзонов из нескольких типов опухолей и соответствующих здоровых тканей. Они обнаружили две широкие и повторяющиеся программы сплайсинга. Одна программа объединяет факторы, которые в опухолях, как правило, более активны и связаны с худшей выживаемостью пациентов — подобие онкогенной программы. Другая включает факторы, систематически менее активные в опухолях и связанные с лучшими исходами, напоминая супрессорную программу. Эти программы затрагивают гены, вовлечённые в ключевые признаки рака, такие как быстрый клеточный цикл и способность опухолей скрываться от иммунной системы. Например, некоторые экзоны, регулируемые программой, похожей на опухолевый супрессор, по-видимому, влияют на то, насколько хорошо пациенты отвечают на терапию ингибиторами контрольных точек иммунитета, указывая на новые маркёры или точки вмешательства.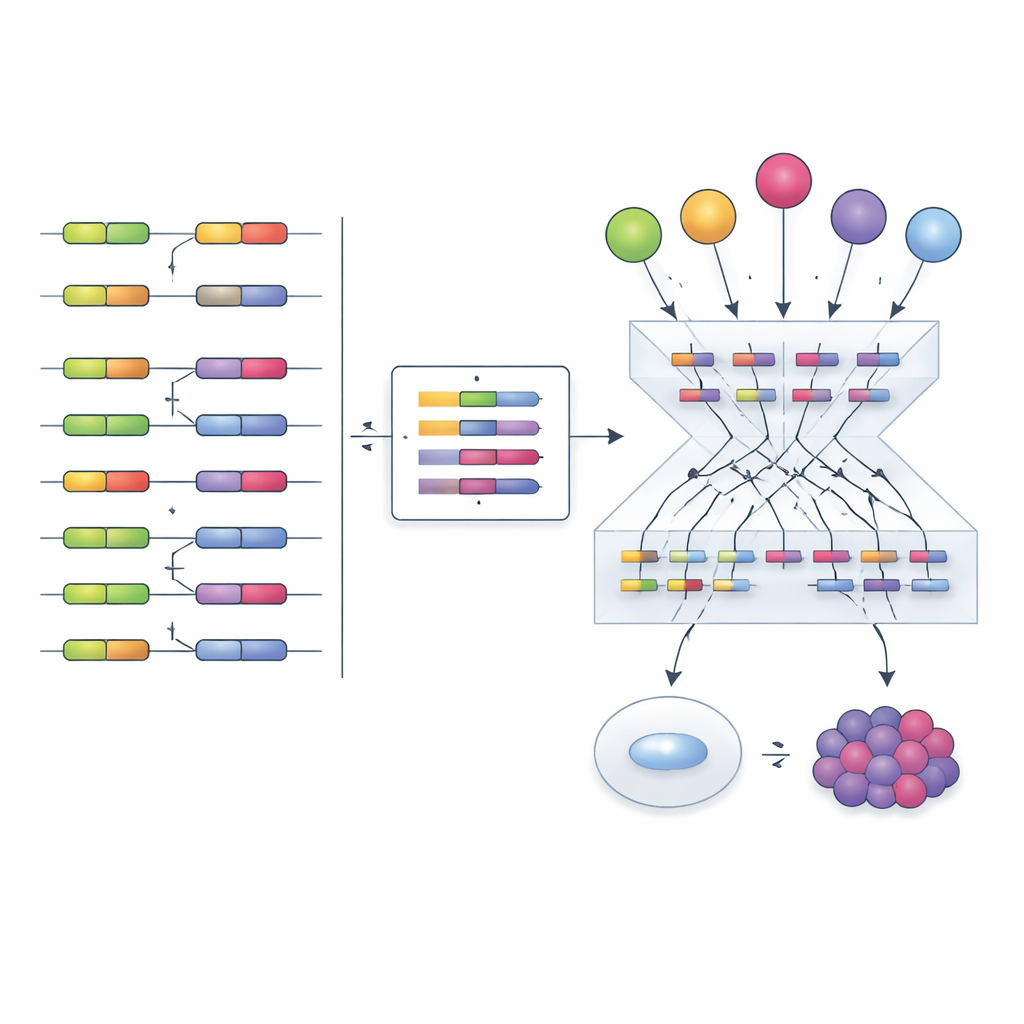
Отслеживание изменений сплайсинга на пути к раку
Команда также изучила пошаговую модель человеческих клеток, прогрессирующих от нормального состояния к бессмертному, опухлеобразующему и, в конечном счёте, метастазирующему состоянию. Они обнаружили, что онкогенная подобная программа сплайсинга становится более активной по мере накопления клетками мутаций, приводящих к раку, в то время как программа, похожая на супрессор опухолей, угасает. Интегрируя несколько слоёв данных — уровни РНК, количество белка, химические модификации и изменения сплайсинга в самих факторах — они выделили ограниченный набор кандидатных молекулярных событий, которые могут вызывать сдвиги этих программ, предложив приоритетный список для дальнейших экспериментальных проверок.
Почему это важно для пациентов и будущих исследований
По сути, исследование демонстрирует, что сложное поведение факторов сплайсинга можно свести к единому, интерпретируемому показателю активности, выведенному из того, как экзоны включаются или пропускаются. Это делает возможным изучение регуляции сплайсинга в больших когортах пациентов и в разнообразных экспериментах, используя только стандартные данные РНК-секвенирования, без необходимости дорогого многослойного профилирования. Для неспециалиста ключевая мысль такова: паттерны того, как гены вырезаются и склеиваются, содержат богатую информацию о скрытых системах контроля клетки, и расшифровка этих паттернов может выявить новые драйверы рака, улучшить прогноз и помочь в поиске более точных терапевтических подходов.
Цитирование: Anglada-Girotto, M., Segura-Morales, C., Moakley, D.F. et al. Exon inclusion signatures enable accurate estimation of splicing factor activity. Nat Commun 17, 1994 (2026). https://doi.org/10.1038/s41467-026-69642-3
Ключевые слова: РНК-сплайсинг, факторы сплайсинга, геномика рака, транскриптомика, вывод активности белков