Clear Sky Science · ru
Генная инженерия микроокружения опухоли с помощью LOAd703 в сочетании с атезолизумабом при метастатической меланоме: клиническое исследование фазы I/II
Почему это новое исследование меланомы важно
Для людей с распространённой кожной меланомой, переставшей реагировать на современные мощные иммунотерапии, варианты лечения ограничены и часто тяжёлы. В этом исследовании проверяется другая идея: вводить прямо в опухоли генетически модифицированный вирус совместно с уже существующим препаратом, усиливающим иммунитет, чтобы активировать защиту организма и вернуть контроль над раком. Ранние результаты показывают, что такой подход можно применять безопасно и он может помочь заметной доле пациентов, у которых ранее болезнь не поддавалась стандартной терапии.
Упрямая форма рака кожи, перехитрившая лечение
Меланома — один из наиболее распространённых серьёзных раков кожи в западных странах, и её распространённость резко выросла за последние десятилетия. Современные препараты, снимающие тормоза с Т‑клеток (ингибиторы контрольных точек), изменили прогнозы, увеличив пятилетнюю выживаемость при продвинутой меланоме примерно до половины пациентов. Тем не менее многие опухоли со временем перестают отвечать. Часто такие резистентные опухоли окружены «холодным» микросредой — клетками и молекулами, которые не пропускают иммунные клетки или подавляют их. Поиск способов перепрограммировать это микроокружение, чтобы Т‑клетки снова могли распознавать и атаковать рак, остаётся приоритетной областью исследований.
Вирус, созданный для перепрограммирования опухолевого окружения
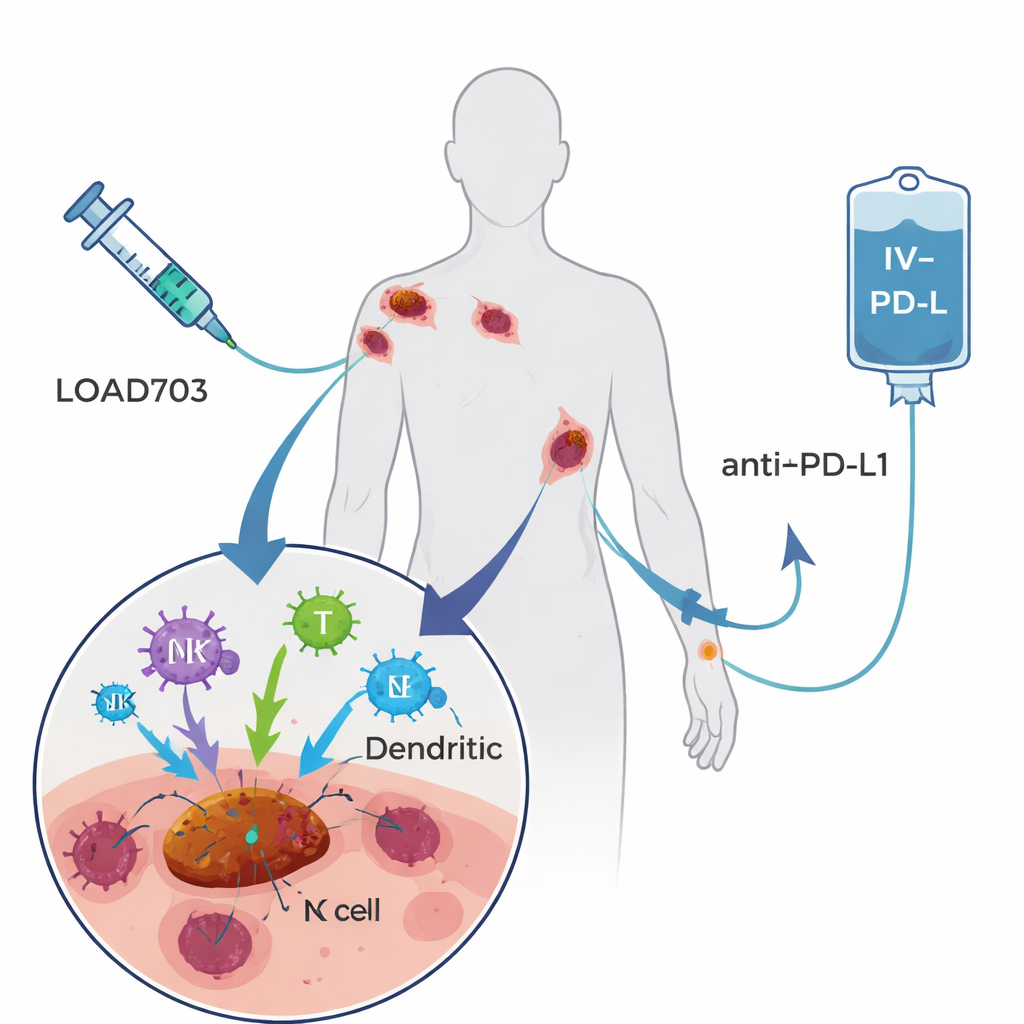
Испытанное здесь средство LOAd703 — это модифицированный аденовирус, тип обычного вируса простуды, сконструированный для двух задач. Во‑первых, он предпочитательно реплицируется в опухолевых клетках и разрушает их — стратегия, известная как онколитическая вирусная терапия. Во‑вторых, он несёт генетические инструкции для двух мощных иммуностимулирующих сигналов, экспрессируемых на инфицированных клетках. Эти сигналы, CD40L и 4‑1BBL, способствуют созреванию профессиональных «сторожевых» клеток иммунитета (дендритных клеток) и презентации фрагментов опухоли, а также укрепляют и расширяют популяции Т‑клеток и натуральных киллеров, борющихся с раком. Пациенты в исследовании получали LOAd703, вводимый непосредственно в одну или несколько опухолей каждые три недели, вместе с атезолизумабом — зарегистрированным антительный препаратом, вводимым внутривенно и блокирующим тормоз PD‑L1 на Т‑клетках. Надежда заключалась в том, что вирус превратит опухоли в фабрики по производству ауто‑вакцин в организме, а антитело будет поддерживать активность реанимированных Т‑клеток.
Кого лечили и каков был результат
В фазу I/II было включено 24 человека с меланомой стадии IV, у которых заболевание явно прогрессировало несмотря по крайней мере на одно предыдущее лечение ингибитором PD‑1; многие уже получали несколько линий иммунотерапии и таргетной терапии. Были исследованы два уровня дозы вируса. В целом сочетание переносилось хорошо. Наиболее частые побочные эффекты, связанные с вирусом — лихорадка, озноб, тошнота и подобные гриппу симптомы — в большинстве случаев были лёгкими и временными. Только у двух пациентов на более высокой дозе возникли более серьёзные, но обратимые реакции, и никому не пришлось прекращать лечение из‑за проблем, связанных с вирусом. При оценке ответов опухолей у четырёх пациентов (17%) наблюдалось измеримое уменьшение опухолей, а у более половины больных сохранялась по крайней мере стабильность заболевания в течение некоторого времени. Через два года после включения в исследование почти половина участников оставалась в живых, в том числе некоторые, чьи сканы показали длительный контроль или полное исчезновение обнаруживаемой болезни после окончания терапии.
Сигналы повторной активации иммунной системы
Чтобы понять, что происходило внутри опухолей и в крови, исследователи проанализировали биопсии тканей и образцы крови, взятые до лечения и примерно через девять недель после начала терапии. В инъецированных опухолях наблюдалась повышенная активность генов, связанных с тип‑1 иммунными ответами, включая маркеры активированных Т‑клеток и натуральных киллеров, а также молекулы, помогающие этим клеткам проникать в опухоль из соседних кровеносных сосудов. Увеличились сигналы, связанные с презентацией антигенов — процессом, в котором фрагменты опухоли демонстрируются Т‑клеткам, что свидетельствует о том, что вирусная терапия переводила микроокружение опухоли из подавляющего в более благоприятное для иммунитета. В крови после терапии повысились несколько иммунных белков, включая сам PD‑L1, что согласуется с широкой активацией иммунных путей. Пациенты с более длительной выживаемостью, как правило, демонстрировали генные профили, связанные с мощной функцией Т‑клеток и антивирусной защитой, тогда как у тех, кто пережил меньше, доминировали шаблоны, ассоциированные с супрессивными типами клеток и сигналами ремоделирования ткани.
Что это может значить для будущей помощи пациентам
Это было небольшое исследование с одной веткой и без контрольной группы, поэтому показатели выживаемости и ответов нужно интерпретировать осторожно. Тем не менее сочетание хорошей переносимости, иммунной активации в опухолях и обнадеживающего контроля болезни у сильно предварительно леченных пациентов намекает, что генетически модифицированные онколитические вирусы, такие как LOAd703, могут помочь заново сделать меланому чувствительной к блокаде контрольных точек — или даже удерживать опухоли под контролем самостоятельно. Результаты обосновывают проведение больших контролируемых испытаний, возможно в комбинации с дополнительными иммунотерапевтическими препаратами, чтобы уточнить, какие пациенты получают наибольшую пользу и как лучше интегрировать эту стратегию в лечение меланомы.
Цитирование: Hamid, O., Ekström-Rydén, V., Mehmi, I. et al. LOAd703-induced tumor microenvironment gene engineering in combination with atezolizumab in metastatic malignant melanoma: a phase I/II trial. Nat Commun 17, 1760 (2026). https://doi.org/10.1038/s41467-026-69629-0
Ключевые слова: меланома, иммунотерапия, онколитический вирус, микроокружение опухоли, резистентность к ингибиторам контрольных точек