Clear Sky Science · ru
Лекарства в «клетках» позволяют фото-каталитически одновременно освобождать оксид азота и анестетики для антибактериального обезболивания
Борьба с микробами и болью одновременно
Бактериальные инфекции угрожают не только нашему здоровью — они ещё и причиняют сильную боль. Стандартные методы лечения обычно нацелены на уничтожение микробов, но оставляют пациентов с отдельными обезболивающими, которые могут быстро перестать действовать или вызвать побочные эффекты. В этом исследовании предложен препарат, управляемый светом, который стремится одновременно убивать бактерии и облегчать боль в одном скоординированном шаге, открывая путь к более умному и комфортному лечению инфекций.
Идея «два в одном»
Исследователи построили подход вокруг тетракаина — известного местного анестетика, применяемого для обезболивания кожи и нервов. Они химически присоединили оксид азота, небольшую молекулу газа, известную своими сильными антибактериальными и противовоспалительными свойствами, к тетракаину. Получился «пролекарство» под названием TTC-NO, которое в основном неактивно до тех пор, пока не будет запущено. TTC-NO затем упаковали вместе со светочувствительным вспомогательным веществом в крошечные полимерные пузырьки — мицеллы, способные перемещаться в водной среде, такой как кровь или тканевая жидкость. 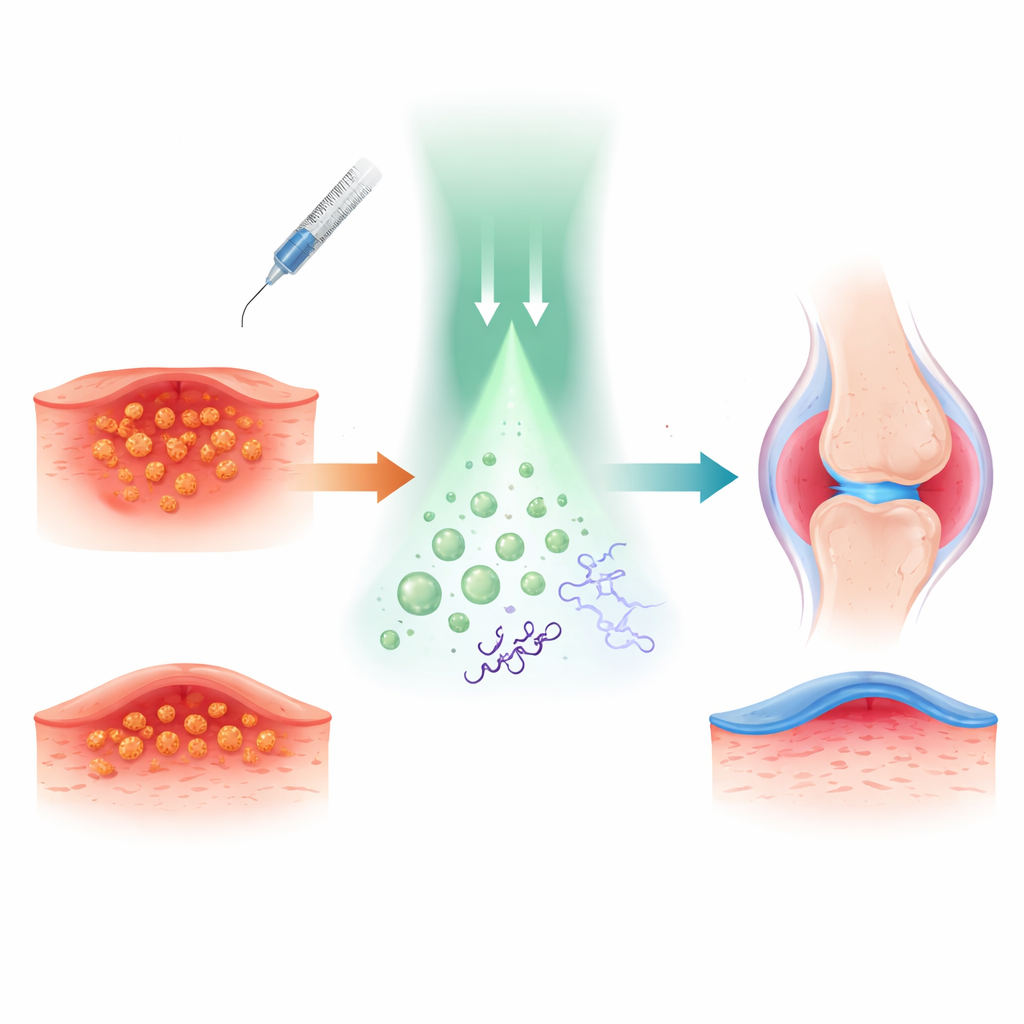
Включение препарата мягким светом
Чтобы понять, как работает этот световой переключатель, команда изучала химию в растворе. Они показали, что фотокатализатор на основе иридия может при освещении зелёным светом передавать электрон на TTC-NO. Это ослабляет определённую связь, вызывая освобождение оксида азота и восстановление тетракаина до активной формы. Измерения спектроскопией и хроматографией подтвердили, что при этих условиях TTC-NO почти полностью превращается в тетракаин и оксид азота, оставаясь практически неизменным в темноте. Когда оба компонента были инкапсулированы в мицеллы, частицы сохраняли стабильность — примерно 80 нанометров в диаметре — и высвобождали содержимое только при облучении, что доказывает возможность внешнего управления концепцией «лекарство в клетке» с помощью света.
Ускорение заживления инфицированных ран
Далее команда перешла к исследованиям на мышах с кожными ранами, преднамеренно инфицированными метициллин-резистентным Staphylococcus aureus (MRSA), проблемным госпитальным штаммом. Часть ран получала стандартные лечения, такие как антибиотик или фактор роста, другие — мицеллы TTC-NO, с облучением или без него. При включённом свете система TTC-NO резко снижала количество бактерий, уменьшала воспаление, способствовала образованию новых кровеносных сосудов и увеличивала отложение коллагена — всё это важно для правильного восстановления. Такие раны заживали быстрее и полнее, чем раны, получавшие только тетракаин или мицеллы в темноте, и по эффективности сравнивались с передовым антибиотиком. Важно, что проверки безопасности не выявили серьёзных повреждений органов или нарушений в показателях крови.
Облегчение боли и подавление нервных сигналов
Поскольку инфекция и повреждение тканей сильно активируют болевые пути, учёные тщательно измеряли поведение, связанное с болью, в той же модели ран. Традиционный тетракаин временно повышал порог силы, необходимой для вызова болевой реакции, но эффект исчезал через несколько часов. Напротив, мицеллы TTC-NO, активированные светом, обеспечивали облегчение до 12 часов. Микроскопические исследования нервных узлов рядом с спинным мозгом и записи активности в сенсорной коре мозга показали, что комбинированное лечение подавляло разрядную активность ноцицептивных нейронов долго после того, как чистый тетракаин утрачивал эффект. Дальнейшие эксперименты указывали, что удлинение действия связано с уменьшением бактериальной нагрузки и воспаления за счёт оксида азота, а не только с блокадой нервов.
Защита болезненных инфицированных суставов
Исследователи также проверили систему на мышах с септическим артритом — тяжёлой MRSA-инфекцией внутри коленного сустава, вызывающей отёк, потерю кости и сильную боль. Мицеллы TTC-NO, активированные светом, уменьшали ширину сустава, сокращали количество бактерий и защищали структуру кости, что было видно на высокоразрешающих снимках. Уровни вредных провоспалительных молекул в крови снижались, в то время как защитные сигнальные молекулы повышались. По поведению обработанные мыши выносливее переносили механическое давление на поражённую лапу и активнее перемещались в открытой арене, снова демонстрируя более длительное облегчение по сравнению с тетракаином. Измерения в нервах и мозге соответствовали этим поведенческим улучшениям, указывая на широкое подавление болевых путей без очевидной местной или системной токсичности. 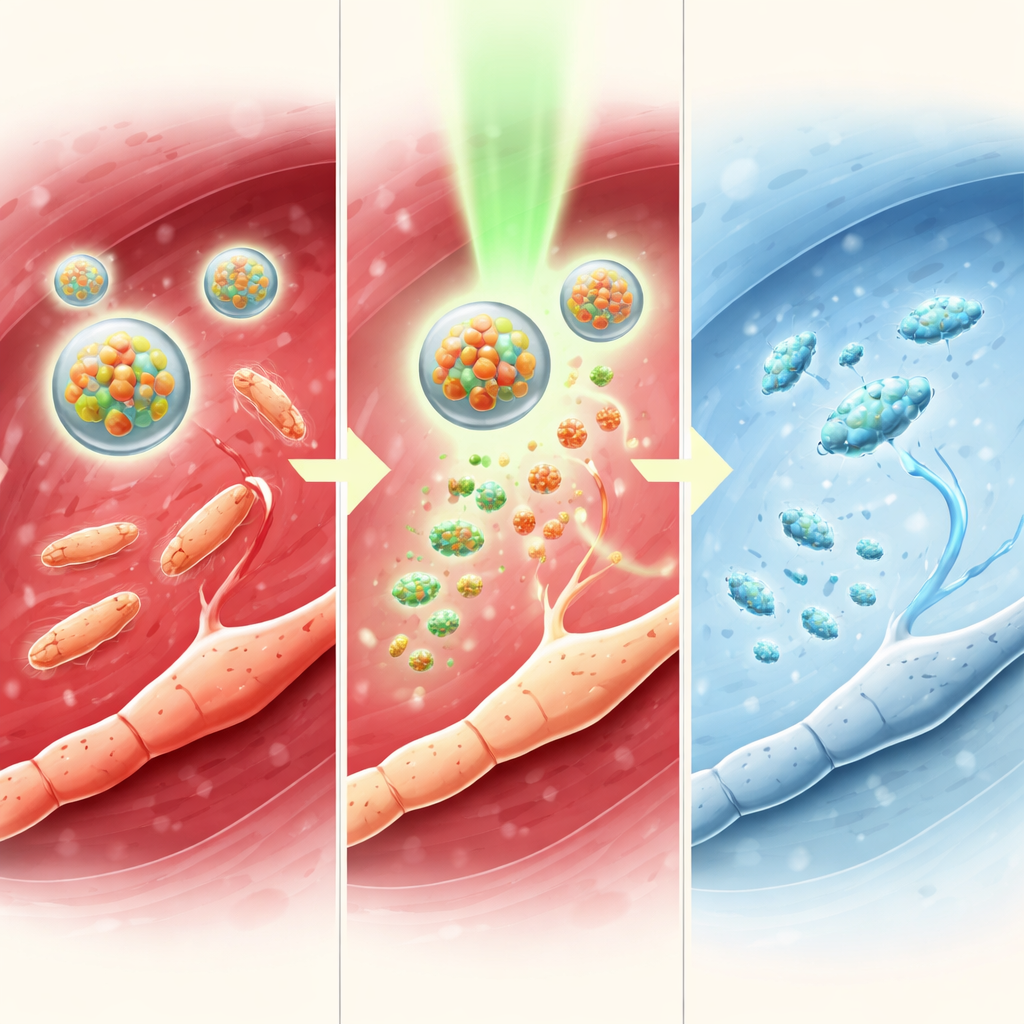
Что это может значить для пациентов
В сумме работа демонстрирует единый светоактивируемый наносистема, которая способна как устранять упорные бактериальные инфекции, так и значительно снижать сопутствующую боль. Химически «заперев» анестетик внутри структуры, высвобождающей оксид азота, и упаковав всё в мицеллы, авторы добились локализованного и управляемого по требованию высвобождения двух полезных агентов при помощи мягкого видимого света. В моделях животных с кожными ранами и суставными инфекциями этот дизайн ускоряет заживление и продлевает обезболивание по сравнению с традиционным местным анестетиком. Хотя до применения у человека ещё предстоит множество испытаний, исследование подчёркивает, как умные переключаемые лекарства однажды могут сделать лечение инфекций более эффективным и комфортным.
Цитирование: Zhang, J., Gan, G., Cao, C. et al. Drug-caged drugs enable photocatalytic dual decaging of nitric oxide and anesthetics for antibacterial analgesia. Nat Commun 17, 2843 (2026). https://doi.org/10.1038/s41467-026-69624-5
Ключевые слова: терапия оксидом азота, светочувствительные препараты, антибактериальное обезболивание, наномедицина, инфекции MRSA