Clear Sky Science · ru
Пиримидинергическая кальциевая сигнализация связывает тубулярный метаболизм с фиброзом при заболевании почек
Почему рубцевание почек важно
Хроническая болезнь почек незаметно затрагивает сотни миллионов людей во всем мире и часто заканчивается образованием рубцов и утратой упругости тканей. Как только развивается этот рубцевый процесс, называемый фиброзом, восстановить утраченную функцию почек очень сложно. При этом у врачей по‑прежнему нет препаратов, целенаправленно останавливающих фиброз. В этой работе задают базовый, но ключевой вопрос: каким образом кратковременное повреждение фильтрующих канальцев почки постепенно превращается в стойкую рубцовую ткань и можно ли, прерывая эту цепочку событий, замедлить или предотвратить почечную недостаточность?
Жизненная активность канальцев и их скрытая химия
Проксимальные канальцы почки — это микроскопические «трудяги», возвращающие большую часть воды и питательных веществ, отфильтрованных из крови. Для выполнения этой работы их биохимия необычайно интенсивна. Анализ данных о экспрессии генов в отдельных клетках мышиных почек показал, что эти клетки особенно богаты генами, участвующими в обмене пиримидинов — семейства небольших молекул, обычно задействованных в синтезе и ремонте ДНК и РНК. В поврежденных канальцах один фермент пути «восстановления», цитидиндезаминаза, оказался сильно повышен, что предполагает, что поврежденные клетки перестраивают использование пиримидинов, чтобы поддерживать запасы некоторых энергоёмких строительных блоков, включая соединение UDP.
Сигналы, вытекающие из повреждённых клеток
Когда команда повреждала в культуре человеческие клетки, похожие на канальцевые, токсинами, имитирующими химиотерапию или передозировку фолиевой кислотой, клетки выделяли UDP в окружающую среду. В действительных мышиных почках, подвергшихся повреждению, окрашивание срезов показало как высокие уровни фермента, обрабатывающего пиримидины, в канальцах, так и признаки пробуждения соседних опорных клеток — фибробластов, которые меняют форму. Фибробласты в норме сидят между канальцами в относительном покое, но при активации они размножаются и помогают откладывать коллаген и другие волокна, утолщающие и уплотняющие почечную ткань. Эти наблюдения наводили на простую идею: повреждённые канальцы могут «выплёскивать» химические сигналы бедствия, которые улавливают соседние фибробласты.
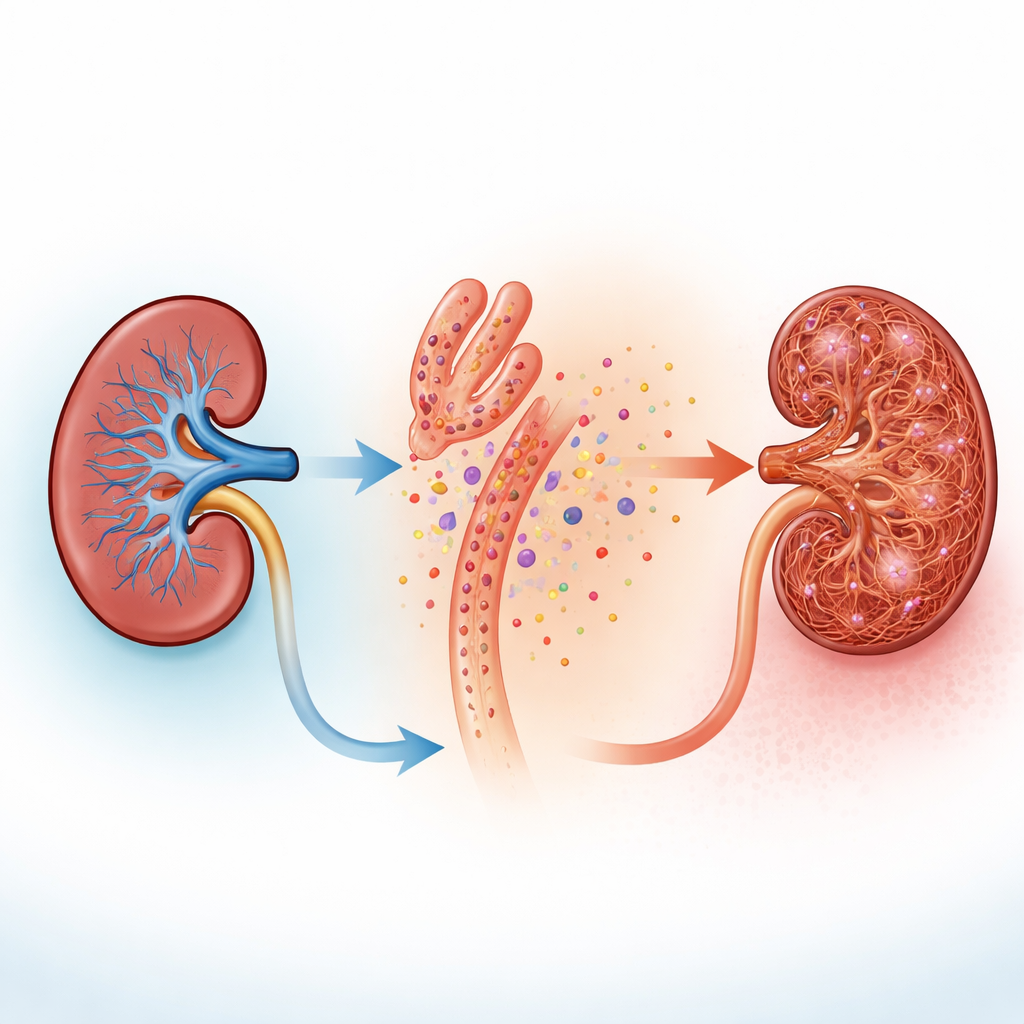
Как фибробласты слушают с помощью кальциевых вспышек
Предполагаемыми «ушами» фибробластов стали рецепторы P2Y6 — белки на поверхности, реагирующие на UDP. Анализ нескольких наборов данных по отдельным клеткам показал, что P2Y6 присутствует в стромальных клетках и усиливается в моделях хронической болезни почек у мышей. Измерения по целым почкам подтвердили значительное повышение уровня P2Y6 в двух разных моделях фиброза. В свежих срезах почек и в культивируемых почечных фибробластах, генетически модифицированных так, чтобы светиться при подъёме внутриклеточного кальция, добавление UDP или препарата, активирующего P2Y6, вызывало быстрые всплески кальция. Эти вспышки начинались в длинных тонких отростках, опоясывающих канальцы, затем охватывали тело клетки и исчезали при блокаде P2Y6 или химическом «поглощении» кальция. В живых мышах высокоразрешающая интравитальная микроскопия показала, что фибробласты вокруг канальцев демонстрируют частую, нерегулярную кальциевую активность, которая резко усиливается при повреждении канальцев, даже когда сами клетки канальцев становятся малоактивными.
От кратких сигналов к стойким рубцам
Внутриклеточные всплески кальция — это не просто фейерверк; они могут перенастраивать поведение клетки. Когда культивируемые фибробласты подвергали действию активатора P2Y6, они быстрее размножались, активнее передвигались и включали гены, связанные с более агрессивным «миофибробластным» состоянием. Эти гены кодируют белки, такие как фибронектин, виментин и коллаген, которые непосредственно способствуют формированию рубца. Блокада P2Y6 или предотвращение подъёма кальция устраняли эти изменения, а подавление гена рецептора ослабляло ответ. У мышей две различные формы повреждения почек — обструкции мочеточника и нефропатия, вызванная фолиевой кислотой — демонстрировали одинаковую картину: в повреждённых почках было больше пролиферирующих фибробластов, больше маркеров миофибробластов, больше коллагена и большие области фиброза.
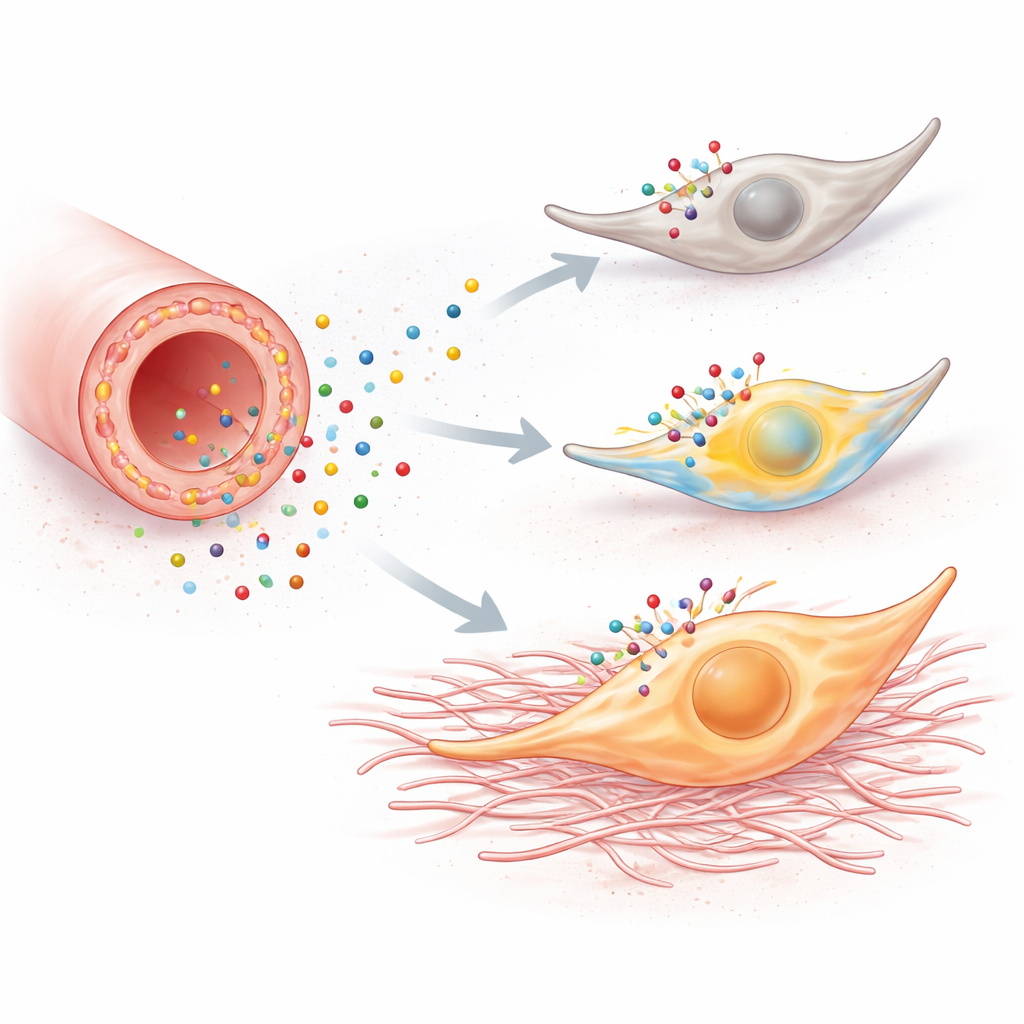
Снижение вредной сигнализации
Чтобы проверить, действительно ли этот путь вреден, исследователи либо удаляли P2Y6 генетически, либо блокировали его лекарственным веществом. У мышей без рецептора развивалось меньше почечного фиброза после обструкции мочеточника или повреждения фолиевой кислотой: их фибробласты менее активно размножались, откладывали меньше волокнистого матрикса и привлекали меньше воспалительных клеток. Анализы крови показали, что у этих нокаутных животных сохранялась лучшая фильтрационная функция почек. Лечение обычных мышей препаратом, блокирующим P2Y6, давало сопоставимую защиту, включая ослабление кальциевой активности фибробластов и уменьшение рубцевания, хотя улучшения системных маркеров крови были более переменными.
Что это значит для будущего терапии
В сумме работа выявляет простую, но мощную цепочку событий. Когда клетки канальцев почки повреждаются, они перестраивают внутренний метаболизм и выделяют UDP в окружающие ткани. Ближайшие фибробласты обнаруживают эту молекулу через рецепторы P2Y6, реагируют вспышками внутриклеточного кальция и переключаются в режим, ведущий к образованию рубца — они размножаются, мигрируют и откладывают коллаген. Прерывание этой пиримидиновой кальциевой сигнализации, особенно на уровне P2Y6, значительно смягчает фиброз в нескольких мышиных моделях. Для пациентов это указывает на новый класс терапевтических мишеней: соединения, селективно блокирующие P2Y6 в почке, могут помочь разорвать связь между повседневными повреждениями канальцев и медленным, необратимым рубцеванием, ведущим к хронической болезни почек.
Цитирование: Figurek, A., Jankovic, N., Kollar, S. et al. Pyrimidinergic calcium signaling links tubular metabolism to fibrosis in kidney disease. Nat Commun 17, 3004 (2026). https://doi.org/10.1038/s41467-026-69602-x
Ключевые слова: хроническая болезнь почек, почечный фиброз, сигнализация фибробластов, пиримидиновый метаболизм, рецептор P2Y6