Clear Sky Science · ru
Двойной набор двух молекул CCM2 на KRIT1 подавляет экспрессию KLF4
Почему кровеносные сосуды мозга требуют тщательного контроля
Сосуды мозга находятся в тонком балансе: они должны быть достаточно прочными, чтобы не протекать, и в то же время достаточно гибкими, чтобы реагировать на потребности организма. Когда этот баланс нарушается, у человека могут развиться церебральные кавернозные мальформации — скопления хрупких, похожих на пузыри сосудов, которые могут кровоточить и вызывать судороги или инсульты. В этом исследовании раскрыт ранее неизвестный молекулярный «рукопожатие» между тремя белками, которое помогает поддерживать стабильность сосудов мозга, и показано, как разрушение этого взаимодействия может приводить к болезни.
Стражи здоровья сосудов
Клетки, выстилающие сосуды, полагаются на набор ключевых переключателей, называемых KLF2 и KLF4, которые контролируют гены, поддерживающие прочность и идентичность сосудов. Если эти переключатели чрезмерно активируются, сосуды становятся аномальными и уязвимыми для повреждений. Два других белка, KRIT1 и CCM2, известны как стражи этой системы. Люди, унаследовавшие дефектные версии любого из этих белков, имеют высокий риск развития церебральных кавернозных мальформаций. До настоящего времени учёные не понимали, как именно KRIT1 и CCM2 совместно удерживают KLF4 в пределах нормы.
Неожиданная команда из трёх
Исследователи использовали клетки, похожие на эндотелиальные, выращенные в лаборатории, и выборочно уменьшали количество CCM2 или KRIT1 с помощью генетических инструментов. При снижении любого из этих белков уровни KLF4 резко возрастали, что повторяло наблюдения в модельных организмах и у пациентов. Восстановление нормального уровня CCM2 или KRIT1 снижало KLF4 — но только если восстановленные белки могли по-прежнему связываться друг с другом. Путём точечного изменения областей взаимодействия CCM2 и KRIT1 команда показала, что этот физический контакт необходим, чтобы не допустить роста KLF4. Эти эксперименты чётко поставили партнёрство KRIT1–CCM2 в центр системы контроля этого важного фактора транскрипции.
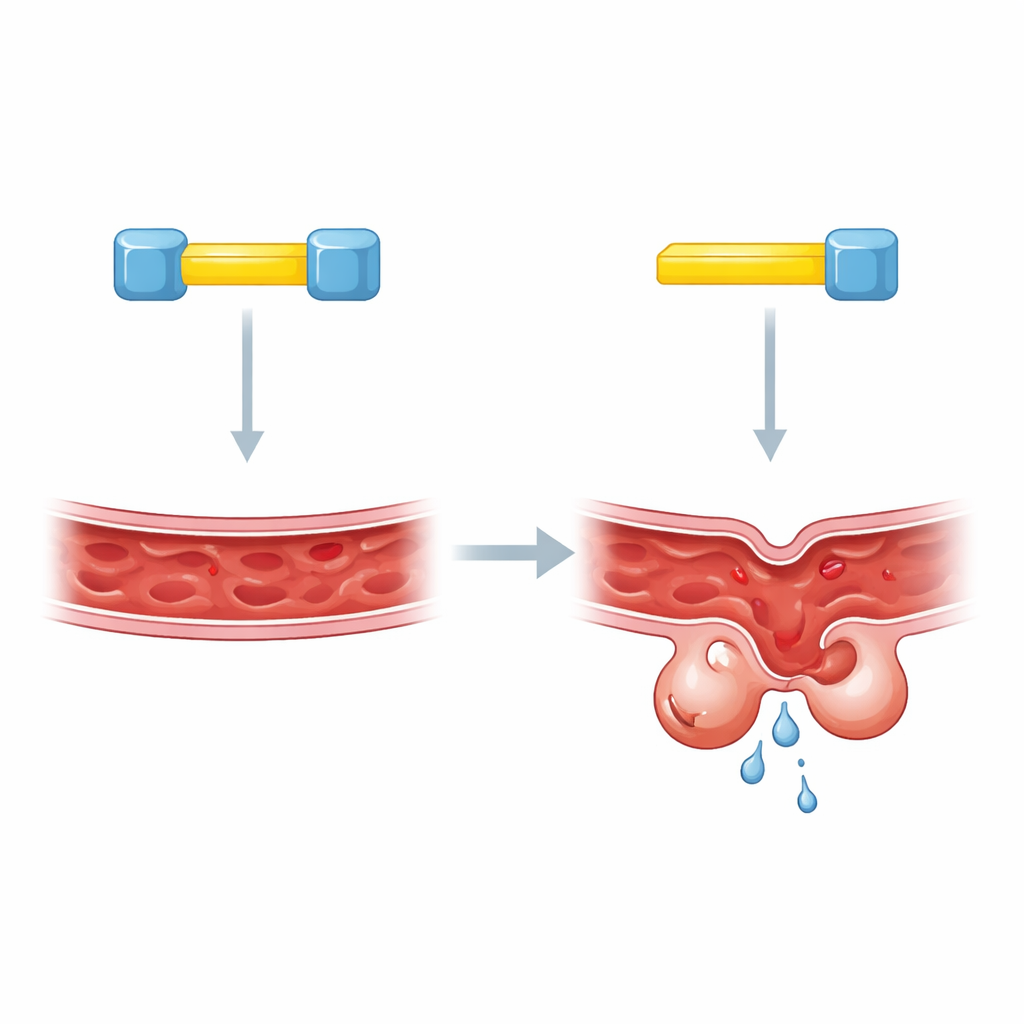
Два замка на один ключ
Чтобы разобраться глубже, авторы сосредоточились на коротких сегментах внутри KRIT1, которые функционируют как молекулярные докинг‑сайты. Предыдущие работы указывали, что CCM2 прикрепляется к KRIT1 в одном из этих сайтов, но разные методы давали противоречивые ответы, какой именно. Новое исследование показывает, что причина путаницы — более сложная картина: KRIT1 несёт два соседних докинг‑сегмента, и оба необходимы. Когда нарушался любой из сегментов, уровни KLF4 оставались аномально высокими, как если бы KRIT1 вовсе отсутствовал. Биохимические тесты в генетически модифицированных клетках показали, что одна молекула KRIT1 может одновременно связывать две отдельные молекулы CCM2, намекая на неожиданную трёхкомпонентную сборку.
Видеть молекулярный зажим в деталях
Далее команда очистила соответствующие фрагменты CCM2 и KRIT1 и изучила, как они собираются в растворе и в кристаллах. Измерения массы комплекса показали, что две копии ключевого региона CCM2 связываются с одной полоской KRIT1, несущей пару докинг‑сайтов. Снимки структуры с высоким разрешением подтвердили соотношение 2:1: один удлинённый пептид KRIT1 проходит между двумя доменами CCM2, причём каждый докинг‑сайт располагается в похожем кармане на разной молекуле CCM2. Короткий спиралевидный сегмент между докинг‑сайтами помогает ориентировать два домена CCM2 рядом друг с другом, создавая плотную, зажимоподобную структуру. Этот тип двойного захвата — два связывающих домена, чётко фиксирующихся на последовательных сайтах одного партнёра — ранее не наблюдался для этого семейства белковых модулей.
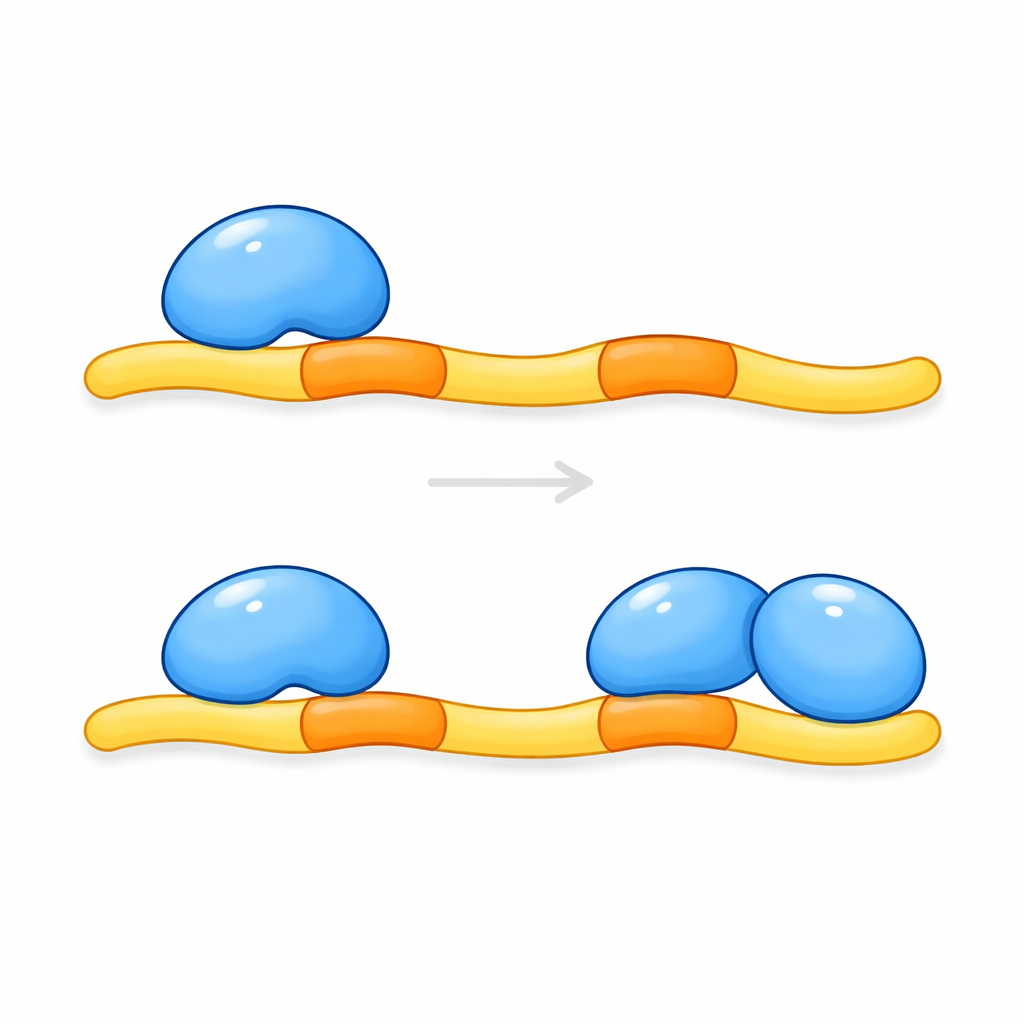
Последствия для заболеваний мозга и не только
Эти результаты показывают, что KRIT1 не просто связывает одну молекулу CCM2; он действует как каркас, привлекающий пару молекул CCM2. Только при занятии обоих докинг‑сайтов на KRIT1 комплекс способен надёжно сдерживать продукцию KLF4 и, соответственно, помогать предотвращать образование хрупких сосудов. Мутации в KRIT1, нарушающие любой из докинг‑сайтов, вследствие этого, вероятно, ослабляют этот защитный зажим и могут объяснять некоторые наследственные формы церебральных кавернозных мальформаций. Поскольку многие другие человеческие белки несут схожие двойные докинг‑мотивы, исследование также указывает на более общий принцип: двойное связывание парами родственных доменов может быть широко используемым способом тонкой настройки сигнальных сетей в клетке. Понимание этого трёхстороннего взаимодействия в конечном счёте может помочь в разработке стратегий стабилизации сосудов у людей, подверженных риску мозговых кровоизлияний.
Цитирование: Huet-Calderwood, C., Fisher, O.S., Das, S. et al. Dual recruitment of two CCM2 molecules to KRIT1 suppresses KLF4 expression. Nat Commun 17, 2719 (2026). https://doi.org/10.1038/s41467-026-69595-7
Ключевые слова: церебральные кавернозные мальформации, эндотелиальные клетки, KRIT1, CCM2, KLF4