Clear Sky Science · ru
Фосфоглицератдегидрогеназа‑опосредованная перенастройка серина усугубляет гипервоспаление макрофагов при пневмонии у мышей, вызванной Pseudomonas aeruginosa
Когда защитники организма заходят слишком далеко
Пневмония, вызванная бактерией Pseudomonas aeruginosa, известна своей трудноизлечимостью, особенно у людей с ослабленными лёгкими. Антибиотики нацелены на микроб, но эта болезнь часто оказывается смертельной не только из‑за самой бактерии, сколько из‑за того, что собственный иммунный ответ организма выходит из‑под контроля. В этом исследовании показано, как один метаболический «переключатель» внутри иммунных клеток способен перевести их из полезного состояния в вредное — и предполагается, что корректировка диеты или клеточного метаболизма могла бы смягчить угрожающее жизни воспаление лёгких.
Опасный танец между микробом и иммунной системой
Pseudomonas aeruginosa — распространённая грамотрицательная бактерия, способная проникать в нижние дыхательные пути и вызывать тяжёлую пневмонию. В норме находящиеся в лёгких иммунные клетки — макрофаги — патрулируют альвеолы, захватывают захватчиков и подают сигнал тревоги с помощью химических медиаторов. Но при высокой бактериальной нагрузке эти клетки привлекают многочисленные дополнительные макрофаги из кровотока. В результате может возникнуть лавина провоспалительных молекул, повреждающих хрупкую ткань лёгких, нарушающая процессы восстановления и в тяжёлых случаях приводящая к дыхательной недостаточности и смерти. Авторы задали вопрос, не приводит ли внутренний метаболизм этих макрофагов к такой вредной сверхреакции.
Метаболический фермент в горячем кресле
Группа сосредоточилась на ферменте фосфоглицератдегидрогеназе (PHGDH) — ключевом входном звене в путь, которым клетки синтезируют аминокислоту серин из глюкозы. В моделях пневмонии у мышей уровни и активность PHGDH резко повышались в лёгких, особенно в макрофагах. Когда мышам давали малую молекулу‑ингибитор PHGDH, или когда ген PHGDH удаляли специфически в миелоидных клетках (включая макрофаги), животные чувствовали себя лучше: они жили дольше, у них было меньше повреждений лёгких, меньшая бактериальная нагрузка и сниженное производство мощных провоспалительных цитокинов, таких как интерлейкин‑6 и интерлейкин‑1β. На клеточном уровне блокада PHGDH отодвигала макрофагов от сильно провоспалительного состояния, не усиливая при этом противоположный, способствующий заживлению фенотип.
Подпитывая пламя: серин и сверхактивная сигнальная цепь
Углубляясь в механизм, исследователи показали, что инфекция перенастраивает макрофаги так, что они направляют больше глюкозы на синтез серина, и что этот серин, в свою очередь, усиливает воспаление. Дополнительный серин заставлял макрофаги выделять больше провоспалительных цитокинов и экспрессировать больше поверхностных маркеров активации, тогда как диеты с ограничением серина защищали инфицированных мышей и снижали число бактерий. Механистически серин поступал в одноуглеродный метаболический цикл, который обеспечивает клетку метильными группами — химическими метками, используемыми в эпигенетической регуляции. Это усиливало конкретную гистоновую модификацию, H3K27 триметилирование, вблизи гена тормозящего белка DUSP4, который обычно помогает выключать сигнальный путь ERK1/2. При подавлении DUSP4 ERK1/2 оставался включённым, усиливая провоспалительные сигналы. Ингибирование PHGDH или снижение серина обращало эту цепочку, восстанавливало DUSP4 и уменьшало фосфорилирование ERK1/2.
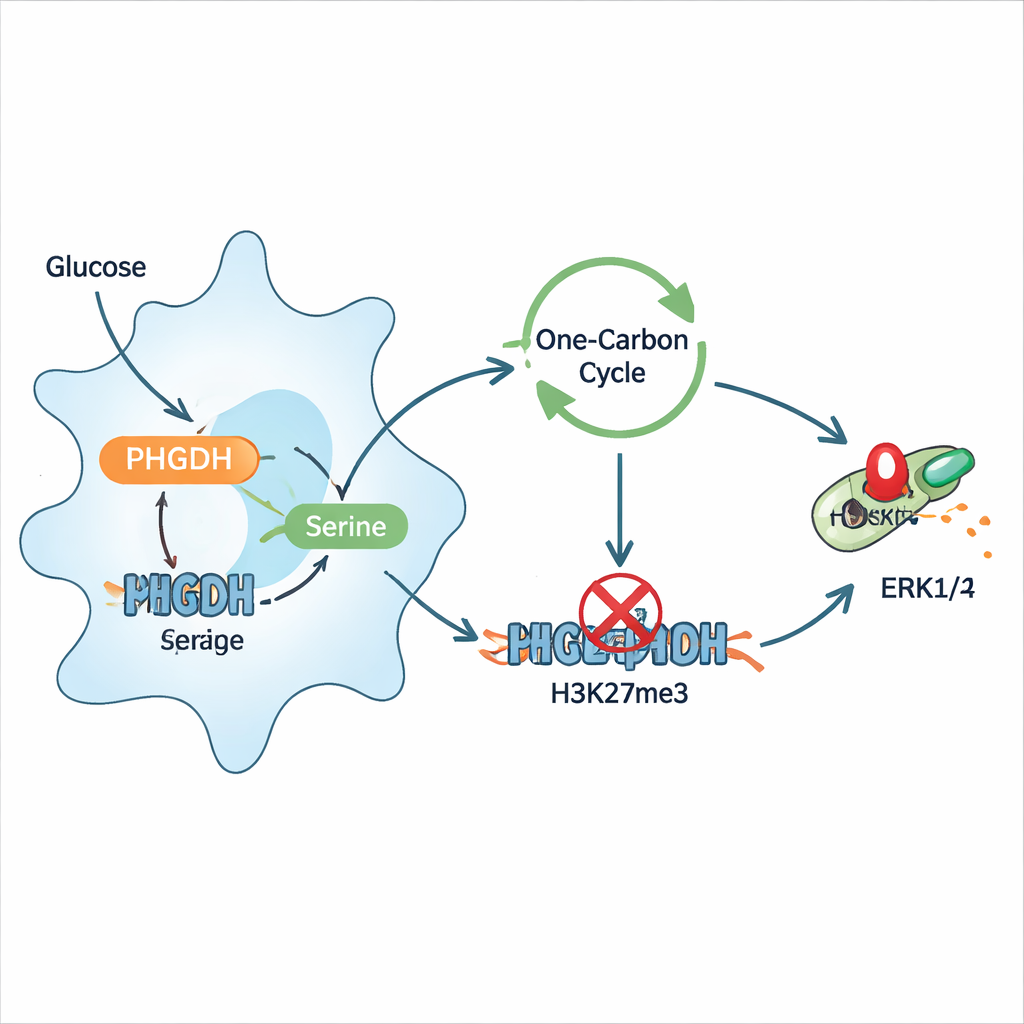
Пересбалансирование макрофагов без ослабления защиты
Важно, что снижение активности PHGDH не парализовало иммунную систему. Наоборот, макрофаги, лишённые PHGDH, лучше захватывали и убивали Pseudomonas на ранних стадиях инфекции, при этом выделяя меньше повреждающих цитокинов. Пересадка этих макрофагов с дефицитом PHGDH в нормальных мышей улучшала исход после бактериального вызова, подчёркивая, что преимущества были связаны с перенастройкой реакции хозяина, а не прямым действием на микроба. Работа также намекает, что диеты, богатые серином, могут непреднамеренно способствовать гипервоспалению при тяжёлой бактериальной пневмонии, тогда как контролируемое ограничение серина может предложить новый способ сдержать чрезмерное повреждение лёгких.
Что это значит для лечения трудноизлечимой пневмонии
Проще говоря, исследование показывает, что некоторые макрофаги при пневмонии Pseudomonas сжигают сахар так, что производят лишний серин, и что этот метаболический обход переключает их воспалительный аппарат на повышенную активность. Блокируя фермент PHGDH или ограничивая серин, исследователи смогли успокоить эту сверхреакцию, защитить ткань лёгких и при этом позволить иммунным клеткам очищать бактерии. Хотя работа проведена на мышах и далека от клинического применения, она указывает на перспективную идею: сочетание традиционных антибиотиков с препаратами или диетическими подходами, тонко корректирующими метаболизм иммунных клеток, может превратить разрушительный иммунный ураган в контролируемое, направленное на бактерии пламя.
Цитирование: Chen, R., Zeng, R., Shi, M. et al. Phosphoglycerate dehydrogenase-mediated serine reprogramming aggravates macrophage hyperinflammation in murine Pseudomonas aeruginosa pneumonia. Nat Commun 17, 1944 (2026). https://doi.org/10.1038/s41467-026-69539-1
Ключевые слова: пневмония Pseudomonas, метаболизм макрофагов, биосинтез серина, воспаление лёгких, PHGDH