Clear Sky Science · ru
FOXF2 регулирует перицит–эндотелиальную сигнализацию, необходимую для сосудистого гомеостаза после неонатального гипероксического повреждения легких
Почему новорожденным легким нужна бережная защита
Для детей, рожденных преждевременно, дыхание может быть затруднено. Многие нуждаются в дополнительном кислороде для выживания, но эта жизнеобеспечивающая терапия может повредить их хрупкие легкие и кровеносные сосуды, способствуя развитию хронического состояния — бронхолегочной дисплазии. В этом исследовании рассматривается малоизученная группа поддерживающих клеток, окружающих крошечные сосуды легкого, и выявляется ключевой генетический переключатель, который помогает этим клеткам защищать и восстанавливать новорожденное легкое после кислородного повреждения.
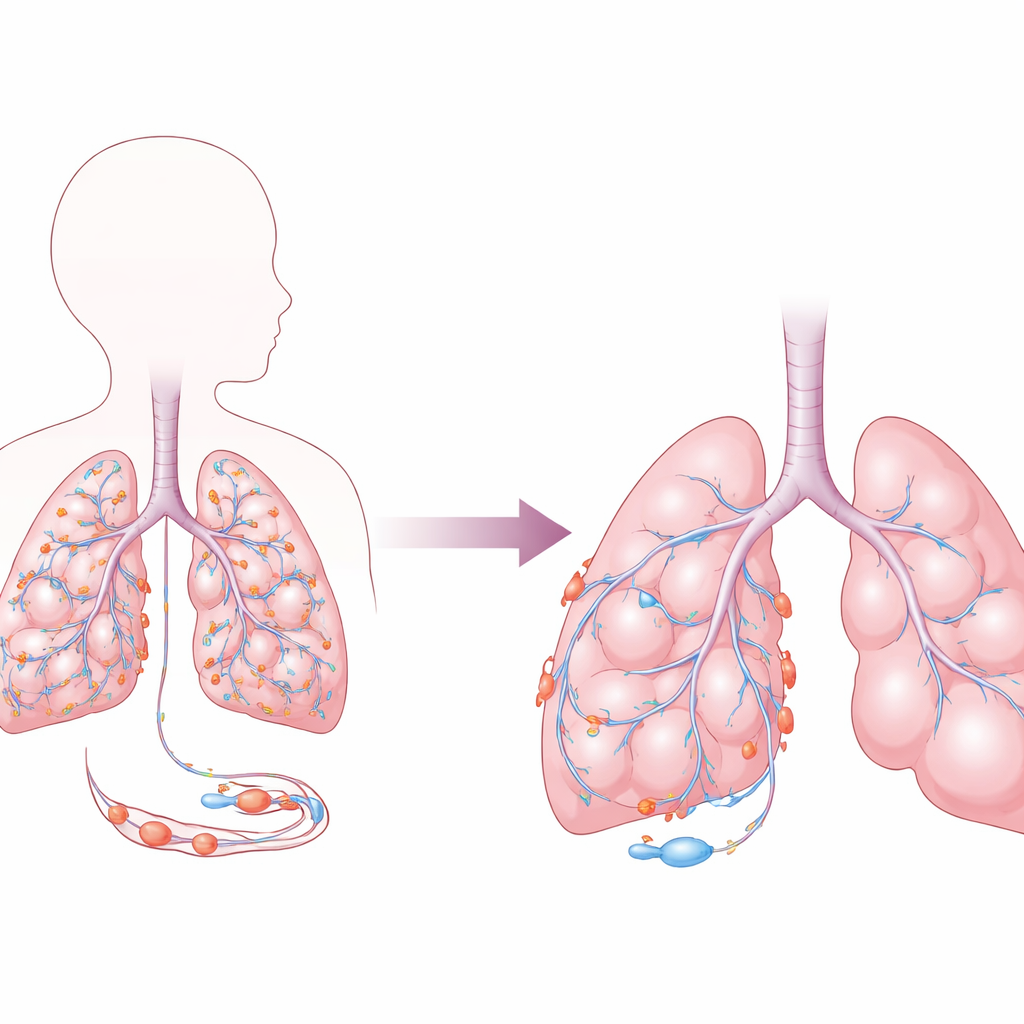
Скрытые помощники вокруг сосудов легкого
Альвеолы легкого, где кислород попадает в кровь, оплетены плотной сетью капилляров. Вокруг многих из этих капилляров располагаются перициты — поддерживающие клетки, которые помогают удерживать сосуды стабильными, направлять рост новых сосудов и поддерживать плотный барьер, чтобы жидкость не просачивалась в воздушные пространства. Авторы сосредоточили внимание на гене FOXF2, транскрипционном факторе, который контролирует, какие другие гены включаются или выключаются в перицитах. Анализируя данные одиночноклеточной РНК из развивающихся легких мышей, они обнаружили, что активность Foxf2 в перицитах растет после рождения параллельно с генами, связанными со зрелостью перицитов, развитием сосудов и клеточной миграцией. Напротив, его активность значительно ниже в других соседних типах клеток, что указывает на специализированную роль в этих сосудистых поддерживающих клетках.
Когда тормоз для перицитов снимается
Чтобы проверить, что на самом деле делает FOXF2, команда создала мышей, в которых Foxf2 можно было удалить специально в PDGFRβ-положительных перицитах сразу после рождения. При нормальных условиях кислорода общая структура легких и уровень кислорода в крови выглядели в целом нормально, но детали показали иную картину. Перициты чрезмерно размножались и плотно окружали капилляры, тогда как маркеры зрелых, хорошо функционирующих перицитов снижались. Эти перициты чаще находились в фазе синтеза ДНК клеточного цикла, а лабораторные эксперименты подтвердили, что прямое блокирование Foxf2 в культивируемых перицитах усиливало их пролиферацию и снижало миграцию. Одновременно гены, которые обычно помогают сосудам расти и оставаться стабильными, такие как Angptl4 и Angpt2, были подавлены, тогда как гены, стимулирующие деление клеток и энергетический обмен, были активнее. В совокупности это рисует картину многочисленных, но менее компетентных перицитов.
Кислородный стресс выявляет критическую уязвимость
Последствия стали намного серьезнее, когда новорожденных мышей подвергли воздействию высокого уровня кислорода — стандартной модели повреждения легких при преждевременных родах. И в легких мышей, и в образцах человеческих тканей от младенцев с бронхолегочной дисплазией уровень FOXF2 в перицитах заметно снижался после такого повреждения. Когда мыши с дефицитом Foxf2 подвергались гипероксии, их выживаемость резко падала, насыщение кислородом крови снижалось, а альвеолы становились увеличенными и упрощенными, что свидетельствует о плохом развитии воздухообменных отделов. Одновременно покрытие капилляров в альвеолах уменьшалось, эндотелиальные клетки делились реже, и больше флуоресцентного трассера просачивалось из сосудов в легочную ткань — признак нарушения сосудистого барьера. Флоуцитометрия подтвердила, что при повреждении число эндотелиальных клеток сокращалось, тогда как перициты дополнительно накапливались и оставались высоко пролиферативными, что подчеркивает разрыв в нормальном партнерстве между этими двумя типами клеток.
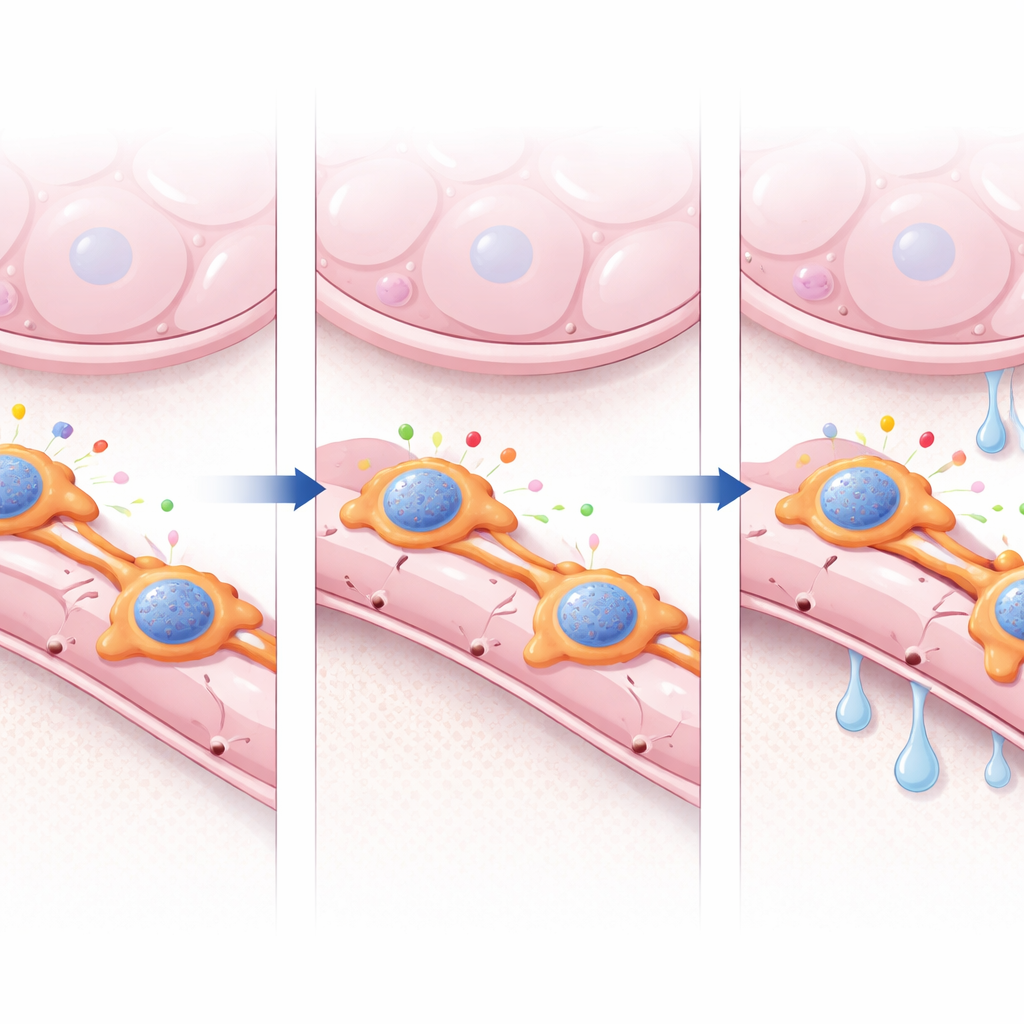
Как сигналы перицитов формируют восстановление сосудов
Углубляясь в молекулярный диалог, исследователи использовали вычислительные инструменты для отображения путей сигнализации между перицитами и эндотелиальными клетками. В здоровых легких преобладали пути, способствующие росту и стабильности сосудов, включая те, в которых участвует ANGPTL4 — секретируемый белок с проангиогенными и барьер-модулирующими свойствами. В легких с дефицитом Foxf2 эти полезные сигналы ослабли, в то время как усилились пути стресса и воспаления. Кондиционированная среда от перицитов, лишенных Foxf2, поддерживала меньшее образование трубочек у человеческих легочных эндотелиальных клеток в культуре, но добавление рекомбинантного ANGPTL4 частично восстанавливало этот дефект, указывая на ось FOXF2–ANGPTL4 как ключевой фактор восстановления. Профилирование хроматина дополнительно показало, что FOXF2 связывается рядом со многими проангиогенными генами и помогает сохранять доступность окружающих регионов ДНК. При потере FOXF2 доступность снижалась на тысячах таких участков, включая локус Angptl4, что предполагает, что FOXF2 действует как организатор хроматина, позволяющий другим факторам поддерживать здоровую программу перицитов.
Что это значит для хрупких легких новорожденных
В совокупности результаты показывают, что FOXF2 выступает в роли главного регулятора, который поддерживает неонатальные перициты легких в зрелом состоянии, сдерживает их рост и обеспечивает способность посылать правильные сигналы соседним эндотелиальным клеткам. Когда уровни FOXF2 падают после кислородного повреждения, перициты становятся чрезмерно многочисленными, но дисфункциональными: они посылают меньше питающих сигналов, таких как ANGPTL4, капилляры не могут правильно восстановиться, стенки сосудов становятся проницаемыми, и архитектура альвеол ухудшается. Для семей и клиницистов, ухаживающих за преждевременно рожденными детьми, эта работа выделяет перициты — и управляемые FOXF2 генетические сети в них — как перспективные мишени для будущих терапий, направленных на сохранение мелких сосудов, улучшение газообмена и снижение долгосрочного повреждения легких после воздействия кислорода в ранней жизни.
Цитирование: Sun, F., Zhao, Y., Do, J. et al. FOXF2 regulates pericyte–endothelial signaling required for vascular homeostasis after neonatal hyperoxic lung injury. Nat Commun 17, 2691 (2026). https://doi.org/10.1038/s41467-026-69525-7
Ключевые слова: бронхолегочная дисплазия, развитие легких, перициты, ангиогенез, неонатальная гипероксия