Clear Sky Science · ru
Чрезмерная активация сигнала FGFR3 при ахондроплазии нарушает обновление хондроцитов покоящейся зоны через сигнальный путь CREB
Почему это исследование роста костей важно
Ахондроплазия — наиболее частая причина наследственного карликовости с укороченными конечностями. Она влияет не только на рост, но и на здоровье позвоночника, подвижность и качество жизни. Существующие методы лечения помогают, но не восстанавливают рост костей полностью. В этом исследовании использована сложная модель мыши, которая выявила ранее незамеченную проблемную зону в растущих костях и указала на новый сигнальный переключатель — CREB — как перспективную мишень для будущих терапий.
Как здоровые кости увеличиваются в длину
Длинные кости, такие как бедренная кость, удлиняются за счет зон роста, расположенных у их концов. Эти зоны организованы в три основных слоя хондроцитов. Вверху находится покоящаяся зона, где клетки ведут себя как пул стволовых клеток: делятся редко и направляют дочерние клетки вниз. Ниже расположена пролиферативная зона с быстро делящимися клетками, уложенными в упорядоченные колонны, которые обеспечивают удлинение. В конце лежит гипертрофическая зона, содержащая увеличенные зрелые клетки, которые помогают формировать новую кость. Баланс между этими зонами поддерживает правильную скорость и форму роста кости.
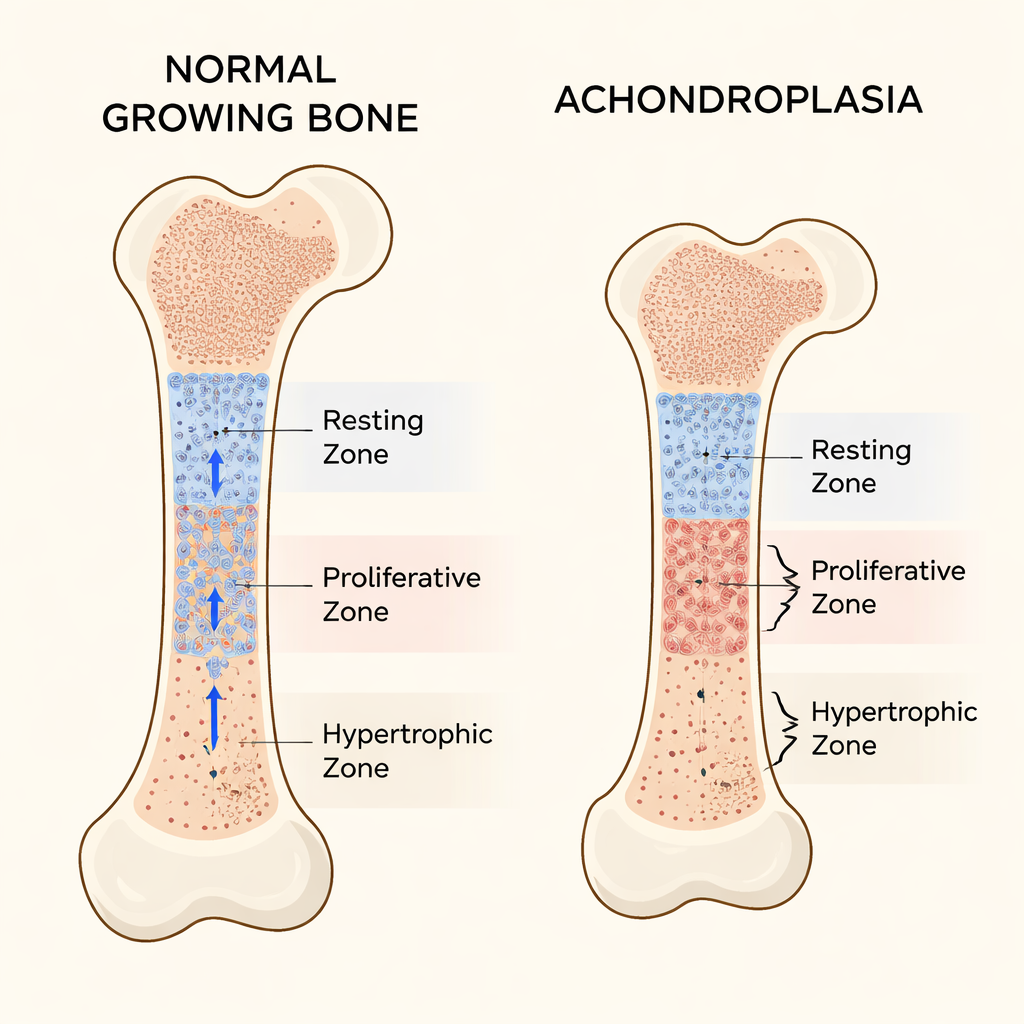
Что идет не так при ахондроплазии
У большинства людей с ахондроплазией одна мутация в гене FGFR3 делает его рецептор сверхактивным, что тормозит рост кости. Ранее показали, что этот сигнал замедляет деление клеток в пролиферативной зоне и блокирует окончательное увеличение клеток в гипертрофической зоне. Используя мышей, несущих человеческую мутацию ахондроплазии, авторы подтвердили выраженное укорочение конечностей и уменьшение зон роста. Но тщательные измерения выявили то, что во многом оставалось незамеченным: сама покоящаяся зона стала необычно утолщенной. Вместо того чтобы быть устойчивым резервом стволовых клеток, эта область расширялась и содержала клетки с дефицитом нормального хрящевого матрикса.
Клетки покоящейся зоны теряют «стволовую» поведенческую программу
Чтобы понять причину расширения, команда отслеживала деление и перемещение клеток зоны роста во времени. У нормальных мышей клетки покоящейся зоны делились редко, а их потомки мигрировали вниз по прямым колоннам, пополняя пролиферативную зону. У мутантных мышей намного больше клеток покоящейся зоны делились редко и оставались на месте, накапливаясь в плотный слой, который плохо снабжал нижние зоны. Трассировка происхождения с помощью многоцветных генетических маркеров показала, что клональные колонны были короткими и дезорганизованными: дочерние клетки блуждали в случайных направлениях, вместо того чтобы образовывать аккуратные ряды. Маркеры «стволоподобной» идентичности, такие как белок CD73, исчезли в расширенной покоящейся зоне, что говорит о том, что сверхактивный FGFR3 нарушил нормальную нишу стволовых клеток.
Новый виновник сигнальной передачи: CREB
Затем исследователи применили одиночноклеточный РНК-секвенсинг, чтобы профильтровать тысячи отдельных клеток зоны роста. Они выделили отдельный кластер, соответствующий расширенной покоящейся зоне, богатый геном Spon1 и другими. Анализ путей подчеркнул активацию CREB — белка, который включает гены в фосфорилированной форме. Микроскопия показала, что клетки покоящейся зоны у мутантных мышей сильно экспрессировали активированный CREB и его коактиватор CBP, вместе с высоким уровнем FGFR3 и сигнальными молекулами вниз по каскаду, такими как STAT5. В культурализованных клетках стимуляция пути FGFR3 усиливала активность CREB и увеличивала уровень SPONDIN1 (белок SPON1), тогда как блокада FGFR3 или CREB снижала эти сигналы. Это поместило CREB в роль ключевого реле между сверхактивным рецептором на поверхности клетки и нарушенным поведением клеток покоящейся зоны.
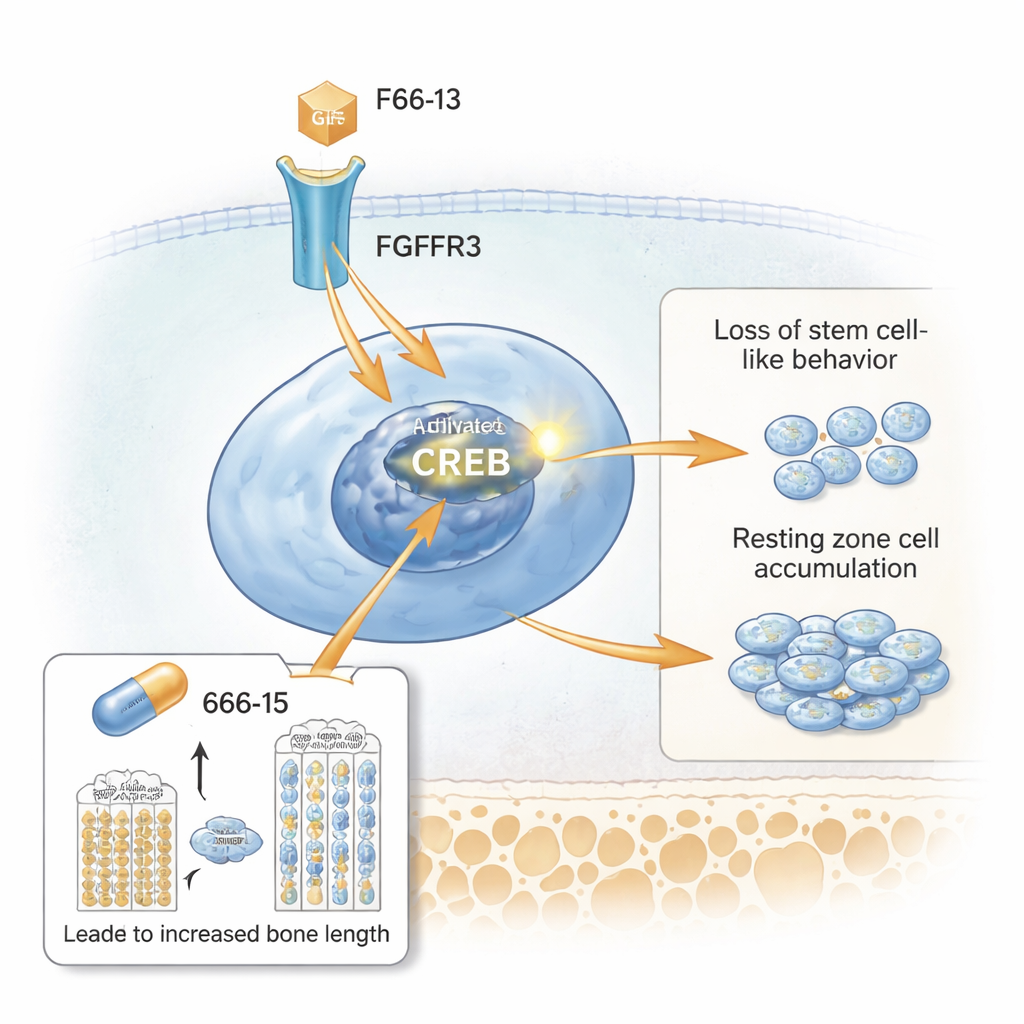
Тестирование препарата, подавляющего CREB
Наконец команда выяснила, может ли ослабление CREB улучшить проблемы роста. Они лечили модельные мыши с ахондроплазией малой молекулой-ингибитором CREB, называемой 666-15, в период быстрого посленатального роста. По сравнению с нелечеными мутантными мышами у животных, получавших 666-15, была большая масса тела и более длинные бедренные кости. Их зоны роста выглядели более нормально: покоящаяся зона истончилась, пролиферативная и гипертрофическая зоны восстановили высоту, и вновь появилось матричное белковое наполнение хряща. Маркеры избыточной активности CREB, включая фосфо-CREB, SPONDIN1 и STAT5, уменьшились в покоящейся зоне, тогда как маркер «стволовости» CD73 вернулся. Важно, что тот же препарат при исследуемой дозе мало влиял на здоровых контрольных мышей, что указывает на его преимущественное действие при патологически высоком уровне CREB.
Что это означает для будущих лечения
Исследование показывает, что при ахондроплазии сверхактивный FGFR3 делает больше, чем просто замедляет деление и рост клеток; он также нарушает тихую, стволоподобную покоящуюся зону, включая CREB. Это нарушение лишает нижележащие слои зоны роста притока новых клеток и способствует укорочению костей. Существующие препараты, такие как восоритид (vosoritide), в основном нацелены на другие пути в пролиферативной и гипертрофической зонах и лишь частично восстанавливают длину кости. Включение CREB в список мишеней — особенно в покоящейся зоне — может позволить комбинированным стратегиям в будущем более полно нормализовать рост у детей с ахондроплазией.
Цитирование: Horike, N., Oura, S., Koyamatsu, S. et al. Excess FGFR3 signaling in achondroplasia disrupts turnover of resting zone chondrocytes via CREB signaling. Nat Commun 17, 1856 (2026). https://doi.org/10.1038/s41467-026-69507-9
Ключевые слова: ахондроплазия, FGFR3, зона роста кости, стволовые клетки хряща, сигнализация CREB