Clear Sky Science · ru
Плотность заряда гидратированного металлического центра как универсальный дескриптор, объясняющий механистические различия активации периодата при деградации загрязнителей
Очистка воды при помощи продуманной химии
Многие лекарства и промышленные химикаты проходят через обычные очистные сооружения и попадают в реки и питьевую воду. В этом исследовании рассматривается перспективный способ разложения таких стойких загрязнителей с использованием распространённого окислителя — периодата — и показано, что простое свойство ионов металлов в воде позволяет предсказать, насколько эффективно и безопасно будет работать эта химия. Понимание этого правила может помочь инженерам проектировать более чистые и эффективные системы очистки для разнообразных реальных вод.
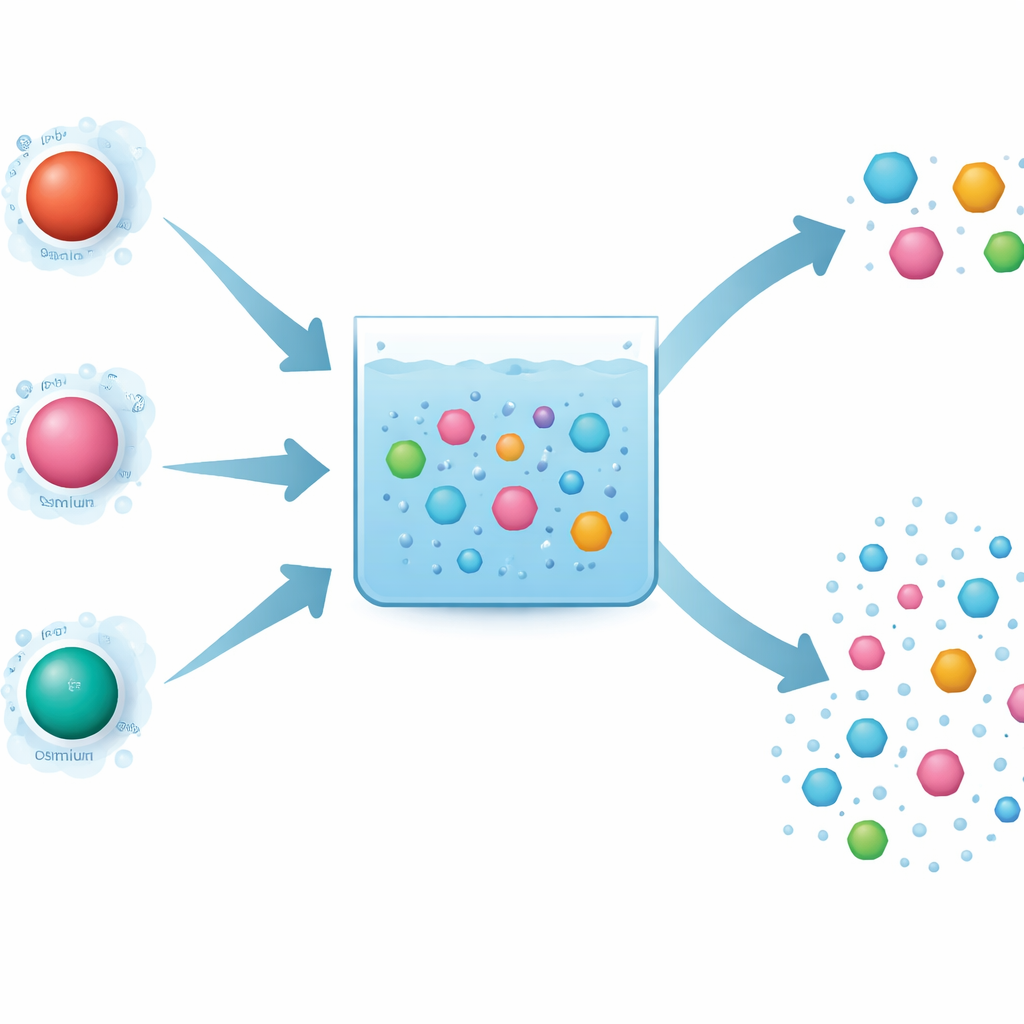
Почему выбор металла важен для разложения загрязнителей
Процессы продвинутого окисления используют мощные реактивные виды для разрыва органических молекул. Периодат — один из таких окислителей, и его можно «включить» растворёнными ионами металлов. Авторы сравнили три близких по свойствам металла — железо, рутений и осмий — которые принадлежат к одному столбцу периодической таблицы и теоретически могли бы вести себя похоже. Все три способны активировать периодат и помогать разлагать тестовый лекарственный загрязнитель карбамазепин. Тем не менее эксперименты выявили поразительные различия: рутений действовал очень быстро, железо было медленнее, а осмий — посередине. Ещё более странно, осмий удалял широкий спектр загрязнителей без явных предпочтений, тогда как железо и рутений были разборчивы, гораздо легче реагируя с одними соединениями, чем с другими.
Два совершенно разных химических пути
Чтобы понять причины этих различий, команда отслеживала, какие короткоживущие окисляющие виды появлялись в каждой системе металл–периодат. В системах с железом и рутением доминировали «металло‑кислородные» фрагменты, действующие как точные инструменты, которые напрямую передают атом кислорода на определённые участки загрязнителя. Эти пути обычно давали эпоксидные продукты — кольцевые структуры с добавленным одним атомом кислорода — что указывает на высокую селективность реакции. В системе с осмием основными действующими лицами были гидроксильные радикалы — чрезвычайно реакционноспособные фрагменты, атакующие почти любую близлежащую органику и дающие гидроксилированные продукты и мелкие кольцо‑раскрытые фрагменты. Тесты с химическими пробами и спектроскопией со спин‑ловушками подтвердили, что гидроксильные радикалы и родственные реактивные формы кислорода, а не высоковалентные осмий‑кислородные единицы, определяют большую часть разрушения загрязнителей в присутствии осмия.
Как условия воды формируют реакции
Команда также изучила, как рН и природные компоненты воды влияют на эти процессы. Для осмия удаление загрязнителей усиливалось по мере сдвига воды в щелочную сторону, где координация дополнительных гидроксид‑ионов вокруг металла облегчает перенос электронов и формирование радикалов. Однако при высоких дозах металла или окислителя система с осмием «самоподавлялась», поскольку вновь образованные радикалы поглощались избыточными химикатами, а не загрязнителями. Природное органическое вещество, которое часто мешает окислительным реакциям, оказывало на удивление небольшое влияние на деградацию, управляемую осмием, что говорит о стабильности радикального пути в реалистичных водах. В отличие от этого, железо и рутений работали лучше в кислых условиях, и природное органическое вещество сильно подавляло их активность, «высасывая» ключевые металло‑кислородные окислители.
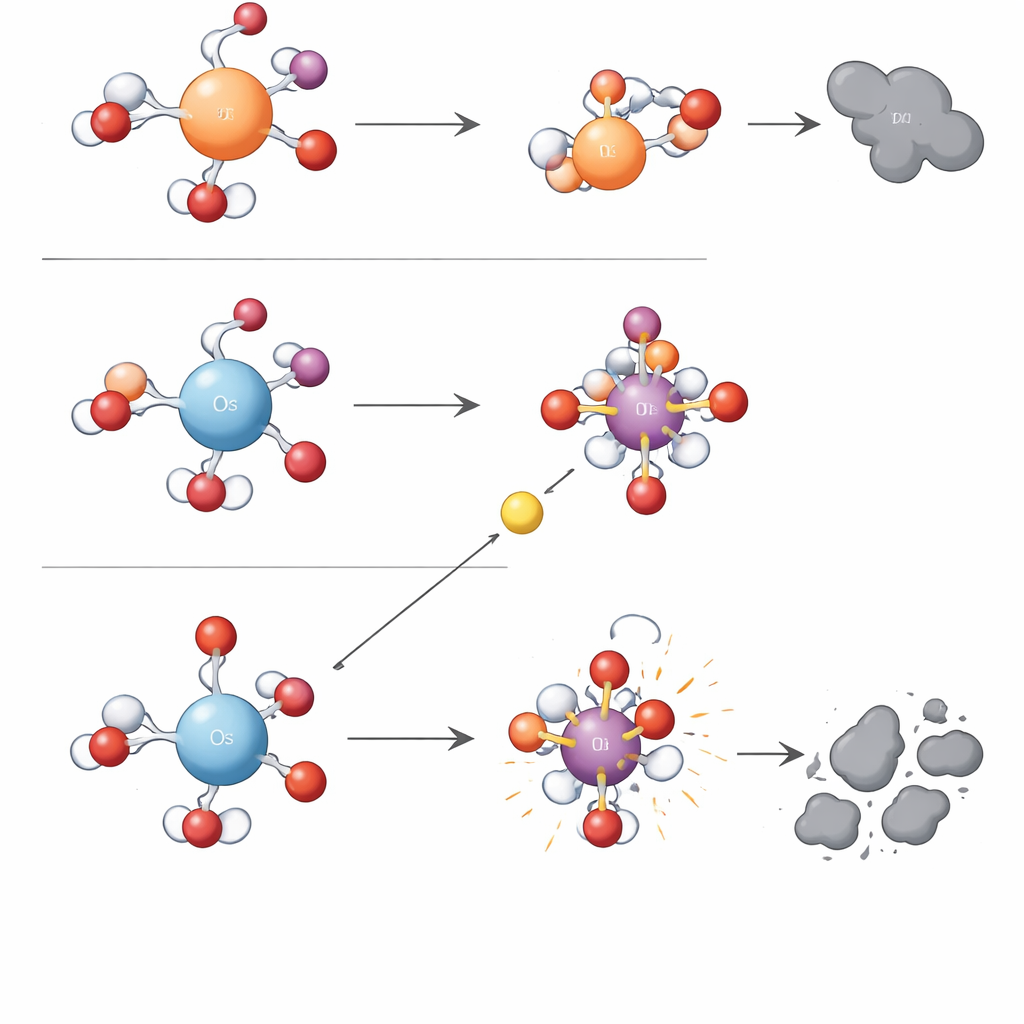
Простое правило заряда в основе сложной химии
Чтобы уйти от подбора методом проб и ошибок, исследователи обратились к квантово‑химическим расчётам. Они обнаружили, что одна электронная характеристика — плотность положительного заряда в гидратированном металлическом центре — может объяснить разделение на два типа реакций. Осмий в воде несёт более высокую сосредоточенную положительную зарядовую плотность, чем железо или рутений. Этот сильный положительный центр крепко удерживает связанный с ним атом кислорода, делая металло‑кислородную единицу стабильной, но вялой по отношению к прямой передаче кислорода. Одновременно сильное притяжение к ближайшей воде и ионам снижает энергетический барьер для одноволновых электронных шагов, которые в конечном счёте разрывают связь кислорода в периодате и высвобождают гидроксильные радикалы. Металлы с меньшей плотностью заряда, такие как железо и рутений, крепче удерживают электроны, что способствует формированию и использованию селективных металло‑кислородных окислителей вместо свободных радикалов. Авторы называют эту организующую идею «механизмом контроля плотности заряда» и показывают, что она также рационализирует тенденции, отмеченные для других металлов, например марганца.
Проектирование лучших систем очистки воды при помощи одного параметра
Связав сложный набор наблюдений с одним простым дескриптором — плотностью заряда металла в водной оболочке — эта работа предлагает дорожную карту для настройки процессов продвинутого окисления. Металлы с высокой плотностью заряда будут способствовать широкому радикальному разложению сложных смесей загрязнителей, особенно в щелочных или органически насыщенных водах. Металлы с низкой плотностью заряда более подходят, когда желательна селективная, более мягкая окислительная трансформация конкретных загрязнителей без чрезмерного реагирования со всем остальным. В практическом плане это означает, что химики и инженеры могут отбирать или проектировать катализаторы для очистки воды, регулируя, насколько плотно металлические центры удерживают заряд в своей водной среде, вместо того чтобы оптимизировать каждую систему методом проб и ошибок.
Цитирование: Qian, Y., Sun, Y., Xu, J. et al. Hydrated metal charge density as a universal descriptor explaining mechanistic variations in periodate activation toward pollutant degradation. Nat Commun 17, 2683 (2026). https://doi.org/10.1038/s41467-026-69496-9
Ключевые слова: процессы продвинутого окисления, активация периодата, очистка воды, катализ переходных металлов, гидроксильные радикалы