Clear Sky Science · ru
Высокопроизводительный химический протеомный рабочий процесс для профилирования динамики цитруллинирования белков
Почему изменение строительных блоков белков важно
Наши клетки постоянно тонко настраивают поведение белков, добавляя к ним небольшие химические правки после синтеза. Одна из таких правок — цитруллинирование — тонко меняет заряд распространённой аминокислоты и может перестроить то, как белки сворачиваются, связываются с ДНК или взаимодействуют с другими молекулами. Эти крошечные правки всё чаще связывают с аутоиммунными заболеваниями, инфекциями, раком и функцией мозга — но увидеть их очень сложно. В данном исследовании представлен высокопроизводительный лабораторный рабочий процесс, который наконец позволяет картировать цитруллинирование на тысячах белков, показывая, когда и где оно появляется в тканях и иммунных клетках.
Скрытый переключатель на белках
Цитруллинирование происходит, когда ферменты, называемые PAD, химически модифицируют аминокислоту аргинин, удаляя её положительный заряд. Это, казалось бы, небольшое изменение может ослабить упаковку ДНК, изменить жёсткость структурных белков или повлиять на то, как иммунная система распознаёт собственные ткани. Аномальное цитруллинирование связывают с ревматоидным артритом, нейродегенеративными расстройствами, вирусными инфекциями и раком. Однако цитруллинированные белки редки и легко путаются с другими, более распространёнными модификациями, поэтому стандартные методы масс‑спектрометрии часто их пропускают. В результате у исследователей была лишь фрагментированная картина «цитруллинома» — полного набора цитруллинированных белков в организме.
Двухэтапная стратегия «пометить и поймать»
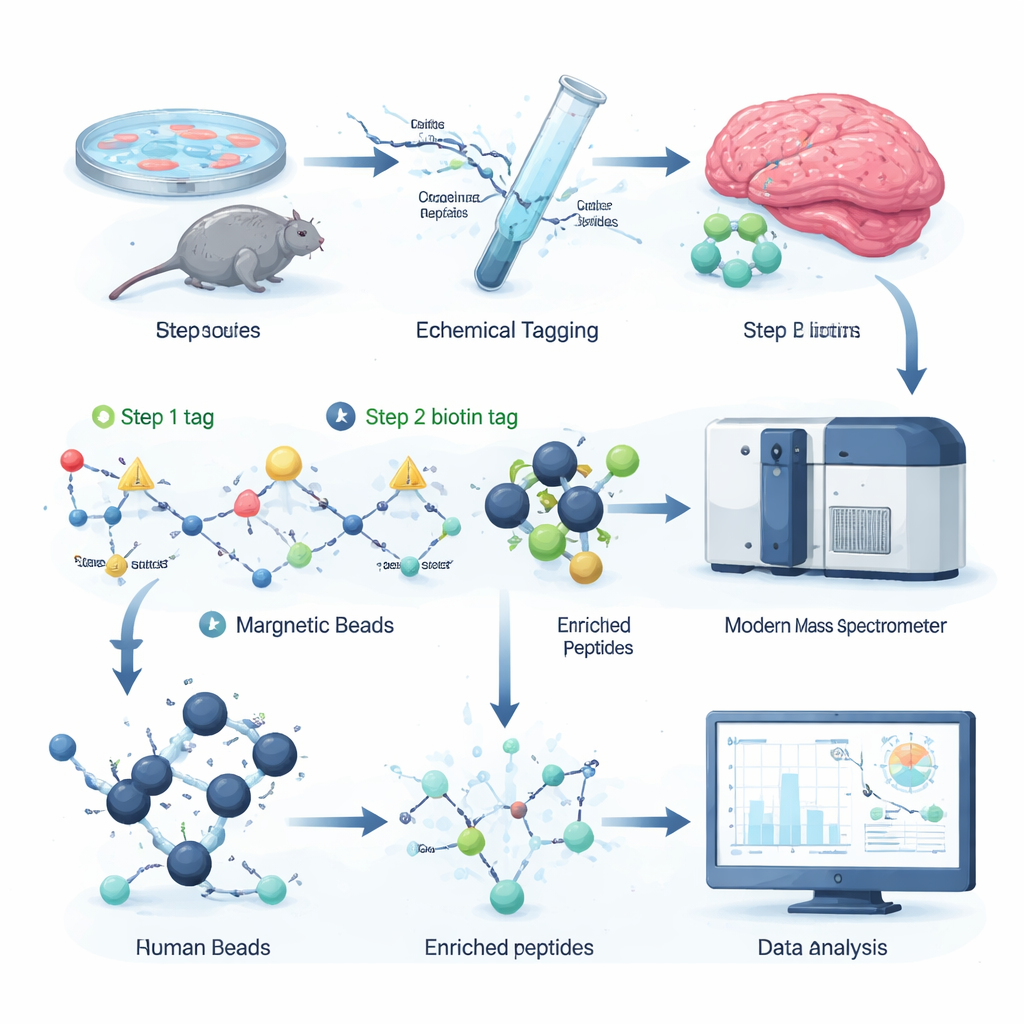
Авторы разработали химическую стратегию мечения, которая селективно присоединяет съёмную «ручку» к сайтам цитруллинирования на пептидах — фрагментах белков, анализируемых масс‑спектрометрией. На первом шаге небольшая реактивная молекула распознаёт цитрулиновую остаток и устанавливает крошечный тег. На втором шаге к нему «подключают» больший биотиновый тег с помощью click‑реакции, что позволяет извлечь меченые пептиды из сложной смеси с помощью стрептавидиновых шариков, обычного биохимического инструмента. Щадящая химическая обработка затем удаляет громоздкую часть тега, оставляя небольшой, чётко определённый сдвиг массы, который масс‑спектрометр легко обнаруживает. Поскольку все реактивы доступны коммерчески, а весь протокол помещается в 96‑луночные планшеты, рабочий процесс быстр, масштабируем и совместим с существующими протеомными установками.
Видеть больше цитруллинома
Добавляя в клеточные экстракты известные цитруллинированные пептиды и систематически их разводя, команда показала, что их стратегия обогащения повышает сигнал цитруллинированных пептидов более чем в десять раз, даже когда они составляют менее одной молекулы из тысячи. В сложных образцах число обнаруженных сайтов цитруллинирования и их измеренные интенсивности резко возросли после обогащения. Применение метода к ткани мозга мыши выявило в два–три раза больше уникальных сайтов цитруллинирования по сравнению с предыдущим передовым подходом, включая многие на основном белке миелина, изолирующем нервные волокна, и на белках, участвующих в синаптической коммуникации. Это указывает на то, что цитруллинирование может влиять как на передачу сигналов нервными клетками, так и на поддержание мозговой проводимости.
Иммунные клетки, плетущие липкие белковые сети
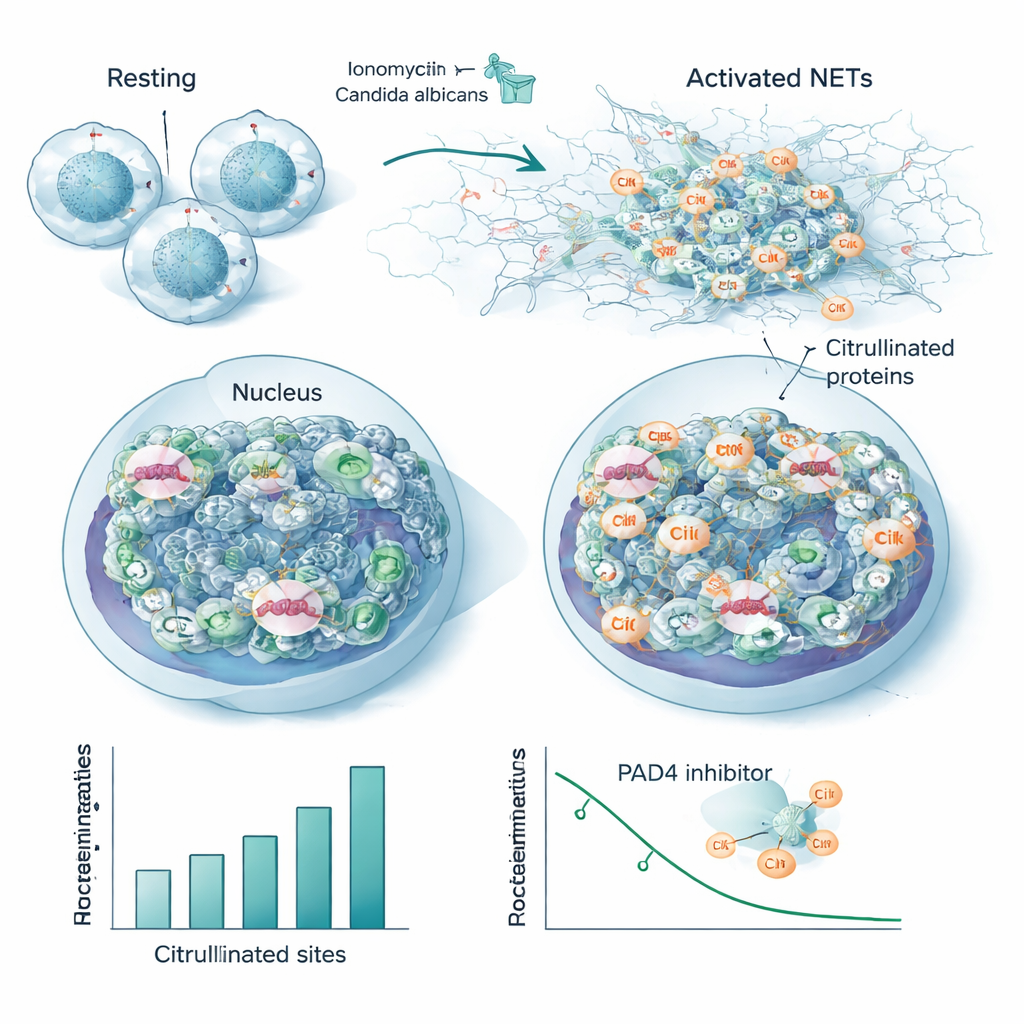
Нейтрофилы, клетки первой линии защиты из числа лейкоцитов, могут бороться с захватчиками, выпуская липкие сети из ДНК и белков, называемые внеклеточными ловушками нейтрофилов (NET). Формирование NET зависит от PAD4 — фермента, цитруллинирующего белки, который ослабляет хроматин, позволяя ДНК выходить наружу. С помощью нового рабочего процесса исследователи проследили, как меняется цитруллинирование в человеческих нейтрофилах, обработанных возрастающими дозами химического активатора. Они обнаружили до 1700 цитруллинированных пептидных фрагментов в 580 белках, причём сотни сайтов изменяли уровень в дозозависимом порядке при сохранении общей концентрации белков. Гистоны — белки, упаковывающие ДНК — проявили широкое цитруллинирование, а не только на нескольких классических сайтах, причём варианты связывающего гистона H1 особенно модифицировались. Структурные белки, такие как регуляторы актинового цитоскелета и ламин B, формирующий ядерную оболочку, также сильно цитруллинировались, что указывает на скоординированное «умягчение» как хроматина, так и клеточного каркаса во время высвобождения NET.
Ядро цитруллинирования при инфекции
Чтобы имитировать реальную инфекцию, команда стимулировала нейтрофилы термально убитой Candida albicans, распространённым грибковым патогеном. Хотя это вызвало в целом меньше модифицированных сайтов, чем сильный химический активатор, подавляющее большинство цитруллинированных белков и позиций перекрывалось между двумя триггерами. Это перекрытие определяет консервативный «ядро цитруллинома», связанное с формированием NET, включающее многие ядерные и цитоскелетные белки и несколько известных аутоантигенов — тех самых мишеней антител при аутоиммунных заболеваниях. При добавлении ингибитора PAD4 многие из этих сайтов теряли цитруллинирование в дозозависимом режиме, что напрямую связывает их с активностью фермента и указывает на то, что они могут служить чувствительными маркерами ингибирования PAD4.
Что это значит для здоровья и болезней
Преобразовав трудноуловимую модификацию в измеримый сигнал, этот рабочий процесс позволяет картировать, где и когда цитруллинирование происходит в тканях, иммунных ответах и моделях заболеваний. Для неспециалистов ключевая мысль такова: цитруллинирование действует как тонкий молекулярный диммер на белках, и возможность видеть его закономерности с высоким разрешением может помочь объяснить, как начинаются аутоиммунные болезни, как инфекции перестраивают иммунные клетки и как со временем меняются белки мозга. Масштабируемость метода и опора на стандартное лабораторное оборудование означают, что он может быть широко принят, открывая путь к обнаружению новых лекарственных мишеней, точной диагностике и более глубокому пониманию того, как малые химические правки могут иметь большие биологические последствия.
Цитирование: Meelker González, R., Laposchan, S., Riedel, E. et al. High-throughput chemical proteomics workflow for profiling protein citrullination dynamics. Nat Commun 17, 1982 (2026). https://doi.org/10.1038/s41467-026-69490-1
Ключевые слова: цитруллинирование, аутоиммунное заболевание, внеклеточные ловушки нейтрофилов, масс-спектрометрия, посттрансляционная модификация