Clear Sky Science · ru
Патофизиологическое значение нарушения KAT7‑зависимой ацетиляции гистона H3K14 при дефиците цинка
Почему крошечные нутриенты важны для нашего здоровья
Цинк — это микроэлемент, который организму нужен в очень малых количествах, но он тихо поддерживает работу сотен белков, обеспечивающих жизнедеятельность клеток. При недостатке цинка — из‑за питания, болезни или старения — это связывают с разными проблемами: от замедленного роста до ослабленного иммунитета и жировой болезни печени. В этом исследовании задан более глубокий вопрос: как именно клетки ощущают падение запасов цинка и каким образом этот дефицит превращается в долговременные изменения активности генов и состояния органов?
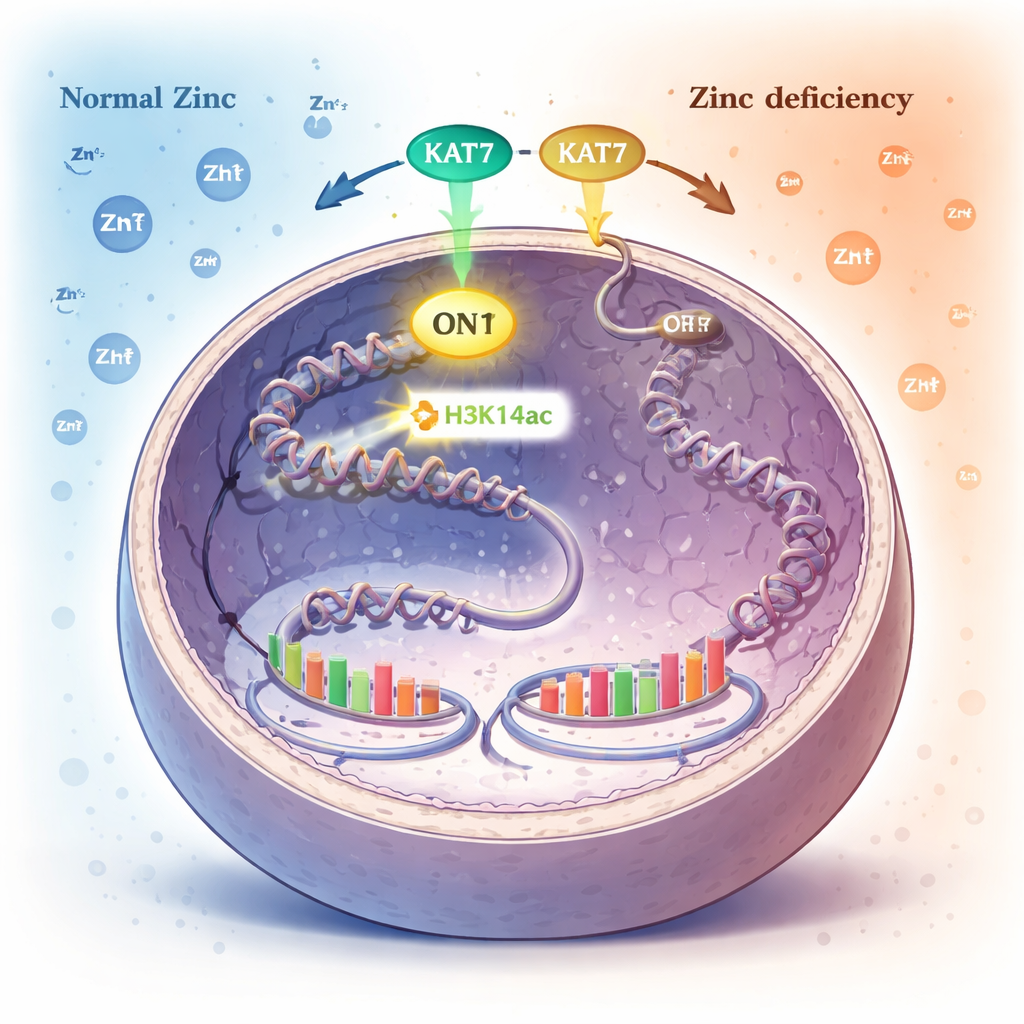
Химическая метка на упаковке ДНК как внутренняя «сигнализация» о цинке
В ядре ДНК намотана на белковые «катушки» — гистоны. Клетки регулируют, какие гены активны, добавляя или удаляя мелкие химические метки на этих гистонах. Одна из таких меток — ацетилирование в определённой позиции гистона H3 (H3K14ac) — вводится ферментом KAT7. Авторы обнаружили, что при нехватке цинка уровни этой метки H3K14ac резко падают, тогда как многие другие обычные гистонные метки остаются без изменений. Это указало на H3K14ac и фермент KAT7, создающий её, как на ключевой сенсор статуса цинка.
Как цинк поддерживает работу ключевого фермента
Путём систематического отключения различных ферментов исследователи показали, что KAT7 — основной источник H3K14ac в человеческих клетках. В активном центре KAT7 есть небольшая структура, связывающая цинк. Когда клетки испытывали дефицит цинка, способность KAT7 наносить метку H3K14ac снижалась, хотя сам белок оставался в ядре и оставался в комплексе с его партнёрами. Детальные тесты с очищенными фрагментами KAT7 показали, что правильно связанный цинк в этой области необходим для активности: нарушение связывания цинка «включало» фермент, а аккуратное добавление цинка восстанавливало его функцию. По сути, KAT7 ведёт себя как цинк‑зависимый переключатель, контролирующий специфическую гистонную метку.
Как потеря цинка превращается в изменения генов, восстанавливающие запасы цинка
Что на самом деле делает потеря этой гистонной метки? С помощью геномного картирования команда показала, что H3K14ac особенно обогащён в энхансерах — регуляторных участках ДНК, точно настраивающих соседние гены. При дефиците цинка H3K14ac исчезал с многих энхансеров, и чем сильнее была потеря, тем сильнее изменялась активность соседних генов. Одним из заметных генов оказался ZIP10, кодирующий белок на поверхности клетки, импортирующий цинк. Когда H3K14ac снижался на энхансере ZIP10, уровень ZIP10 в мембране возрастал, что позволяло клетке втягивать больше цинка. Блокирование KAT7 или предотвращение потери H3K14ac нарушало эту реакцию и снижало поглощение цинка, даже после добавления цинка. Это демонстрирует, что клетки преобразуют дефицит цинка в эпигенетический сигнал, который усиливает механизмы импорта цинка для восстановления баланса.
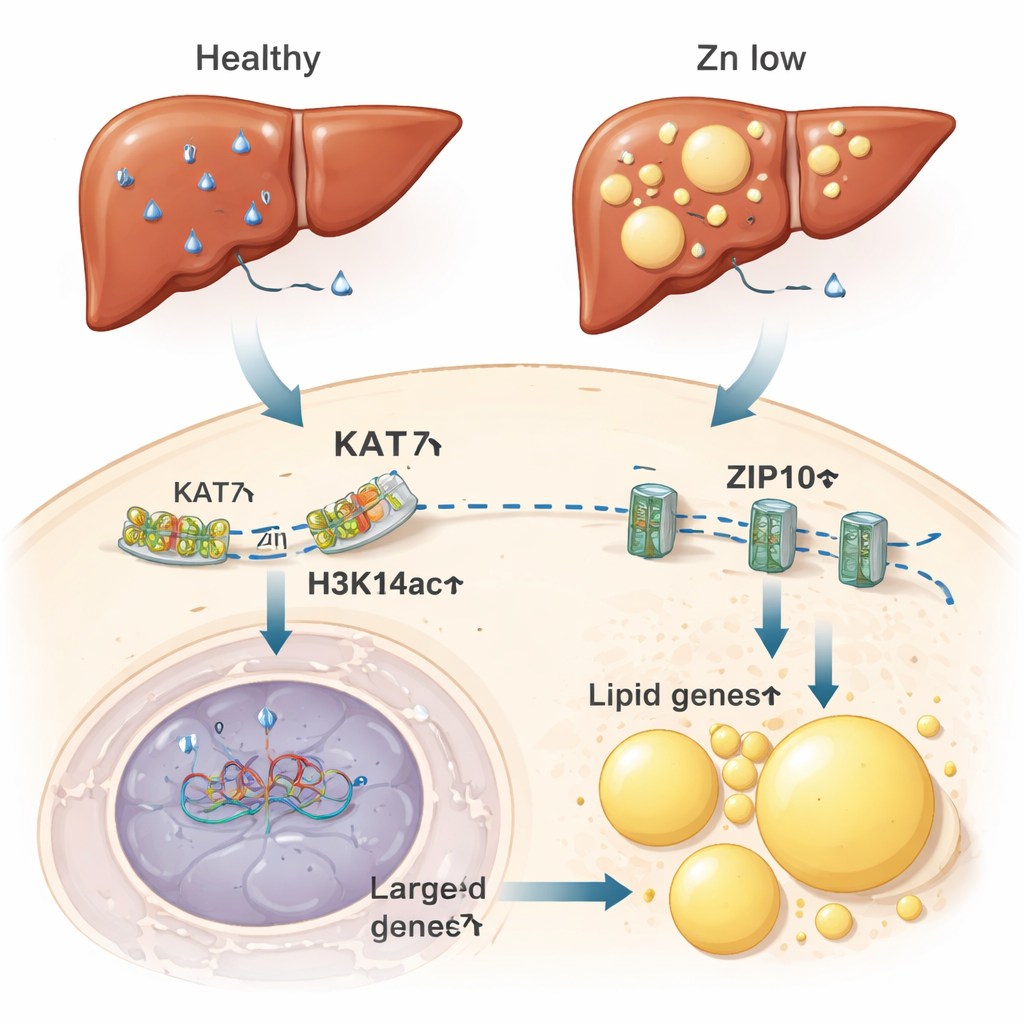
От истощённых цинком клеток до жировой печени
Авторы далее изучили, имеет ли этот цинк‑чувствительный переключатель последствия в целом организме. У мышей на диете с дефицитом цинка печень — центральный узел обмена цинка и липидов — показывала пониженные уровни цинка, снижение H3K14ac и ослабление активности KAT7. Эти изменения совпадали с повышенной экспрессией генов, стимулирующих накопление жира и образование липидных капель — микроскопических жировых пакетов в клетках. Печень мышей с дефицитом цинка накапливала жир в степени, сопоставимой с таковой при высокожировой диете. Поразительно, простое снижение активности KAT7 с помощью препарата, без изменения диеты по цинку, было достаточным, чтобы способствовать накоплению жира в клетках печени. И наоборот, дополнительная подача цинка ослабляла накопление жира, вызванное высокожировой диетой.
Что это значит для риска заболеваний у людей
Помещая свои результаты в клинический контекст, исследователи проанализировали работы, измерявшие уровни цинка в тканях печени у людей. Во множестве отчётов у людей с жировой болезнью печени и родственными расстройствами в печени было значительно меньше цинка, чем у здоровых контрольных групп. В сочетании с экспериментами на мышах это указывает на то, что хронический дефицит цинка может способствовать развитию жировой болезни печени, подавляя KAT7, стирая метку H3K14ac и долговременно повышая экспрессию генов, склоняющих к накоплению жира. Проще говоря, работа выявляет внутреннюю «схему от цинка к эпигенетике»: при падении цинка цинк‑зависимый фермент теряет силу, упаковка ДНК меняется таким образом, что сначала помогает клеткам втягивать больше цинка, но со временем может и подталкивать печень к нездоровому накоплению жира.
Цитирование: Fujisawa, T., Takenaka, S., Maekawa, L. et al. Pathophysiological significance of impaired KAT7-dependent histone H3K14 acetylation during zinc deficiency. Nat Commun 17, 1710 (2026). https://doi.org/10.1038/s41467-026-69476-z
Ключевые слова: дефицит цинка, эпигенетика, жир в печени, ацетилирование гистонов, транспортеры цинка