Clear Sky Science · ru
Общий справочник, определённый консенсусными пиками, для анализа данных single-cell ATAC-seq
Почему важно картографировать «открытые двери» нашей ДНК
Каждая клетка вашего тела по сути содержит одну и ту же ДНК, но клетки мозга, клетки крови и опухолевые клетки ведут себя совсем по-разному. Одной из ключевых причин является то, что в любой момент открыты и доступны для работы лишь определённые участки ДНК. Новые одноклеточные технологии теперь позволяют измерять эту доступность по всему геному, но до сих пор им не хватало общего эталонного набора — некоего стандартного атласа — чтобы сравнивать результаты между экспериментами и лабораториями. В этом исследовании создана такая карта, названная cPeaks, и показано, как она позволяет более чётко различать типы клеток, этапы развития и особенности рака.
Объединение множества экспериментов в одну общую карту
Авторы начали с того, что собрали 624 высококачественных эксперимента, измерявших открытый хроматин — доступные участки ДНК — более чем в 40 органах человека. В каждом эксперименте программное обеспечение уже помечало « пики», где ДНК особенно экспонирована. Вместо того чтобы рассматривать каждый набор данных отдельно, команда аккуратно наложила все эти списки пиков вдоль генома и объединила перекрывающиеся области. Затем они оценили, как часто каждая мельчайшая позиция внутри объединённых регионов отмечалась как открытая в разных экспериментах, превращая каждый регион в характерную форму, отражающую степень его воспроизводимости. Когда объединённый регион содержал несколько тесно расположенных открытых сайтов, его разделяли на несколько более простых единиц. Эти единицы — примерно 1,4 миллиона в сумме — стали наблюдаемыми консенсусными пиками, или cPeaks, кандидатами в справочный каталог доступности хроматина человека. 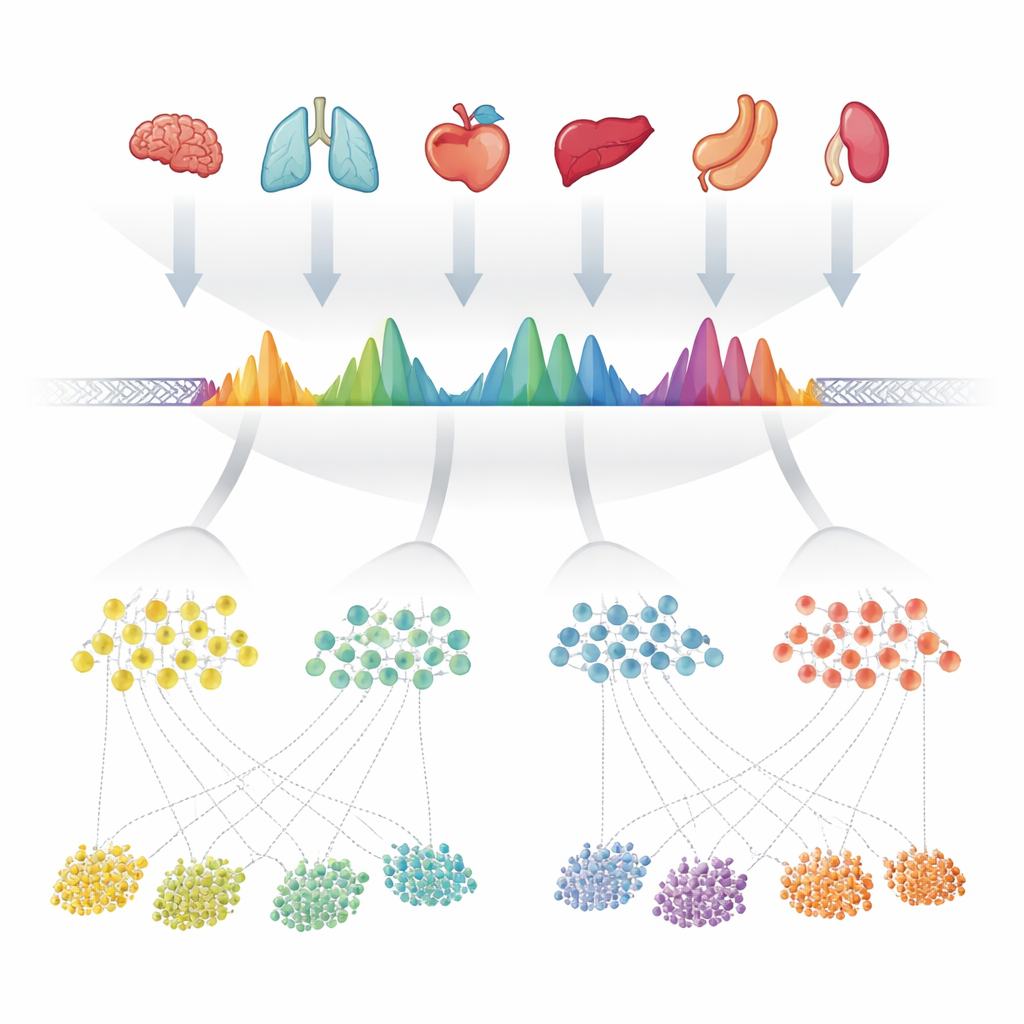
Стабильный отпечаток между тканями и технологиями
Чтобы быть полезным справочником, cPeaks должны отражать подлинные, повторяющиеся особенности генома, а не артефакты отдельных образцов или программ. Авторы проверили это, воссоздав свои объединённые регионы, используя только образцы крови, только плотные ткани, отдельные публичные базы данных и даже разные лабораторные методы обнаружения открытой ДНК. В каждом случае одни и те же геномные локусы давали удивительно похожие формы пиков, и большинство одноклеточных наборов данных, которые они исследовали, перекрывались с каталогом cPeaks более чем на 90% собственных пиков. Риды из многих органов точно сходились вокруг центров cPeaks, показывая, что эти регионы надёжно фиксируют места открытого хроматина. По сравнению с предыдущими справочными наборами, основанными на родственных технологиях, cPeaks покрывали больше доступной ДНК, обнаруженной в ATAC-seq экспериментах, и улавливали почти столько же сигнала, сколько пики, определённые заново в каждом наборе данных — несмотря на то, что cPeaks фиксированы и повторно используемы.
Обучение нейронной сети находить пропущенные регионы
Даже сотни существующих образцов не могут охватить все возможные типы клеток. Чтобы расширить карту в областях, ещё не наблюдавшихся, команда обратилась к глубинному обучению. Они обучили одномерную сверточную нейронную сеть на последовательностях ДНК: примеры, лежащие внутри наблюдаемых cPeaks, служили положительными образцами, тогда как случайно выбранные фоновые регионы — отрицательными. Модель научилась отличать их с высокой точностью, что указывает на наличие узнаваемых последовательностных паттернов в cPeaks. Когда исследователи намеренно скрывали пики, специфичные для одной ткани, сеть всё равно восстанавливала их по последовательности, включая редкие тканеспецифические сайты. Затем они скользили небольшим окном по остальной части генома, оценивая каждый сегмент и добавив примерно 280 000 высоко оценённых новых регионов в каталог как предсказанные cPeaks, что особенно улучшило покрытие для тканей, недостаточно представленных в исходных данных.
Связывание открытых регионов с генами, типами клеток и редкими клетками
Имея более богатый справочник, авторы спросили, для чего служат эти регионы. Многие cPeaks находятся рядом с участками начала и окончания генов или перекрывают известные регуляторные элементы, такие как промоторы, энхансеры и сайты связывания архитектурных белков вроде CTCF. Небольшое подмножество доступно почти во всех наборах данных; эти более длинные «домашние» cPeaks обычно располагаются в основных промоторных областях генов, необходимых для базового поддержания клетки. Команда также классифицировала cPeaks по тому, насколько острыми и согласованными являются их границы в разных образцах, что отражает, насколько точно прилегает ДНК к нуклеосомам. Регионы с чётко определёнными границами обогащены определёнными семействами транскрипционных факторов, которые известны тем, что перестраивают хроматин и направляют развитие. Когда cPeaks использовали в качестве набора признаков для анализа множества одноклеточных наборов данных, они улучшали точность маркировки типов клеток и особенно помогали выявлять редкие типы клеток и тонкие подтипы, которые предыдущие наборы пиков или простые геномные сетки часто слили воедино.
Отслеживание развития и рака с помощью общего языка
Сила стандартного справочника становится очевидной при сравнении очень разных биологических контекстов. С помощью cPeaks авторы переанализировали одноклеточные данные развивающейся человеческой сетчатки, крупные атласы эмбриональных и взрослых тканей и несколько видов рака. Им удалось реконструировать траектории развития и увидеть, что доля чётко ограниченных, «хорошо расположенных» cPeaks имеет тенденцию к увеличению на переходных стадиях, а затем уменьшаться по мере того, как клетки фиксируют стабильные идентичности. Аналогичная картина наблюдалась на стадиях опухолей: промежуточные стадии показывали более высокий процент этих структурированных регионов, что указывает на интенсивную перестройку регуляции. В одной опухоли яичника cPeaks помогли выявить два различных подклона раковых клеток с разными изменениями числа копий ДНК, демонстрируя, как справочник может выявлять скрытую сложность в болезни.
Что это означает для будущих исследований генома
Для неспециалистов cPeaks можно рассматривать как стандартизованный набор координат, отмечающих, где геном с наибольшей вероятностью физически открыт и активен в различных типах клеток человека. Выравнивая новые одноклеточные эксперименты по хроматину на эту общую карту, исследователи могут сопоставлять результаты между исследованиями, легче замечать редкие или переходные клеточные состояния и начинать строить крупномасштабные модели регуляции генов — подобно тому, как стандартизованные каталоги генов способствовали созданию атласов single-cell RNA. Текущий каталог cPeaks — это черновой вариант, который будет расти по мере поступления новых данных, но уже сейчас он даёт общий язык для описания доступности хроматина, приближая нас к единому представлению о том, как упаковка ДНК направляет развитие, здоровье и болезни. 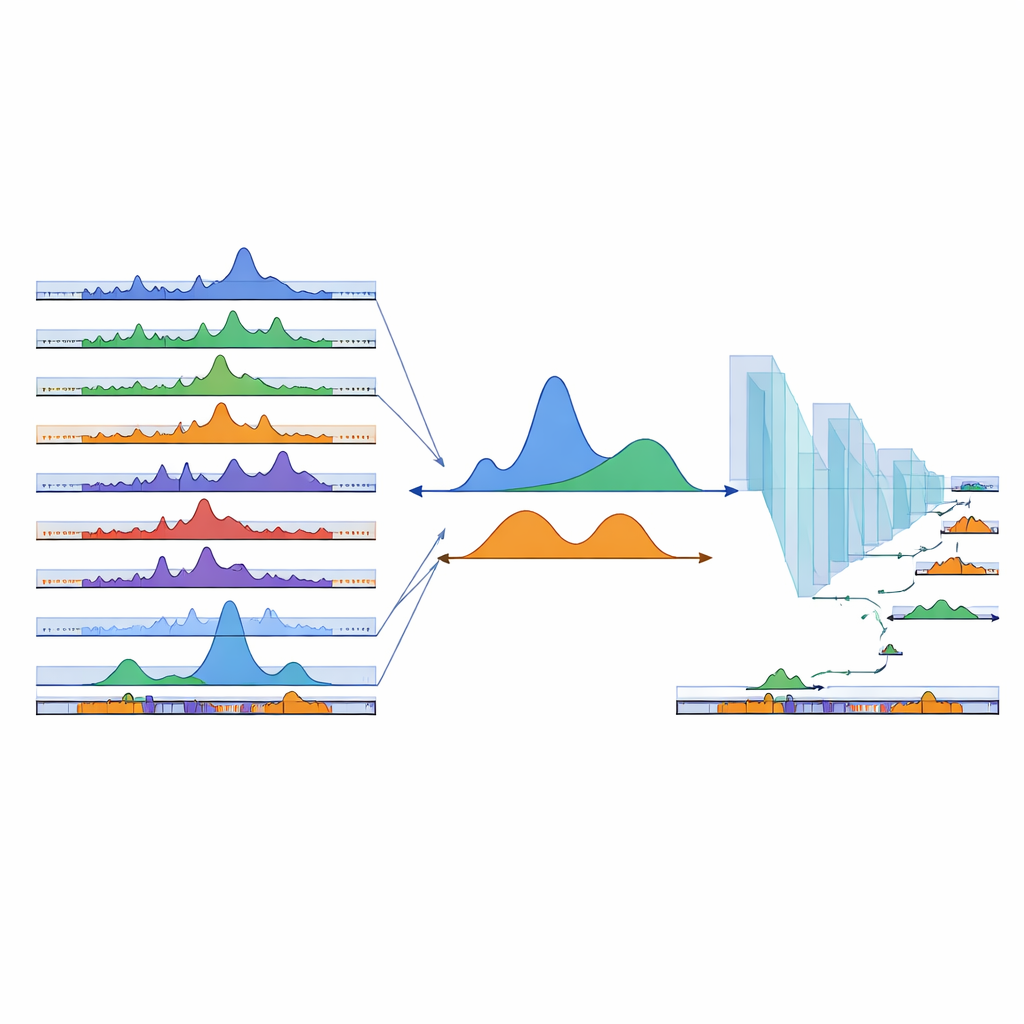
Цитирование: Meng, Q., Wu, X., Chen, W. et al. A generic reference defined by consensus peaks for single-cell ATAC-seq data analysis. Nat Commun 17, 2522 (2026). https://doi.org/10.1038/s41467-026-69461-6
Ключевые слова: доступность хроматина, single-cell ATAC-seq, консенсусные пики, регуляция генов, глубокое обучение в геномике