Clear Sky Science · ru
Тройное нацеливание на STING, TGF-β и PD-L1 усиливает сигнализацию CXCL16–CXCR6 для мощного антитуморного ответа
Преобразуя «холодные» опухоли в «горячие»
Иммунотерапия рака изменила подход к лечению у некоторых пациентов, но многие опухоли по‑прежнему сопротивляются этим мощным препаратам. В этом исследовании изучают, почему некоторые виды рака устойчивы к современным иммунным «контрольным точкам», и предлагают более умную, трёхзвенную атаку, которая пробуждает защитные силы организма, привлекает элитные киллерные T‑клетки и поддерживает их активность прямо в опухоли.
Почему существующих иммунных препаратов недостаточно
Большинство одобренных иммунотерапий нацелены на одну тормозящую цепь в иммунных клетках, например путь PD-1/PD-L1. Новый класс препаратов пытается пойти дальше, одновременно блокируя TGF-β — молекулу, которая сильно подавляет иммунитет при прогрессирующем раке. Один из таких препаратов, YM101, сочетает блокаду TGF-β и PD-L1 в одном антителе и показал обнадеживающие результаты на мышах. Но даже у генетически идентичных животных некоторые опухоли почти не уменьшались. Сравнив ответившие и устойчивые опухоли, исследователи обнаружили, что успешное лечение сопровождалось сильной «врождённой» иммунной активацией, особенно через путь STING, который распознаёт аномальную ДНК и запускает сигналы, похожие на противовирусную тревогу.
Добавление третьего рычага: путь STING
Предположив, что слабая врождённая активация — недостающее звено, команда комбинировала YM101 с пероральным агонистом STING под названием MSA-2 в нескольких мышиных моделях опухолей, включая обычно трудно поддающиеся лечению «холодные» опухоли. Тройной подход — активация STING в сочетании с блокадой TGF-β и PD-L1 — эффективнее сокращал опухоли, продлевал выживаемость и часто защищал мышей от регенерации опухоли при повторном введении, что указывает на длительную иммунную память. Это превзошло более традиционную пару агониста STING и блокады PD-L1 и даже усилило эффективность агониста STING при только блокированной TGF-β, показывая, что TGF-β сам по себе является значительным тормозом для STING‑опосредованного иммунитета. 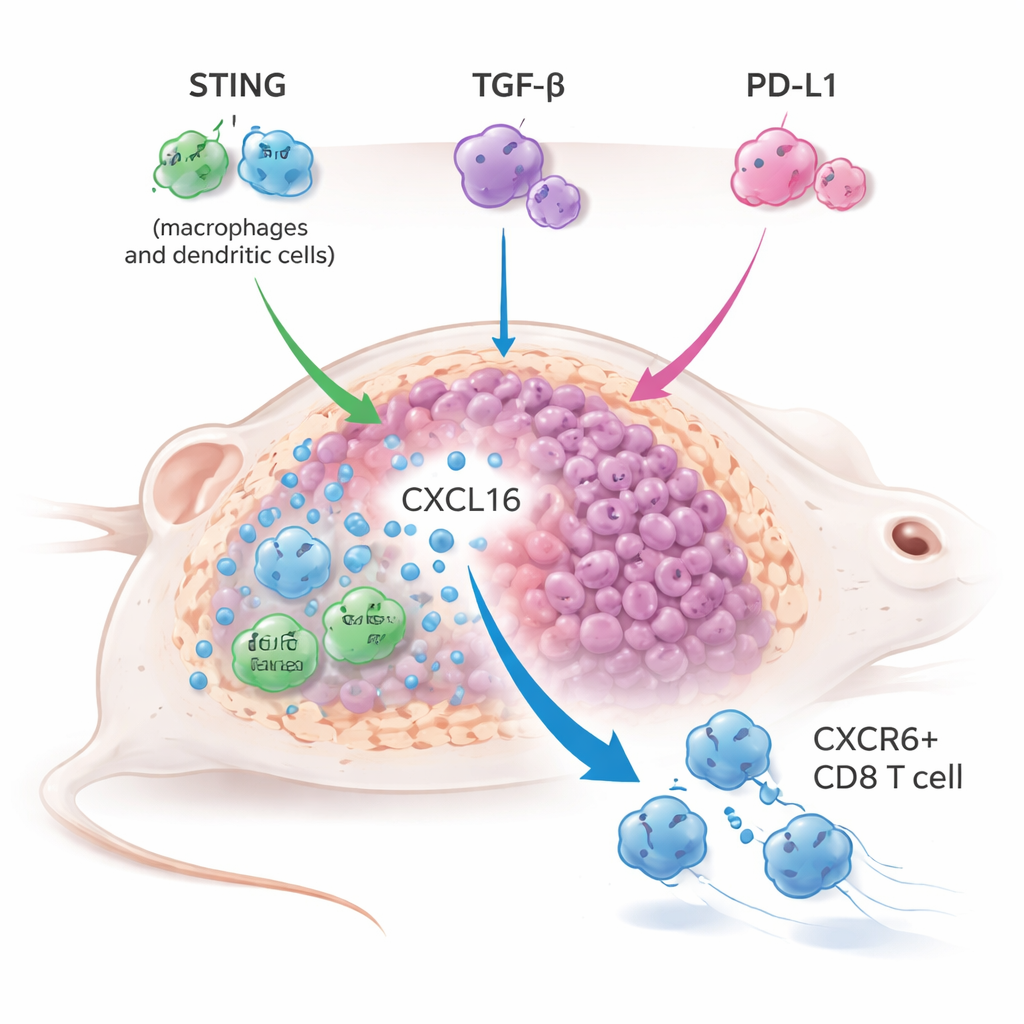
Привлечение специализированного отряда киллеров
Чтобы понять, как работала эта тройная стратегия, исследователи применили секвенирование РНК по отдельным клеткам и детальное иммунное профилирование обработанных опухолей. Они обнаружили заметное расширение специфического подмножества киллерных T‑клеток, помеченных рецептором CXCR6. Эти CXCR6+ CD8 T‑клетки были сильно вооружены — высоко экспрессировали гранзимы, перфорин и провоспалительные молекулы — и демонстрировали явные признаки активации и пролиферации. Одновременно макрофаги и дендритные клетки, ассоциированные с опухолью, увеличили производство хемокина CXCL16, который связывается с CXCR6 и помогает удерживать эти T‑клетки в опухоли. Когда связь CXCL16–CXCR6 была нарушена — либо путём блокирования CXCL16, либо путем генетического удаления CXCR6 в T‑клетках — комбинированное лечение почти полностью теряло свою антитуморную силу, доказывая, что эта ось является центральной для успеха терапии.
Как включается каскад сигналов
Углубляясь, команда выясняла, как активация STING и блокада TGF-β совместно повышают уровень CXCL16. В клетках человека и мышей агонисты STING сильно увеличивали CXCL16 и антивирусный цитокин IFN‑β, тогда как добавление TGF-β резко снижало оба показателя. Исследователи показали, что STING запускает сигналы IFN‑I, которые активируют транскрипционный фактор STAT1; STAT1 затем напрямую связывается с регуляторной областью гена CXCL16 и включает его экспрессию. TGF-β нарушает эту цепочку, мешая ключевому этапу STING‑сигналинга, вероятно через белок HDAC4 и реактивные формы кислорода, ослабляя активацию IRF3 и последующее производство IFN‑β и CXCL16. Блокада TGF-β снимает этот тормоз, позволяя агонистам STING в полной мере запускать путь STAT1–CXCL16 в миелоидных клетках и тем самым обеспечивать CXCR6+ T‑клетки сигналами, необходимыми для их удержания и борьбы в опухоли.
Создание единого точного препарата
Чтобы сделать эту сложную схему более практичной и нацеленной на опухоль, исследователи сконструировали единое «иммуностимулирующее антитело‑конъюгат» под названием Y101S. Эта молекула объединяет двунаправленное антитело, блокирующее TGF-β/PD-L1, с агонистом STING, прикреплённым через расщепляемый линкер. Y101S нацеливается на PD-L1‑положительные миелоидные клетки в опухоли, подвергается эндоцитозу и затем высвобождает STING‑препарат внутри этих клеток. В нескольких мышиных моделях рака Y101S сопоставимо или превосходило по эффективности комбинацию YM101 и высокодозного свободного агониста STING, несмотря на то, что содержало лишь крошечную долю той дозы STING. Он усиливал количество CXCL16+ макрофагов и дендритных клеток, расширял популяцию CXCR6+ CD8 T‑клеток, вызывал прочную иммунную память и концентрировал провоспалительные сигналы в опухолях, щадя здоровые органы, при благоприятном профиле безопасности у мышей. 
Что это значит для будущего лечения рака
Для неспециалистов ключевая мысль в том, что атака рака только одним или двумя иммунными переключателями может быть недостаточной — особенно когда опухоли активно отключают ранние системы тревоги. Эта работа показывает, что сочетание активации STING с блокадой TGF-β и PD-L1 может перестроить опухолевое окружение, мощно привлечь и поддержать специализированную группу киллерных T‑клеток и обеспечить более глубокие и долговременные ответы в доклинических моделях. Тройное нацеливание в виде антитело‑лекарственного конъюгата Y101S воплощает эту стратегию в одном целевом препарате и предлагает дорожную карту для иммунотерапий следующего поколения, направленных на опухоли, которые в настоящее время сопротивляются стандартным препаратам контроля иммунитета.
Цитирование: Yi, M., Li, T., Gu, Y. et al. Triple targeting of STING, TGF-β, and PD-L1 boosts CXCL16–CXCR6 signaling for potent antitumor response. Nat Commun 17, 1441 (2026). https://doi.org/10.1038/s41467-026-69456-3
Ключевые слова: иммунотерапия рака, путь STING, блокада TGF-бета, антитело против PD-L1, CXCL16 CXCR6 T-клетки