Clear Sky Science · ru
Положительная кооперативность между доменами связывания RAS и богатым цистеином регулирует кинетику связывания RAF с мембраной через боковое перевосстановление
Почему этот крошечный молекулярный танец важен
Внутри наших клеток решения «жить или умереть» о росте, делении и выживании часто принимаются на поверхности клеточной мембраны. Ключевой участник этих решений — белок RAF, который передаёт сигналы роста и часто оказывается неправильно настроенным при раке. В этом исследовании с беспрецедентной кинетической точностью показано, как RAF прикрепляется к мембране, как долго он там остаётся и почему плотные скопления другого белка, RAS, могут удерживать RAF активным дольше, чем можно было ожидать.
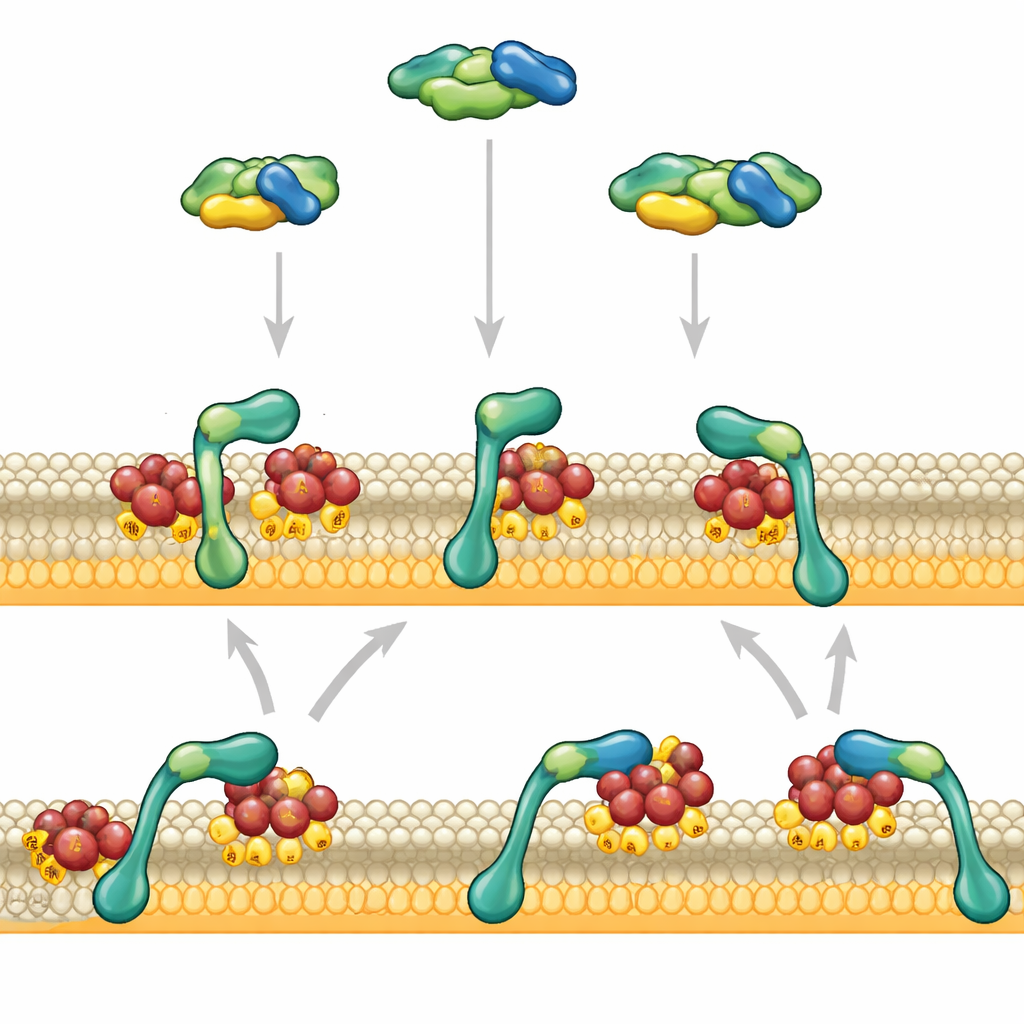
Сигналы, встречающиеся на поверхности клетки
RAF действует в крупной сигнальной магистрали, известной как путь MAPK, который связывает внешние сигналы, такие как факторы роста, с изменениями активности генов. В покое RAF плавает в цитоплазме в сложенном, самоподавленном состоянии. Он включается только при встрече с RAS, небольшим молекулярным переключателем, прикреплённым к внутренней поверхности клеточной мембраны. RAS должен быть в «включённом» состоянии и находиться в подходящей липидной среде, чтобы RAF был рекрутирован и активирован. Поскольку молекул RAF относительно мало по сравнению со многими другими компонентами сигнальной сети, то, как именно они взаимодействуют с мембраной и избегают преждевременного диссоциирования, сильно влияет на то, ответит ли клетка слабее или сильнее на сигнал роста.
Две «руки» для захвата мембраны
Авторы сосредоточились на двух областях на переднем конце RAF: одной, которая сцепляется с RAS, и другой, предпочитающей отрицательно заряженные липиды мембраны. Используя искусственные мембраны и очищенные белки, они наблюдали отдельные фрагменты RAF, связывающиеся с поверхностями, украшенными RAS, с помощью продвинутой микроскопии. Когда домен связывания RAS действовал в одиночку, он касался мембраны коротко и отпускал примерно за секунду. Домен, предпочитающий липиды, сам по себе почти не удерживался. Но когда эти два домена были связаны вместе, их поведение кардинально изменилось: RAF крепко прикреплялся и задерживался на мембране на десятки секунд, особенно если мембрана содержала много отрицательно заряженных липидов, похожих на липиды в настоящих клетках.
Кооперация, замедляющая уход
Это драматическое изменение возникло не потому, что RAF стал быстрее находить мембрану, а потому, что он медленнее с неё уходил. Сначала сегмент RAF, связывающийся с RAS, распознаёт активный RAS и швартует RAF у мембраны. Только после этого «первого рукопожатия» домен, связывающийся с липидами, полностью взаимодействует с окружающими липидами, замедляя боковое движение RAF и прочнее его якоря. Этот второй контакт, в свою очередь, стабилизирует исходное взаимодействие RAS–RAF, создавая положительную обратную связь между белково‑белковыми и белково‑липидными контактами. Эксперименты, изменявшие короткую петлю (линкер), соединяющую два домена, показали, что их тесная пространственная координация критична: увеличение гибкости или длины линкера ослабляло способность RAF оставаться на мембране.
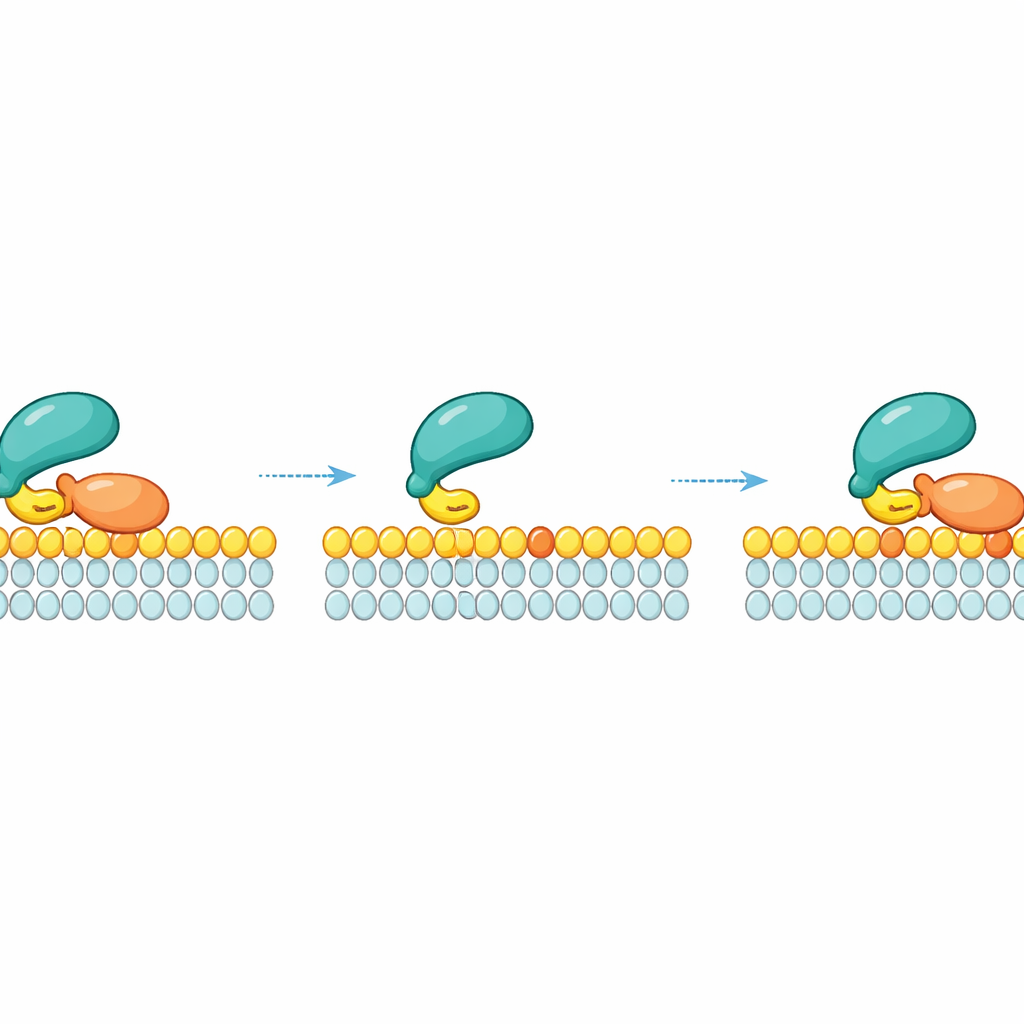
Боковое перевосстановление: скольжение вместо падения
Ключевая идея работы заключается в том, что RAF не просто отрывается в окружающую жидкость сразу после разрыва с конкретной молекулой RAS. Вместо этого, после освобождения от RAS, RAF может остаться кратковременно прикреплённым к мембране через слабый липидный контакт и соскользнуть вбок. Находясь в этом переходном состоянии, он может «перехватить» соседнюю молекулу RAS на том же участке мембраны. Это боковое перевосстановление создаёт кинетическую сеть безопасности: при высокой локальной плотности RAS — например, в нанокластерах, где молекулы RAS плотно упакованы — у RAF появляется много шансов вновь связаться с RAS прежде, чем он уйдёт. Измерения и моделирование показали, что чем выше плотность активного RAS на мембране, тем дольше RAF остаётся связанным с мембраной из‑за этих повторяющихся локальных перевязок.
От долгих визитов к надёжной активации
Продолжительное время пребывания RAF на мембране имеет важные последствия. Активация RAF — не одноразовое событие, а многоступенчатая последовательность, включающая конформационные изменения, снятие ингибирующих меток и объединение двух молекул RAF в активный димер. Исследование показывает, что лишь те молекулы RAF, которые задерживаются на мембране достаточно долго, могут завершить эту последовательность — форма «кинетической проверки», помогающая клеткам избегать случайной активации от мимолётных слабых сигналов. Описав, как взаимодействие связывания с RAS, контактов с липидами и бокового перевосстановления определяет время пребывания RAF на мембране, работа очерчивает общую стратегию, с помощью которой клетки могут использовать множество небольших слабых взаимодействий на мембранах для тонкой настройки мощных сигнальных путей.
Цитирование: Jimenez Salinas, A., Tevdorashvili, K., Grim, J. et al. Positive cooperativity between RAS-binding and cysteine-rich domains regulates RAF membrane binding kinetics via lateral rebinding. Nat Commun 17, 2593 (2026). https://doi.org/10.1038/s41467-026-69437-6
Ключевые слова: RAS, киназа RAF, сигнализация на клеточной мембране, боковое перевосстановление, кинетическая проверка