Clear Sky Science · ru
Секвенирование метилирования и гидроксиметилирования ДНК в контексте совмещённых хроматиновых признаков
Чтение химических заметок наших клеток
Каждая клетка организма несёт одинаковую ДНК, но нервные клетки, клетки кожи и стволовые клетки ведут себя очень по-разному. Одна из причин — клетки оставляют химические «заметки» на ДНК и на белках-упаковщиках ДНК, помогая включать или выключать гены. До сих пор учёным было трудно одновременно прочитать несколько таких заметок на одном и том же участке ДНК, что оставляло пробел в нашем понимании их совместной работы. В этом исследовании предложен новый метод, позволяющий одновременно читать и генетический код, и ключевые химические метки, раскрывая, как они объединяются для управления важными переключателями ДНК, называемыми энхансерами.
Зачем ДНК нужны пометки карандашом
ДНК не действует в одиночку. Она обёрнута вокруг белков, называемых гистонами, образуя хроматин, и как сама ДНК, так и гистоны могут быть украшены маленькими химическими группами. Две важные метки на ДНК — это метил и гидроксиметил, добавляемые к букве C (цитозин). Эти метки влияют на то, насколько плотно упакована ДНК и активен ли рядом лежащий ген. В общих чертах метильные метки часто ассоциируются с подавлением генов, тогда как гидроксиметильные метки чаще встречаются там, где гены активны. Но эффект этих меток зависит от локального контекста: от того, где именно они находятся в геноме и рядом с какими гистоновыми метками.
Проблема отдельных карт
Существующие методы секвенирования позволяют картировать метил и гидроксиметил по всему геному, а другие методы отображают гистоновые метки, указывающие на активные или молчащие участки. Однако обычно эти измерения выполняют в отдельных экспериментах и затем сравнивают в компьютере. Это показывает, какие признаки склонны сосуществовать в одном районе, но не доказывает, находятся ли они действительно на одном и том же фрагменте ДНК в отдельной клетке. Более ранние попытки объединить эти измерения опирались на жёсткие химические обработки, которые повреждали ДНК и, что важно, не позволяли надежно отличать метил от гидроксиметила в одном прочтении. В результате у исследователей не было чёткой молекулярной картины того, как комбинации меток взаимодействуют.
Новый метод многоуровневого чтения
Авторы разработали метод, названный 6-base-CUT&Tag, который может читать все четыре буквы ДНК плюс два химических состояния цитозина — обычный, метилированный и гидроксиметилированный — на фрагментах ДНК, физически прикреплённых к выбранным хроматиновым признакам. Сначала они используют антитела как молекулярные крючки, чтобы извлечь ДНК, обёрнутую вокруг гистонов с конкретной меткой, например меткой активного хроматина. Инженерный фермент затем вставляет специальные адаптеры, превращая каждый захваченный фрагмент ДНК в маленькую петлю, устойчивая к этапам очистки, разрушающим случайные обрывки. Далее уточнённый химический и ферментативный процесс переводит разные состояния цитозина в отличимые сигналы последовательности, которые могут прочитать современные секвенаторы. Таким образом одно прочтение сообщает, откуда пришёл фрагмент, какую гистоновую метку он нес и какие цитозины на нём были метилированы или гидроксиметилированы.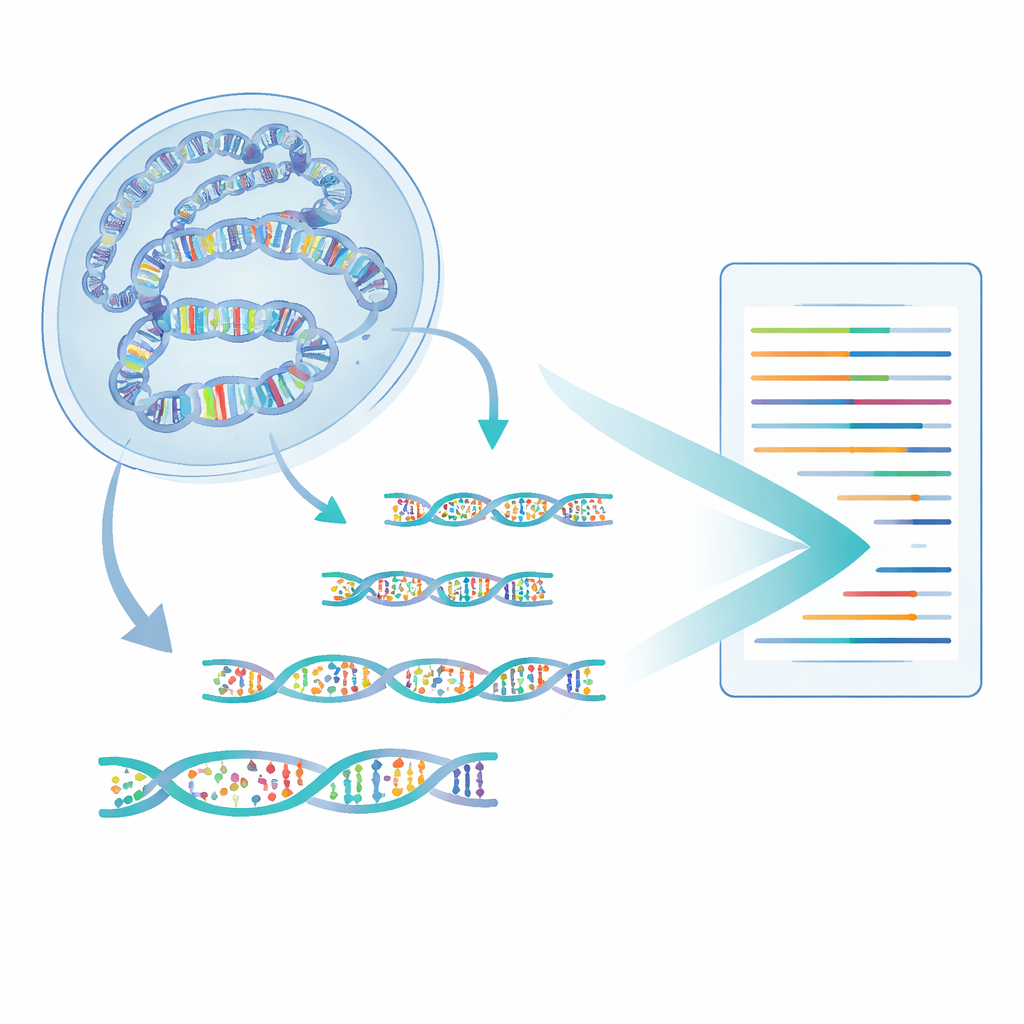
Приближение к генетическим переключателям
Используя в качестве тестового примера эмбриональные стволовые клетки мыши, команда применила 6-base-CUT&Tag к нескольким ключевым гистоновым меткам, маркирующим разные типы регуляторной ДНК. Они сосредоточились на энхансерах — участках ДНК, действующих как переключатели, контролирующие когда и где гены включаются. Энхансеры могут находиться в «активном», «подготовленном» или «готовом к активации» состояниях, различающихся по конкретным гистоновым меткам. Исследователи обнаружили, что энхансеры, помеченные только гистонной меткой H3K4me1 (часто рассматриваемой как «подготовленная»), несли самые высокие уровни как метил-, так и гидроксиметил-меток на ДНК, особенно при прямом изучении нуклеосом, связанных с H3K4me1. Напротив, энхансеры с признаками сильной активности или репрессии содержали меньше этих ДНК-меток или демонстрировали сдвиг в сторону гидроксиметилирования, что указывает на происходящее стирание метильных пометок.
Декодирование состояний энхансеров с большей точностью
Поскольку все типы энхансеров разделяют метку H3K4me1, команда спросила, может ли детальная картина ДНК-меток именно на H3K4me1-помеченной ДНК сама по себе различать состояния энхансеров. Они обучили модель машинного обучения на данных 6-base-CUT&Tag для классификации энхансеров как активных, подготовленных или готовых к активации, исключительно на основе того, сколько метила и гидроксиметила содержалось у них в этом единственном гистоновом контексте. Эта модель превзошла иначе идентичную модель, обученную на стандартных данных по всему геному, не ограниченных какой-либо гистоновой меткой. Иными словами, чтение ДНК-меток в непосредственном контексте их возникновения даёт более чёткую картину, чем усреднение по всей ДНК в клетке.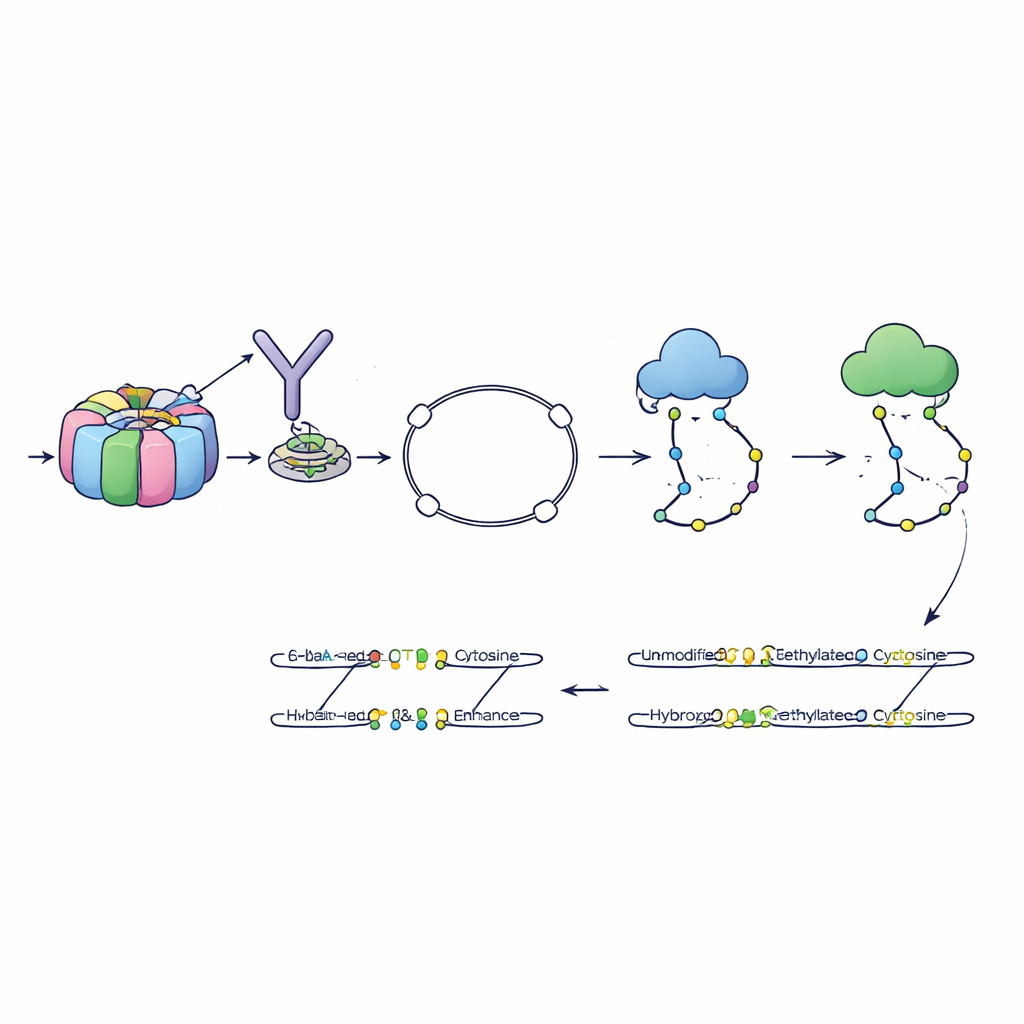
Что это значит для понимания клеточной идентичности
Для неспециалиста главный вывод в том, что этот метод позволяет учёным одновременно читать несколько уровней информации — последовательность ДНК, метки на ДНК и гистоновые метки — на одной и той же молекуле. Такой детальный взгляд показывает, как конкретные комбинации химических меток определяют готовность генетических переключателей в стволовых клетках. Поскольку 6-base-CUT&Tag эффективнее и менее разрушителен, чем предыдущие подходы, он может выявлять тонкие закономерности, которые ранее оставались скрытыми. Со временем это многоуровневое чтение хроматина может помочь объяснить, как клетки запоминают свою идентичность, как они меняются в ходе развития или при заболеваниях и как мы могли бы точнее нацеливать регуляторный код в терапиях.
Цитирование: Araujo Tavares, R.d.C., Dhir, S., He, X. et al. Sequencing DNA methylation and hydroxymethylation at co-occurring chromatin features. Nat Commun 17, 2591 (2026). https://doi.org/10.1038/s41467-026-69429-6
Ключевые слова: эпигенетика, метилирование ДНК, хроматин, энхансеры, стволовые клетки