Clear Sky Science · ru
Отсутствие MDA5 замедляет старение кроветворения, модулируя воспалительное старение и протеостаз у мышей
Почему важно сохранять молодую кровь по мере старения
С возрастом система, производящая клетки крови, постепенно изнашивается. Стволовые клетки в костном мозге, которые обычно пополняют эритроциты, иммунные клетки и тромбоциты, становятся более склонными к воспалению и с большей вероятностью производят одни типы клеток в ущерб другим. Этот сдвиг способствует анемии, ослаблению иммунитета и повышенному риску рака в пожилом возрасте. В данном исследовании изучается неожиданный участник этого процесса: антивирусный сенсор MDA5. Отключив этот одиночный белок у мышей, исследователи обнаружили, что стволовые клетки крови сохраняют функциональную «молодость» дольше.
Сенсор, созданный для борьбы с вирусами, который дает сбой с возрастом
MDA5 — это сенсор врожденного иммунитета, распознающий двуцепочечную РНК, молекулярный паттерн, распространенный при вирусах, но также образующийся из наших собственных геномов, особенно из активных мобильных генетических элементов, активность которых возрастает с годами. При распознавании такой РНК MDA5 запускает каскад воспалительных сигналов и антивирусных ответов. Команда поставила вопрос, не вызывает ли такая постоянная низкоуровневая активация у старых животных «воспалительное старение» — хроническое, тлеющее воспаление, сопровождающее старение — в костном мозге. Сравнивая нормальных мышей и мышей, лишенных MDA5, они измеряли множество иммунных сигнальных молекул в жидкости костного мозга. У старых мышей без MDA5 были заметно снижены уровни ключевых воспалительных цитокинов, включая интерферон-β и интерлейкин-1, и наблюдалось уменьшение активации воспалительных участков ДНК в стволовых клетках, что указывает на более спокойную, менее воспаленную среду.
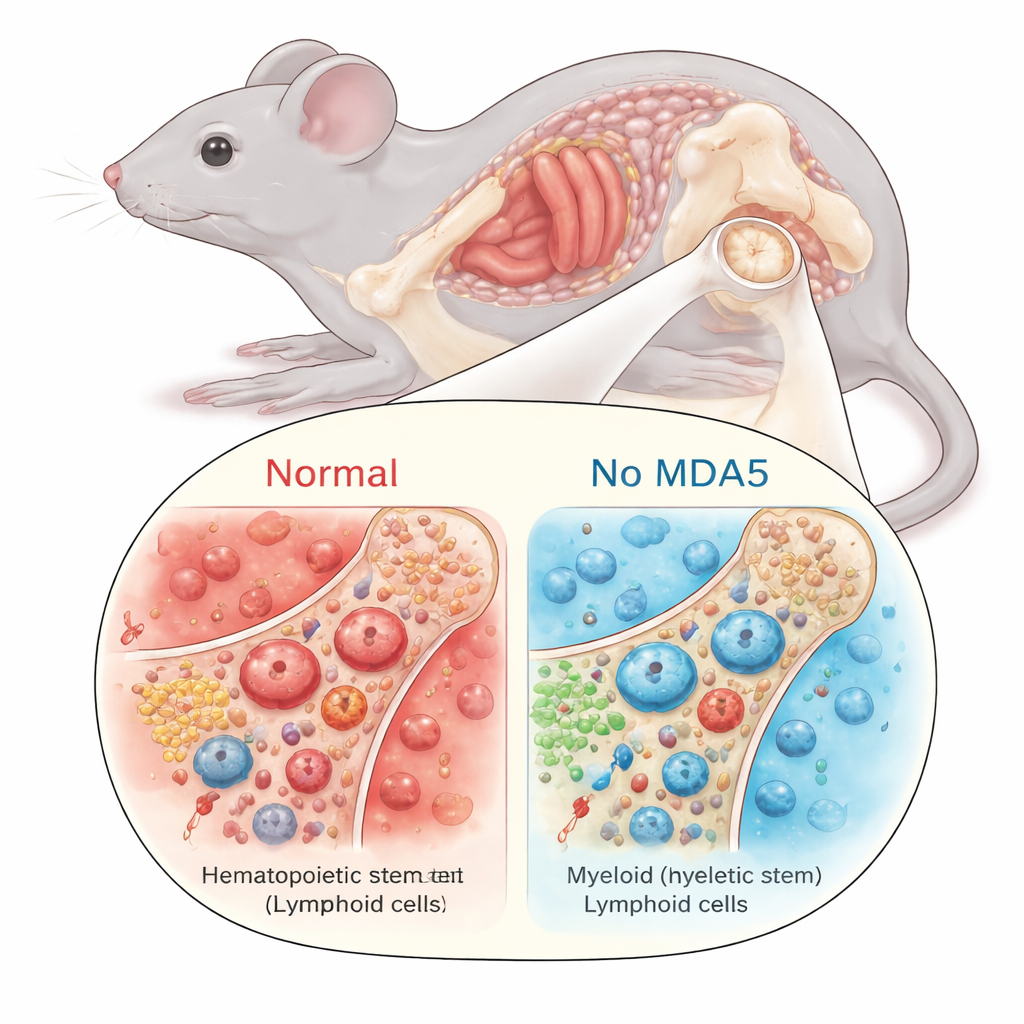
Более «молодое» поведение стареющих стволовых кроветворных клеток
При снижении воспаления в мозге стволовые клетки крови стали вести себя иначе. При обычном старении эти гемопоэтические стволовые клетки (HSC) склонны накапливаться в числе, но терять в качестве: они чаще делятся, теряют долгосрочную регенеративную способность и приобретают смещение в сторону продукции миелоидных клеток (например, некоторых типов лейкоцитов) за счет лимфоидных клеток, поддерживающих адаптивный иммунитет. У пожилых мышей без MDA5 эта типичная картина была сглажена. Их HSC меньше расширялись в количестве, демонстрировали уменьшенную миелоидную предрасположенность и оставались более покоящимися — проводили больше времени в состоянии покоя, а не в циклах деления. При пересадке равного числа стволовых клеток в облученных реципиентах пожилые HSC, лишенные MDA5, лучше восстанавливали систему крови в условиях без конкуренции, что свидетельствует о лучшем функциональном резерве по сравнению со взрослыми нормальными HSC.
Метаболизм и контроль качества белков остаются более молодыми
Помимо числа клеток и их поведения, исследователи изучили внутреннюю работу этих стволовых клеток. Сочетая анализ экспрессии генов, доступности хроматина, профилирование метаболитов и одноклеточные методы, они обнаружили, что потеря MDA5 сохраняет более молодую метаболическую и протеостатическую программу. У пожилых HSC без MDA5 были более благоприятные маркеры редокс‑состояния, такие как более низкий уровень окисленной глутатиона и более высокие уровни NAD и NADP — молекул, связанных с устойчивостью клетки. Внутри этих клеток было меньше неправильно свернутых и несвернутых белков — признака старения и стресса — тогда как маркеры аутопагии, процесса утилизации поврежденных компонентов, были повышены. Синтез белка был ослаблен, а аминокислоты накапливались, что согласуется со сдвигом в сторону тщательного контроля качества белков, а не быстрого, подверженного ошибкам синтеза.
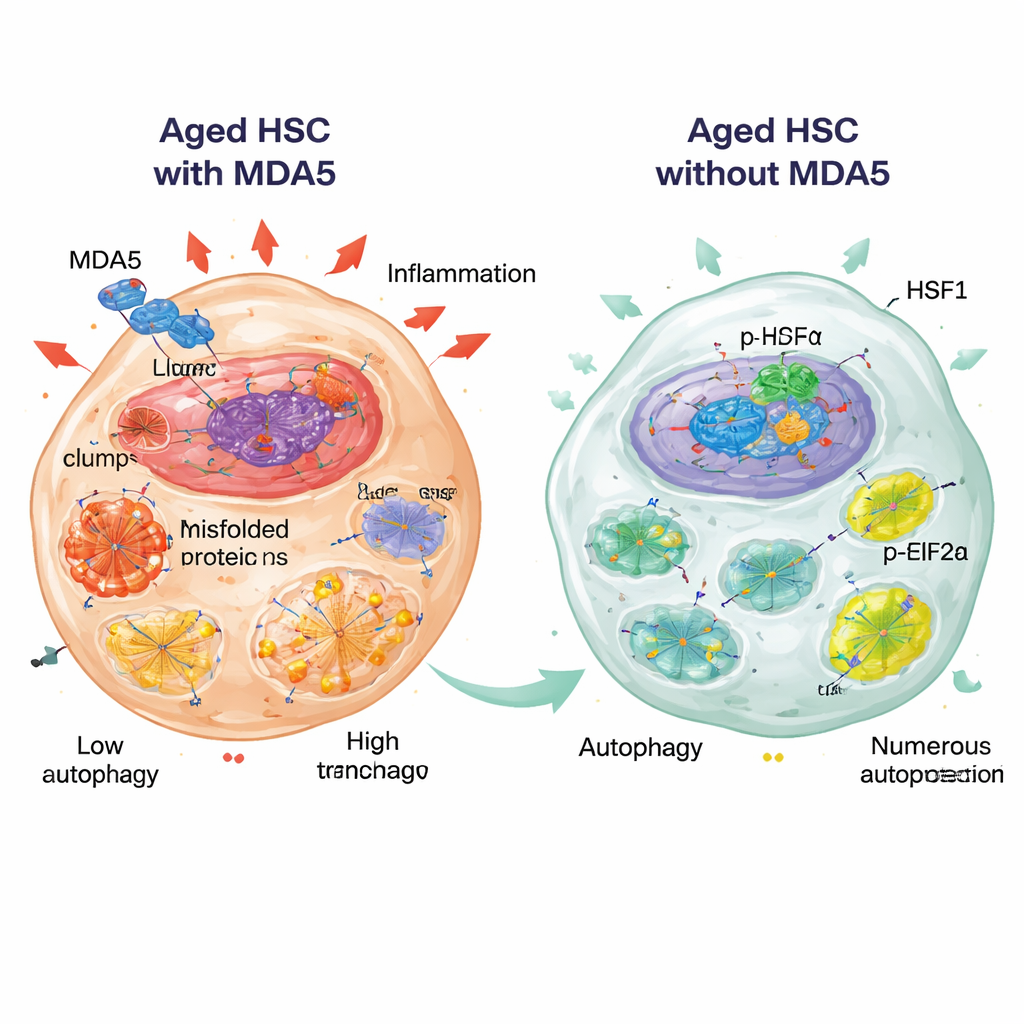
HSF1 и eIF2α: сторожа протеостаза
Два молекулярных регулятора оказались центральными для этого защитного состояния: HSF1, главный транскрипционный фактор, усиливающий продукцию шаперонов и других белков-защитников, и eIF2α, фактор трансляции, фосфорилированная форма которого (p-eIF2α) замедляет синтез белка при стрессе. В пожилых HSC без MDA5 уровни белка HSF1 и его локализация в ядре были повышены, а p-eIF2α также увеличен, что согласуется с активной программой защиты от стресса. Авторы обнаружили, что MDA5 может находиться в близкой физической близости с HSF1 и при сверхэкспрессии удерживать HSF1 в цитоплазме, что предполагает, что активный MDA5 может ограничивать полезные ядерные функции HSF1. Важно, что при фармакологической активации HSF1 в пожилых нормальных HSC с помощью малой молекулы эти клетки становились более покоящимися и лучше сохраняли способность формировать колонии при повторных культивированиях, частично имитируя «молодые» черты, наблюдаемые при отсутствии MDA5.
Что это значит для поддержания здоровья крови при старении
Вместе эти результаты рисуют картину, в которой хроническая активация антивирусного сенсора MDA5 постепенно толкает гемопоэтические стволовые клетки в состояние воспаления, метаболического стресса и повреждения белков. Удаление MDA5 у мышей прерывает этот цикл: воспалительные сигналы в костном мозге ослабляются, HSC остаются более отдохнувшими и менее смещенными по профилю, а их внутренние системы контроля качества белков сохраняют работоспособность. Хотя прямое выключение MDA5 у людей было бы рискованным из‑за его роли в борьбе с инфекциями, эта работа подчеркивает более общий принцип: нацеленность на возраст‑ассоциированное воспаление и укрепление протеостаза может помочь сохранить функцию стволовых клеток крови в поздней жизни. В долгосрочной перспективе более безопасные способы модуляции путей, связанных с MDA5, или усиления стресс‑ответов, управляемых HSF1 и eIF2α, могут предложить стратегии по продлению здорового срока службы нашей крови и иммунной системы.
Цитирование: Bergo, V., Bousounis, P., To Vu, G. et al. Lack of MDA5 delays hematopoietic aging by modulating inflammaging and proteostasis in mice. Nat Commun 17, 1645 (2026). https://doi.org/10.1038/s41467-026-69424-x
Ключевые слова: стволовые клетки крови, воспалительное старение, MDA5, протеостаз, старение крови