Clear Sky Science · ru
Структурные и молекулярные основания аллостерической регуляции и каталитической связи человеческой фосфорибозилформилглицинамидазной синтетазы
Почему этот фермент важен для здоровья
Каждая клетка вашего тела зависит от пуринов — небольших молекул, которые приводят в движение реакции, хранят энергию и несут генетическую информацию. Раковые клетки, которые быстро делятся, особенно нуждаются в пуринах и часто перестраивают пути их синтеза. В этом исследовании изучается человеческий фермент FGAMS, ключевой участник синтеза пуринов «с нуля». Раскрывая трехмерную структуру FGAMS и то, как его части движутся и взаимодействуют, авторы выясняют, как фермент включается и выключается, и как его можно нацелить, чтобы замедлить рост опухолей.
Строительные блоки жизни под контролем
Клетки синтезируют пурины по требовательной конвейерной цепочке, известной как путь de novo, который использует энергию и несколько ферментов для сборки сложного кольца. FGAMS выполняет четвертый шаг в этой последовательности и находится в центре более крупного ферментного комплекса — пуринозомы, который помогает эффективно направлять субстраты. Поскольку быстро растущие раковые клетки часто усиливают этот путь, такие ферменты, как FGAMS, представляют собой привлекательные мишени для лекарств: их блокирование может лишить опухоли нуклеотидов, необходимых для роста, тогда как здоровые клетки смогут переключиться на пути утилизации.
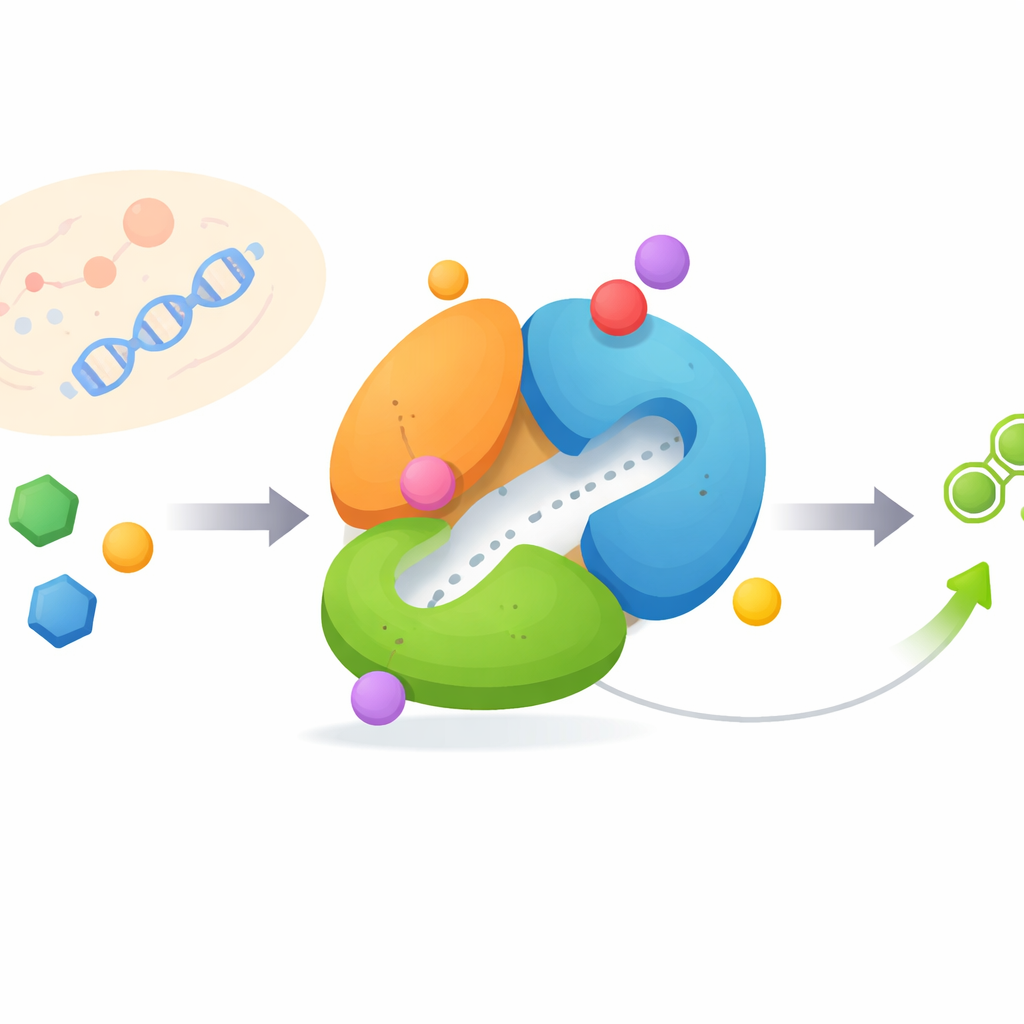
Машина, меняющая форму
FGAMS состоит из трех связанных между собой доменов, каждый из которых выполняет свою задачу и должен кооперировать в точной последовательности. Один домен отщепляет аммиак от аминокислоты глутамина, другой использует этот аммиак для модификации малой сахаро-содержащей молекулы, а третий домен служит регуляторным узлом. С помощью крио-электронной микроскопии высокого разрешения исследователи захватили FGAMS в трех различных рабочих состояниях: при связанном переносчике энергии, с захваченным кратковременным реактивным интермедиатом и с одновременным присутствием нескольких субстратов и интермедиатов. Сравнение этих состояний показало, что гибкие петли и N-концевой «рычаг» движутся драматически, переконфигурируя фермент по мере протекания реакции.
Скрытый туннель и молекулярные ворота
Ключевой загадкой было то, как аммиак, высвобождаемый в одном домене, безопасно перемещается к удаленному месту его использования, не диффундируя и не причиняя вреда. Новые структуры выявляют ранее невидимый внутренний туннель, соединяющий оба сайта, а также ряд «ворот», образованных специфическими аминокислотами. Когда правильные субстраты связываются и формируется интермедиат, центральная петля резко упорядочивается, натягивая N-концевой домен и переставляя соседние петли в каталитическом домене. Эта хореография открывает два входных шлюза, позволяя перерабатываться глутамину, и кратковременно перестраивает участок, стабилизирующий высокоэнергетический интермедиат, необходимый для разрыва связей.
Связывание химии через движение
По мере протекания реакции фермент не просто ждет; он использует каждый химический шаг как сигнал. Как только в домене, генерирующем аммиак, формируется ковалентный тиоэстерный интермедиат, ранние движения частично обращаются. Это ослабляет центральную петлю и переставляет ворота так, что пути утечки закрываются, в то время как две дополнительные заслонки по обеим концам туннеля открываются. Тонкие сдвиги в нескольких «узких» остатках расширяют внутренний проход, позволяя молекуле аммиака пройти по туннелю прямо во второй активный центр, где она реагирует с захваченным интермедиатом и образует конечный продукт. Мутации в Residues ворот приводят к утечке аммиака или рассоединению двух половин реакции, подтверждая, что эта система ворот и канала необходима для эффективного катализа.
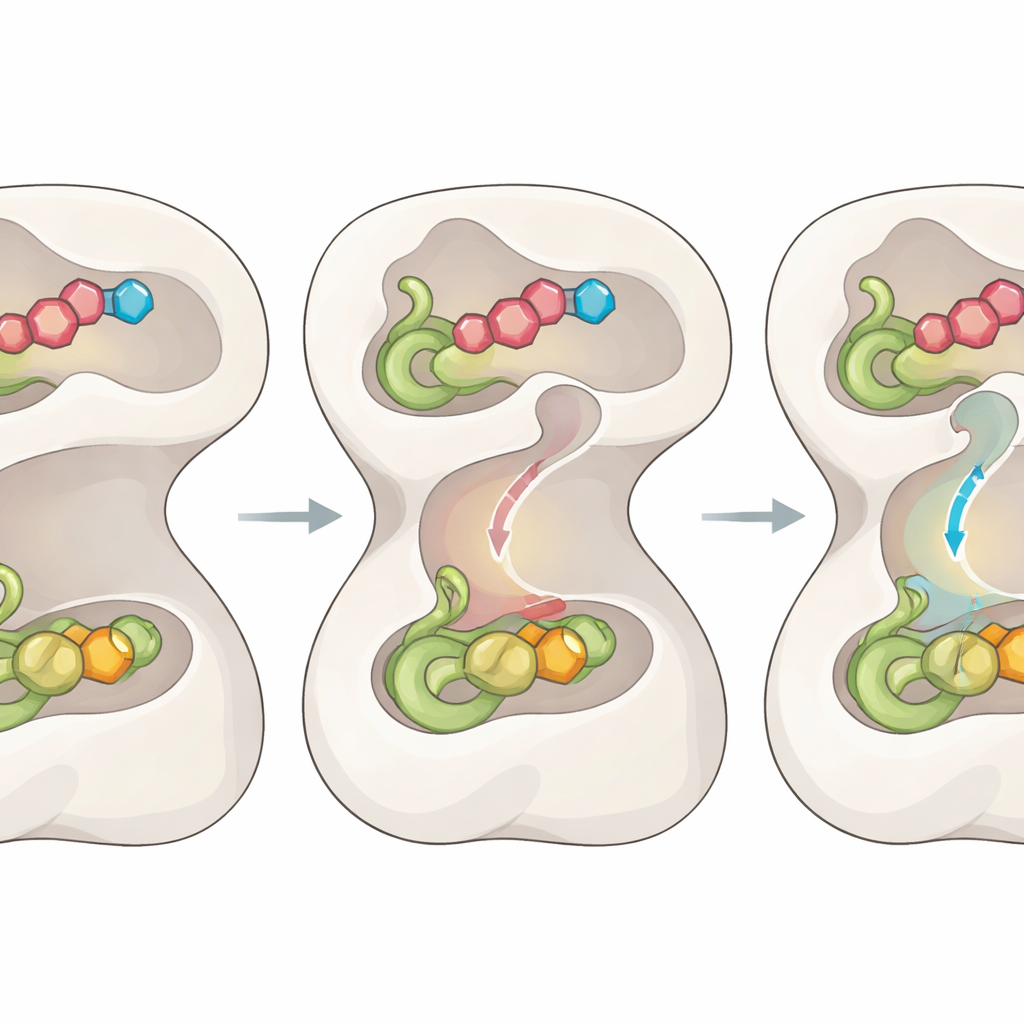
От структурного понимания к терапевтическим путям
Проследив FGAMS через его каталитический цикл, исследование рисует детализированную картину того, как движения доменов, гибкие петли, внутренние ворота и временный туннель связаны между собой для координации химии. Для широкой аудитории вывод прост: фермент действует как крошечная программируемая фабрика — он открывает «двери» и внутренний конвейер только тогда, когда все нужные компоненты на месте, обеспечивая скорость и безопасность процесса. Поскольку FGAMS поддерживает производство пуринов в раковых клетках и связан с плохим прогнозом при опухолях печени, структурные чертежи и недавно выявленные контрольные точки предлагают несколько точек приложения для разработки препаратов, которые блокируют туннель, замораживают ворота или захватывают ключевые интермедиаты, потенциально давая начало новому классу целенаправленных противораковых терапий.
Цитирование: Sharma, N., Zhou, W. & French, J.B. Structural and molecular basis for allosteric regulation and catalytic coupling of human phosphoribosylformylglycinamidine synthase. Nat Commun 17, 2732 (2026). https://doi.org/10.1038/s41467-026-69423-y
Ключевые слова: биосинтез пуринов, аллостерическая регуляция, канализация аммиака, метаболизм рака, крио-ЭМ структура