Clear Sky Science · ru
Микроокружение гранулем, направляющее соно-иммунотерапию для лечения и предотвращения рецидивов туберкулёза
Почему этот новый подход к туберкулёзу важен
Туберкулёз по-прежнему инфицирует четверть населения Земли и может возвращаться даже после длительного курса антибиотиков. В этом исследовании описана целенаправленная «звуковая плюс иммунная» терапия, которая нацелена не только на уничтожение бактерий туберкулёза, скрывающихся глубоко в лёгких, но и на переподготовку иммунной системы, чтобы болезнь значительно реже рецидивировала. Подход сочетает анализ образцов от пациентов с умной наночастицей, активируемой медицинским ультразвуком.
Скрытое поле боя внутри лёгочных узелков
Когда возбудители туберкулёза проникают в лёгкие, иммунные клетки стенки лёгкого изолируются в плотные узлы ткани, называемые гранулёмами. Эти структуры предназначены для камеры бактерий, но они также создают укрытую нишу, где микробы могут затаиться и ускользать от действия антибиотиков. Переанализировав данные одноядерной РНК-секвенции (single-cell RNA-seq) из человеческой лёгочной ткани, исследователи сравнили обычные нетуберкулёзные гранулёмы с истинными туберкулёзными гранулёмами и со здоровыми лёгкими. Они обнаружили, что в туберкулёзных очагах ключевые «первоприступные» клетки — макрофаги и дендритные клетки — перешли в приглушённое состояние. Молекулярные пути, которые обычно распознают бактерии и подают сигнал тревоги, были подавлены, тогда как гены, ослабляющие иммунную активность, оказались усилены.
Когда иммунная система включает тормоза
Далее команда изучила образцы крови людей с лекарственно-устойчивым и лекарственно-чувствительным туберкулёзом, а также пациентов, у которых болезнь либо рецидивировала, либо оставалась излеченной. Во всех группах проявилась одинаковая картина: гены и пути, негативно регулирующие иммунитет, были более активны у тех, у кого наблюдалась лекарственная устойчивость и рецидив. Сигналы, которые должны помогать иммунным клеткам распознавать и устранять бактерии, были слабее. Это указывало на то, что неудача лечения связана не только с лекарствами или бактериями, но и с иммунной средой, сдвинутой в чрезмерно сдержанный, «толерантный» режим, особенно внутри гранулём.
Конструирование звукоактивируемой вспомогательной частицы
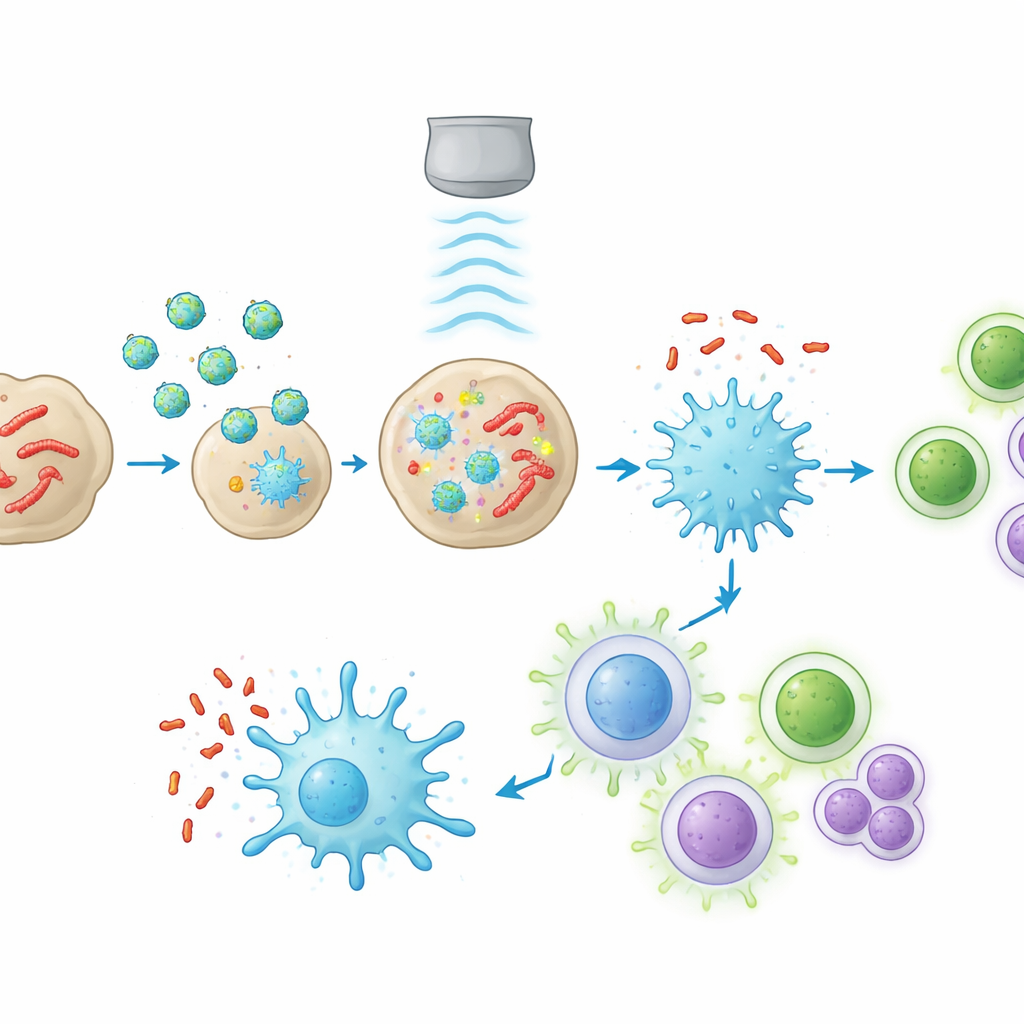
Руководствуясь этой картиной иммунного «паралича», исследователи создали наночастицу под названием manSNI. Она построена из органического полупроводящего полимера, способного генерировать всплески реактивных видов кислорода (ROS) при воздействии ультразвука, покрыта маннозной оболочкой для нацеливания на макрофаги и содержит небольшой иммунно-активирующий молекулярный компонент, стимулирующий толл-подобный рецептор на этих клетках. В пробирках частицы manSNI накапливались в лизосомах инфицированных макрофагов и под ультразвуком производили достаточно ROS, чтобы уничтожить более 99% модельных бактерий туберкулёза, даже когда ультразвук проходил через несколько сантиметров ткани. ROS также разрушали бактериальные мембраны, высвобождая бактериальные белки, которые могут выступать в роли антигенов.
Преобразование «холодной» гранулёмы в «горячий» иммунный узел
У мышей с лёгочным заболеванием, похожим на туберкулёз, manSNI накапливался в гранулёмах гораздо лучше, чем аналогичные частицы без маннозной направляющей группы. Когда лёгкие кратковременно подвергали ультразвуку, количество бактерий в лёгком снизилось практически до нуля. В то же время локальный иммунный ландшафт трансформировался: макрофаги сместились в провоспалительное, антибактериальное состояние; дендритные клетки созрели и перенесли информацию об антигенах в близлежащие лимфатические узлы; а специфические к туберкулёзу Т‑клетки и В‑клетки, продуцирующие антитела, расширились в численности. Анализ экспрессии генов лёгочной ткани показал, что несколько ключевых путей распознавания и защиты, ранее подавленных в человеческих гранулёмах, теперь были сильно реактивированы.
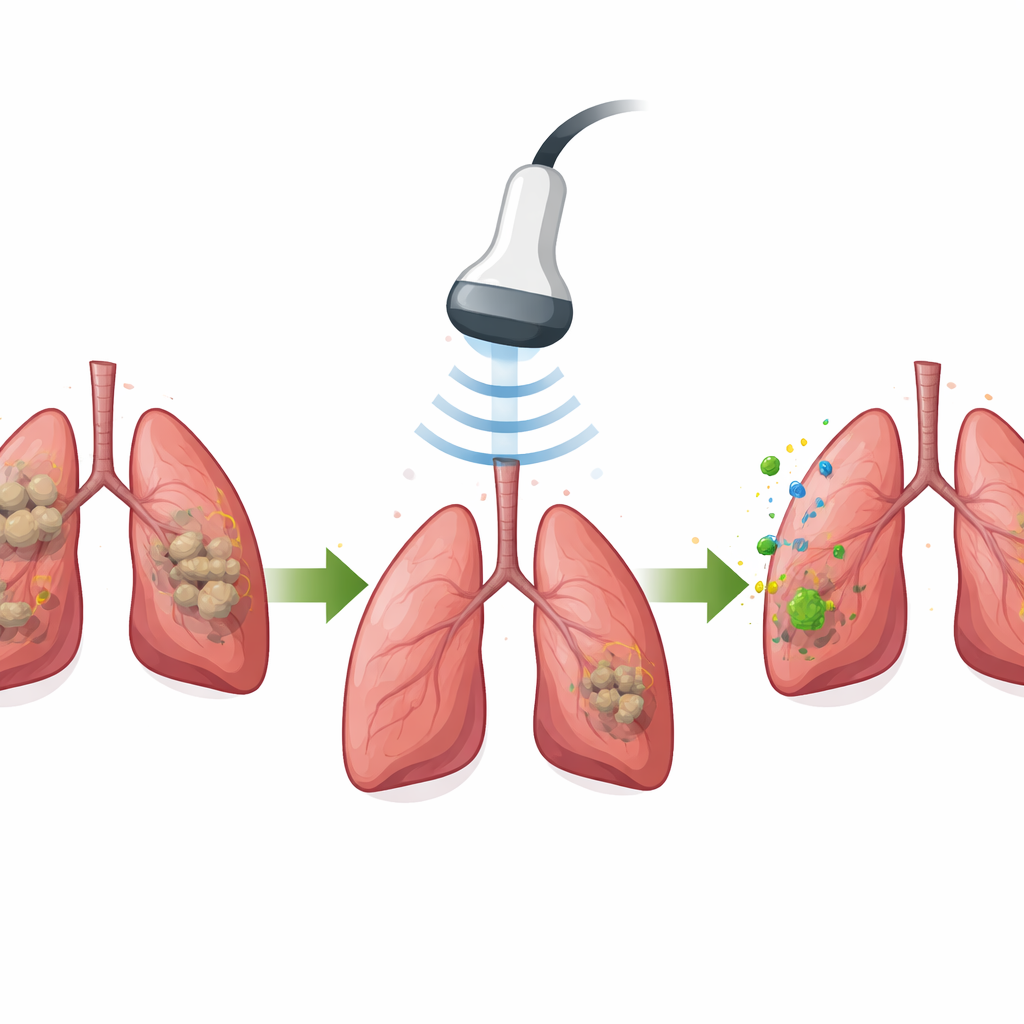
Формирование длительной защиты от рецидива и повторного заражения
Устранение первичной инфекции — лишь часть задачи; многие пациенты вновь сталкиваются с туберкулёзом либо из‑за сохраняющихся бактерий, либо из‑за нового заражения. В долгосрочных исследованиях на мышах авторы сравнили стандартный антибиотик (рифампицин) с manSNI в сочетании с ультразвуком. Оба режима первоначально устраняли обнаруживаемые бактерии, но рецидивы были обычным явлением при приёме только антибиотиков, тогда как после соно‑иммунотерапии рецидивы встречались редко. Животные, получавшие manSNI, развивали более высокий уровень тканевых резидентных Т‑клеток памяти в лёгких, центральных и эффекторных Т‑клеток памяти в лимфоидных органах, а также долговременные В‑клетки памяти и антитела в крови. При целенаправленном повторном воздействии модельными бактериями у большинства таких мышей наблюдалась стойкость к повторному заражению или лишь лёгкие, кратковременные поражения.
Что это может означать для будущего лечения туберкулёза
Для неспециалиста главный вывод состоит в том, что эта работа предлагает двухэтапную стратегию: непосредственно уничтожать бактерии, скрывающиеся в труднодоступных узелках лёгких, и одновременно переводить локальную иммунную среду из состояния «выключено» в состояние «включено». Подход использует ультразвук — уже широко применяемый в клиниках — чтобы неинвазивно активировать точно нацеленную наночастицу, которая и убивает возбудителей, и действует как встроенный усилитель вакцины. Хотя эксперименты проведены на мышах и с более безопасными модельными штаммами, а не с наиболее опасными штаммами туберкулёза, результаты указывают на путь к более коротким и эффективным лечебным схемам, которые не только излечивают туберкулёз, но и значительно снижают вероятность его возвращения.
Цитирование: Wang, W., Li, F., Mo, W. et al. Granulomas microenvironment-guided sono-immunotherapy to treat and prevent recurrence of tuberculosis. Nat Commun 17, 2595 (2026). https://doi.org/10.1038/s41467-026-69420-1
Ключевые слова: туберкулёз, соно-иммунотерапия, наночастицы, гранулёмы, ультразвуковая терапия