Clear Sky Science · ru
Молекулярный механизм действия малой молекулы SMT-738 на транспортер бактериальных липопротеинов LolCDE
Почему этот новый антибиотик важен
По мере того как все больше госпитальных инфекций становятся невосприимчивыми к нашим лучшим антибиотикам, врачам срочно требуются препараты, которые убивают опасные бактерии, не разрушая при этом полезную микробиоту хозяина. В этом исследовании раскрывается, как перспективное экспериментальное соединение SMT-738 блокирует ключевой транспортный механизм в внешней оболочке некоторых трудноизлечимых бактерий. Точное определение участка и способа, которыми препарат заедает механизм, открывает путь к более продуманным антибиотикам, направленным на супербактерии при щадящем воздействии на кишечную микробиоту.
Внешняя броня вредных бактерий
Многие из наиболее опасных госпитальных патогенов относятся к группе, известной как граммотрицательные бактерии. Их трудно уничтожить, потому что они окружены двуслойной внешней оболочкой. Эта внешняя прослойка создается и поддерживается рядом молекулярных машин, которые транспортируют ключевые строительные блоки из внутренней мембраны, где они синтезируются, на поверхность. Одним из важных грузов являются липопротеины, которые помогают сохранять целостность внешней оболочки и участвуют в процессах, таких как захват питательных веществ и устойчивость к антибиотикам. Транспортная система, называемая путём Lol, и в частности насос LolCDE, извлекает липопротеины из внутренней мембраны и передаёт их шаперонам, доставляющим их к внешней поверхности. Поскольку эти шаги необходимы для выживания клетки, они представляют собой привлекательные мишени для новых антибиотиков.
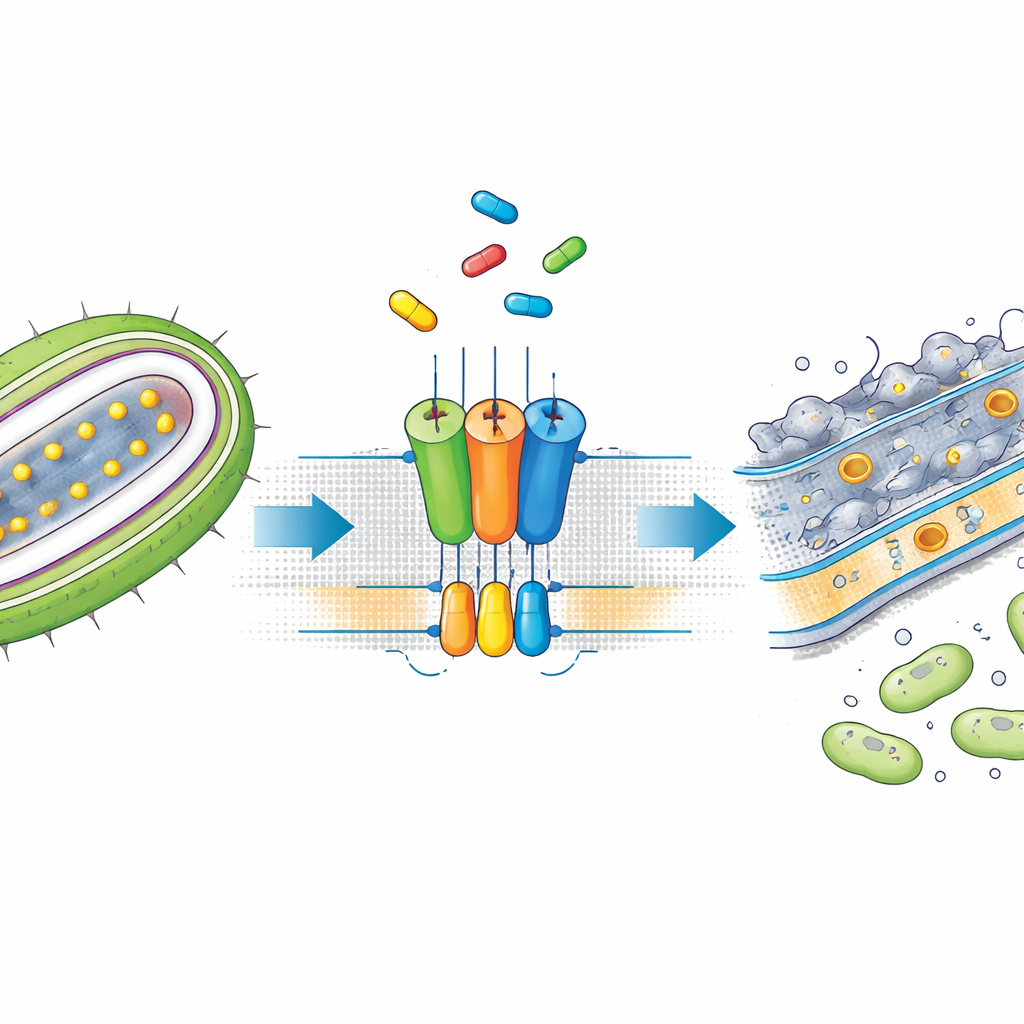
Малая молекула, останавливающая конвейер
SMT-738 был выявлен в ранних скринингах как мощный ингибитор граммотрицательных патогенов из семейства Enterobacteriaceae, включая штаммы Escherichia coli и Klebsiella pneumoniae, устойчивые к нескольким препаратам. Однако точный механизм его действия оставался неясным. Авторы сначала показали, что SMT-738 препятствует высвобождению тестового липопротеина из LolCDE в конструктивно модифицированных бактериях, подтверждая, что препарат действительно останавливает шаг транспорта. Важно, что при наличии определённых мутаций в генах комплекса LolCDE бактерии становились резистентными к SMT-738, что указывает на прямое связывание препарата с этим насосом. Эти наблюдения подготовили почву для структурного исследования взаимодействия соединения с транспортером.
Заклинивание насоса изнутри
С помощью высокоразрешающей крио-электронной микроскопии исследователи получили трёхмерное изображение LolCDE со связанным SMT-738. Структура показывает, что препарат закреплён в кармане на периплазматическом конце — со стороны, обращённой в пространство между внутренней и наружной мембранами — между двумя основных субъединицами, LolC и LolE. Это место частично совпадает с нормальной зоной посадки для липопротеинового груза. Когда SMT-738 занимает этот карман, окружающие аминокислоты в LolC и LolE смещаются на величину до примерно одного нанометра. Эти движения создают стерические столкновения с положением, в котором обычно располагался бы липопротеин с его жирными хвостами, эффективно блокируя вход груза в насос. Мутации во многих остатках, выстилающих этот карман, либо ослабляли связывание препарата, либо делали бактерии резистентными, что чётко соответствует структурной картине.
Запуск одностороннего разрушения
История не заканчивается на сайте связывания. LolCDE приводится в движение двумя копиями моторной субъединицы LolD, расположенными со стороны цитоплазмы и расходующими ATP для обеспечения транспорта. Поразительно, что в структуре со связанным SMT-738 прикреплён была только одна молекула LolD; партнёрная LolD диссоциировала. Биохимические гели и ATPазные анализы подтвердили, что связывание SMT-738 вызывает утрату одной LolD и резкое снижение активности по превращению энергии насоса. Компьютерные моделирования транспортера в мембране подкрепили эту картину: при посадке SMT-738 в карман по структуре прошли конформационные изменения вниз по цепочке, подталкивающие сцепные спирали, которые связывают LolC и LolE с LolD. Эти сдвиги создавали неблагоприятное столкновение для LolD, связанной с LolC, в результате чего она отваливалась, тогда как LolD, связанная с LolE, оставалась на месте. В итоге образуется асимметричная «засlocked» машина, которая больше не способна транспортировать липопротеины.
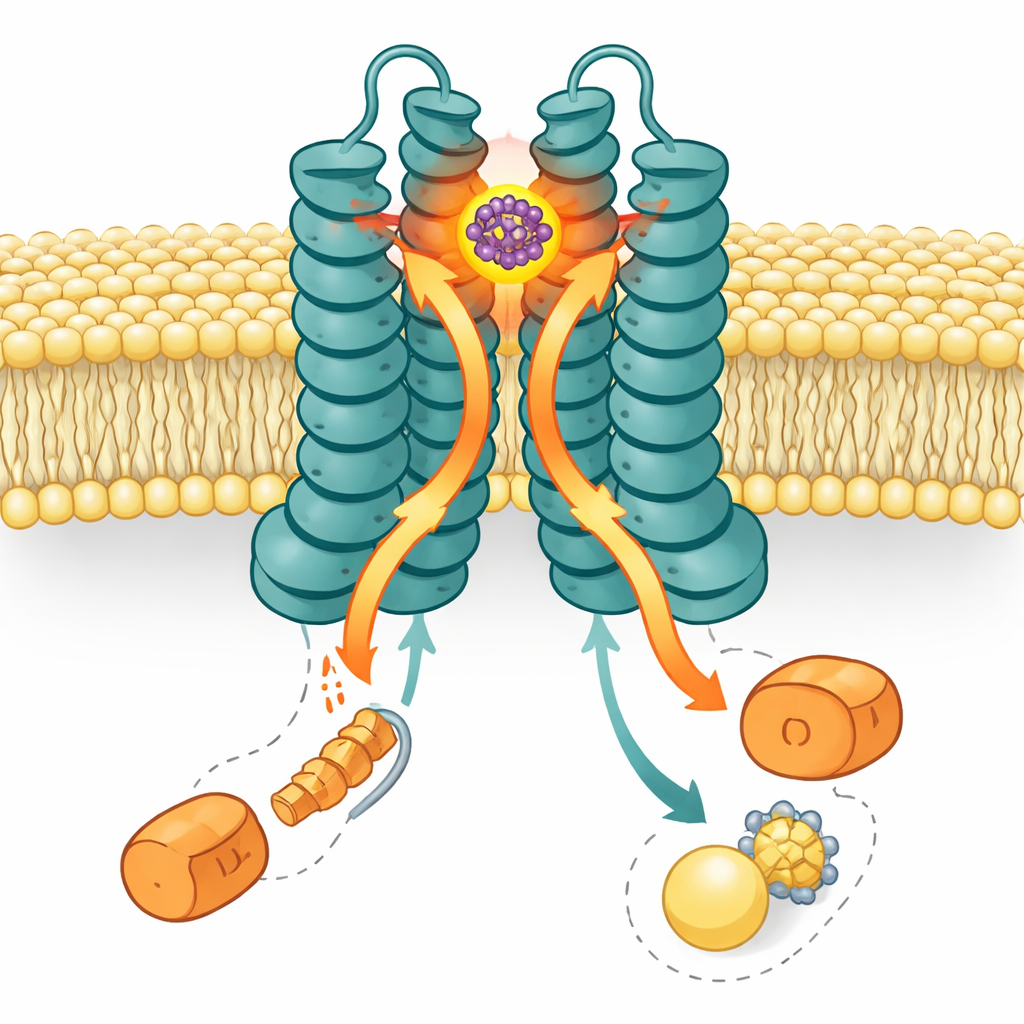
Почему одни бактерии поражаются, а другие остаются невредимы
SMT-738 обладает желательным свойством: он сильно действует на лекарственно-устойчивые Enterobacteriaceae, но оставляет многие другие граммотрицательные виды в кишечнике по большей части нетронутыми. Чтобы понять эту селективность, команда сравнила последовательности LolE у восприимчивых и резистентных бактерий и сосредоточилась на позициях, контактирующих с SMT-738. Два остатка в LolE, особенно соответствующий положению D264 в E. coli, выделялись. У чувствительных патогенов эти позиции совпадали с версией, контактирующей с препаратом в E. coli, тогда как у многих резистентных кишечных комменсалов они были заменены другими аминокислотами. Когда исследователи сконструировали E. coli с такими заменами, бактерии стали сильно резистентными к SMT-738 при условии сохранной экспрессии LolCDE. Моделирования предположили, что эти изменения меняют локальную гибкость вокруг кармана, уменьшая способность SMT-738 туда войти. Интересно, что другой ингибитор LolCDE, лоламицин, опирался на частично пересекающиеся контактные точки и проявлял другую картину резистентности, указывая на различные способы нацеливания одного и того же насоса.
Новые чертежи для будущих антибиотиков
Комбинируя структурную визуализацию, сканы мутаций, биохимические тесты и компьютерные симуляции, работа показывает, что SMT-738 — это не просто пробка в канале. Препарат сцепляется с периплазматической стороной насоса LolCDE, блокирует сайт входа липопротеина и затем запускает дальнодействующие сдвиги, которые отрывают одну из двух моторных единиц, замораживая транспортер в нерабочем состоянии. Этот механизм «аллостерической блокировки» представляет собой новый способ выведения из строя бактериальной машины и помогает объяснить, почему SMT-738 может нацеливаться на опасные патогены, щадя при этом большую часть микробиоты. Детальная карта кармана связывания и ключевого селективного остатка в LolE теперь предлагают рациональную основу для разработки антибиотиков следующего поколения, эксплуатирующих ту же уязвимость с ещё большей мощностью и точностью.
Цитирование: Li, H., Zhu, X., Zhang, D. et al. Molecular mechanism of action of small molecule SMT-738 on bacterial lipoprotein transporter LolCDE. Nat Commun 17, 2540 (2026). https://doi.org/10.1038/s41467-026-69411-2
Ключевые слова: устойчивость к антибиотикам, граммотрицательные бактерии, транспорт липопротеинов, ингибитор LolCDE, структура крио-ЭМ