Clear Sky Science · ru
Лактат, происходящий от макрофагов, стимулирует фенотипическое ремоделирование дермальных фибробластов кожи через MCT1-опосредованную лактилцию лизина 23 гистона H3 в гипертрофическом рубце
Почему некоторые рубцы становятся толстыми и приподнятыми
Большинство порезов и ожогов со временем перерастают в тонкие, плоские рубцы. Но некоторые раны заживают с толстыми, выпуклыми полосами ткани — гипертрофическими рубцами, которые могут вызывать зуд, боль и ограничивать подвижность. В этом исследовании выявлен неожиданный фактор таких упорных рубцов: распространённый метаболический побочный продукт — лактат, вырабатываемый иммунными клетками в жёсткой заживающей коже, который перепрограммирует соседние клетки ремонта, заставляя их вести себя более агрессивно и способствовать образованию рубца.
От нормального восстановления к проблемному рубцу
При здоровом заживлении ран клетки кожи работают совместно, чтобы закрыть повреждение и восстановить ткань. Фибробласты, основные клетки восстановления в глубоком слое кожи, временно переходят в усиленное состояние, в котором они синтезируют коллаген — белковый каркас кожи. После закрытия раны эти клетки снова затихают. Однако при гипертрофических рубцах фибробласты застревают в этом сверхактивном состоянии и откладывают слишком много коллагена в толстых, неорганизованных пучках. Авторы начали с сопоставления нормальной кожи и ткани гипертрофического рубца и обнаружили явный метаболический сдвиг: в среде рубца доминирует быстрый сахарный метаболизм, который генерирует большие количества лактата, а также высокий уровень транспортного белка MCT1, переносящего лактат внутрь клеток. 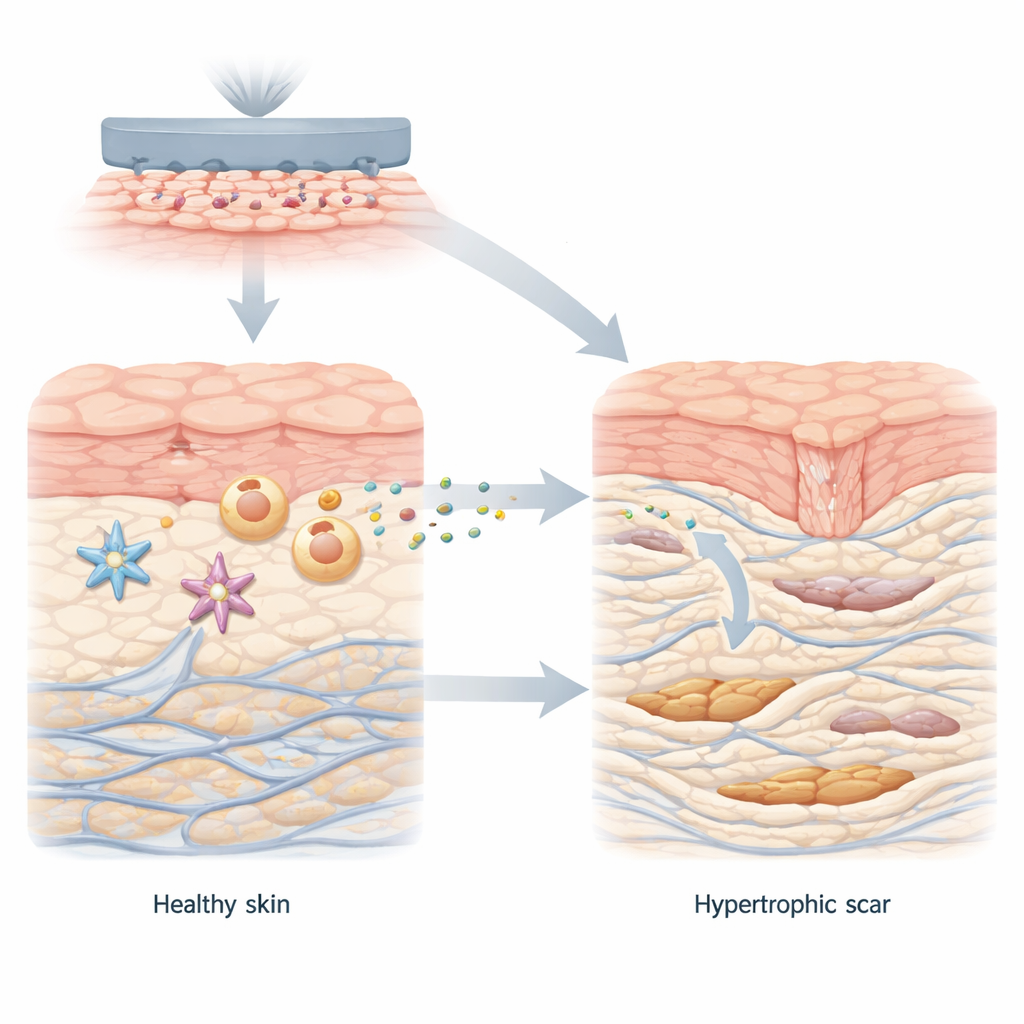
Иммунные клетки как неожиданные фабрики лактата
Чтобы выяснить, откуда берётся весь этот лактат, команда исследовала разные типы клеток из человеческой кожи и мышиных моделей: макрофаги (иммунные клетки, убирающие мусор и координирующие заживление), клетки кровеносных сосудов и фибробласты. Их выращивали на мягких или жёстких субстратах, имитирующих нормальную и рубцовую кожу. На жёстких поверхностях только макрофаги переключались в высокогликолитический, «сахаро‑жадный» режим и выбрасывали большие количества лактата — как в лабораторных культурах, так и в реальной ткани рубца. При удалении макрофагов из заживающих ран мышей уровень лактата в ткани снижался, а образование рубца уменьшалось. Эти результаты указывают на макрофаги, особенно те, которые ощущают жёсткую среду, как на главные фабрики лактата, формирующие микроокружение рубца.
Лактат как сигнал, перенастраивающий фибробласты
Дальше исследователи спросили, как этот избыток лактата влияет на фибробласты. Когда фибробласты купали в лактатно‑богатом кондиционированном средовом растворе от макрофагов, выращенных на жёстких субстратах, они быстрее размножались, активнее мигрировали и вырабатывали больше коллагена — все эти признаки соответствуют агрессивному состоянию миофибробластов. Блокирование транспортёра MCT1 на фибробластах или снижение производства лактата в макрофагах резко уменьшало эти изменения. Внутри фибробластов поступающий лактат делал не только вклад в энергообеспечение: он вызывал специфическую химическую метку на гистонах — белках, упаковывающих ДНК в ядре клетки. Эта метка, называемая H3K23 лактилцией, была значительно выше в фибробластах, формирующих рубец, чем в нормальных, и действовала как переключатель, включающий два ключевых гена — HEY2 и COL11A1, которые вместе усиливают рубцовое программирование.
Самоподдерживающаяся петля рубцевания
Белки, активируемые этой гистоновой меткой, образуют мощную обратную связь. HEY2 усиливает активность пути с участием YAP1 и SMAD2, который известен тем, что направляет фибробласты к более контрактильному, коллагенопродуцирующему состоянию. COL11A1, структурный белок, связанный с коллагеном, физически взаимодействует с транспортёром MCT1 на фибробластах, помогая стабилизировать его и повышая эффективность захвата лактата. Иными словами, вхождение лактата в клетку меняет регуляцию генов так, что это ещё больше усиливает поступление лактата и синтез коллагена, запирая фибробласты в про‑рубцовой идентичности. 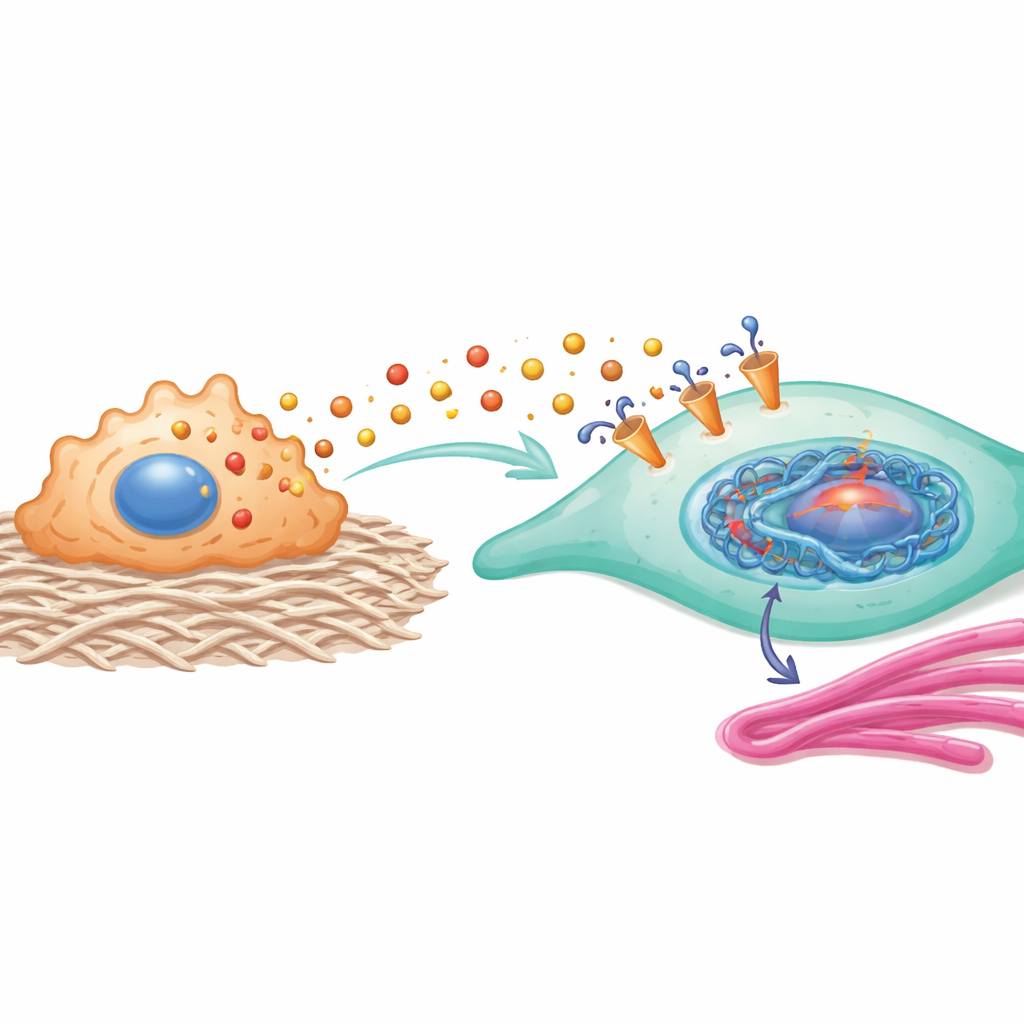
Ослабление петли для улучшения заживления
Чтобы проверить, можно ли улучшить заживление, прерывая эту петлю, команда использовала мышей, у которых MCT1 можно было селективно удалить из фибробластов, а также препарат, блокирующий MCT1. В обоих вариантах раны заживали быстрее, вновь образованная кожа выглядела более организованной, а волокна коллагена были тоньше и лучше выровнены, с меньшим количеством признаков гипертрофического рубцевания. Конкретная гистоновая метка и её целевые гены также снижались. Истощение макрофагов — основного источника лактата — или химическое снижение уровня лактата давало аналогичный антирубцовый эффект. Эти эксперименты показывают, что цепочка «жёсткая рана–макрофаг–лактат–фибробласт» — это не просто корреляция, а ключевой драйвер патологического рубцевания.
Что это значит для будущих методов лечения рубцов
Эта работа переставляет лактат из разряда простого метаболического «мусора» в ранг мощного мессенджера, связывающего механические воздействия, метаболизм и регуляцию генов при заживлении ран. Показав, как лактат, происходящий от макрофагов и транспортируемый через MCT1, меняет гистоны и запускает самоподдерживающуюся программу рубцевания в фибробластах, исследование выделяет несколько перспективных терапевтических мишеней. Препараты, которые модулируют производство лактата, блокируют MCT1 или вмешиваются в специфическую гистоновую модификацию, могут однажды помочь ранам заживать быстрее и образовывать более плоские, менее заметные рубцы.
Цитирование: Yuan, Y., Xiao, Y., Zou, J. et al. Lactate derived from macrophages drives skin dermal fibroblasts phenotypic remodeling via MCT1-primed histone H3 lysine 23 lactylation in hypertrophic scar. Nat Commun 17, 2694 (2026). https://doi.org/10.1038/s41467-026-69388-y
Ключевые слова: гипертрофический рубец, сигнализация лактата, взаимодействие макрофаг–фибробласт, лактилирование гистонов, терапия заживления ран