Clear Sky Science · ru
Миоферлин — компонент везикул поздней стадии транспорта вРНП для оболочечных РНК-вирусов
Почему это важно для повседневного здоровья
Сезонный грипп и другие респираторные инфекции могут казаться рутиной, но вместе они ежегодно убивают миллионы людей во всем мире. Многие из этих вирусов, включая вирус гриппа A и респираторно-синцитиальный вирус (RSV), уже ускользают от вакцин и противовирусных препаратов за счет быстрого накопления мутаций. В этом исследовании внимание смещено на то, что вирусы изменить не в состоянии: молекулярный аппарат человеческой клетки, который они захватывают, чтобы покинуть инфицированную клетку. Выявив общую уязвимость в этом аппарате, работа указывает путь к препаратам, которые могли бы одновременно ослабить широкий спектр респираторных вирусов.
Клеточный путь доставки, который используют вирусы
Эпителиальные клетки дыхательных путей постоянно перерабатывают фрагменты своей наружной мембраны в процессе, называемом рециркуляцией. Небольшие мембранные пузырьки, или везикулы, переносят грузы изнутри клетки обратно на поверхность, управляемые семейством белков, известных совместно как Rab11. Вирус гриппа A, RSV и родственный им вирус Сендай используют этот маршрут на поздних этапах инфекции. Они загружают свой генетический материал, упакованный в рибонуклеопротеиновые комплексы, на везикулы, содержащие Rab11, которые доставляют их на апикальную (обращенную к воздуху) сторону клетки, где образуются и отщепляются новые вирусные частицы. До сих пор Rab11 был единственным фактором хозяина, ясно общим для этих транспортных везикул, что оставляло значительный пробел в понимании их формирования и функционирования.
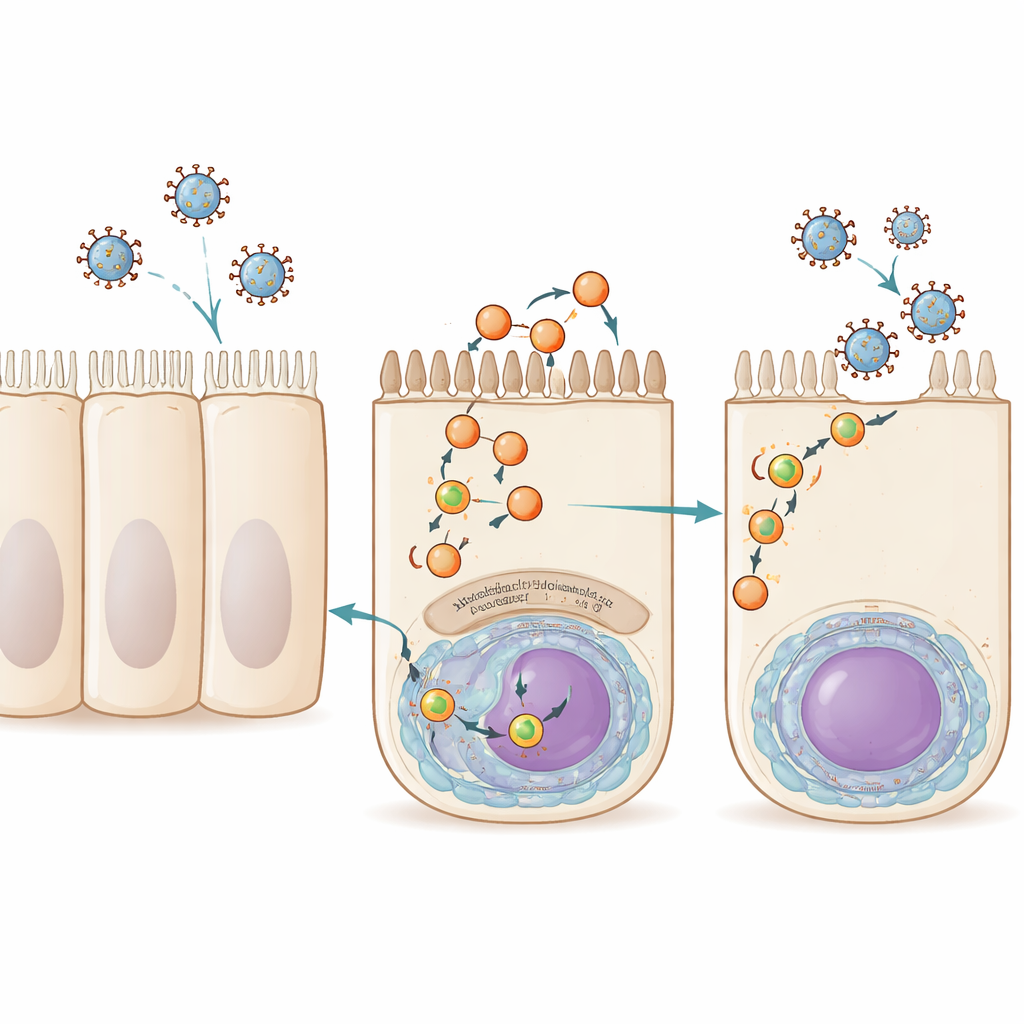
Поиск нового участника: миоферлин
Исследователи начали с вопроса, какие человеческие белки физически ассоциируют с аппаратом упаковки генома гриппа в разные моменты инфекции. Они модифицировали вирус гриппа A так, чтобы его полимераза несла молекулярную метку, а затем с помощью масс-спектрометрии каталогизировали человеческие белки, связанные с этим комплексом на ранних и поздних стадиях инфекции. Среди сотен кандидатов на поздних временных точках выделился один: миоферлин, крупный мембраноассоциированный белок, ранее связанный с развитием мышц, эндоцитозом и восстановлением мембран. Когда команда снизила уровни миоферлина в клетках легочного происхождения с помощью малых интерферирующих РНК или блокировала его малой молекулой-ингибитором, клетки по-прежнему синтезировали вирусную РНК и белки в нормальном объеме, но выделяли значительно меньше инфекционных частиц гриппа. Это указывало на то, что миоферлин не обязателен для копирования вирусного генома, но крайне важен на поздних этапах, когда новые вирусы собираются и покидают клетку.
Миоферлин сопровождает вирусный груз
Высокоточное микроскопирование показало, где располагается миоферлин во время инфекции. В неинфицированных клетках миоферлин в основном совпадает по расположению с Rab11-положительными рециркуляционными везикулами как вблизи ядра, так и в направлении края клетки, и потеря любого из этих белков нарушает нормальное распределение другого. Во время инфекции гриппом сеть Rab11 заметно перестраивается в увеличенные, неправильной формы везикулы, которые несут рибонуклеопротеиновые комплексы вируса. Миоферлин сохраняется в этих перестроенных везикулах и сильно ко-локализуется с вирусным геномом и Rab11. Когда команда использовала препарат, заставлявший вирусные геномные комплексы и их транспортные везикулы слипаться в агрегаты, миоферлин оказался втянут в те же агрегаты, что подтверждает: он является встроенным компонентом этих структур поздней стадии транспорта, а не просто случайно находящимся поблизости белком.
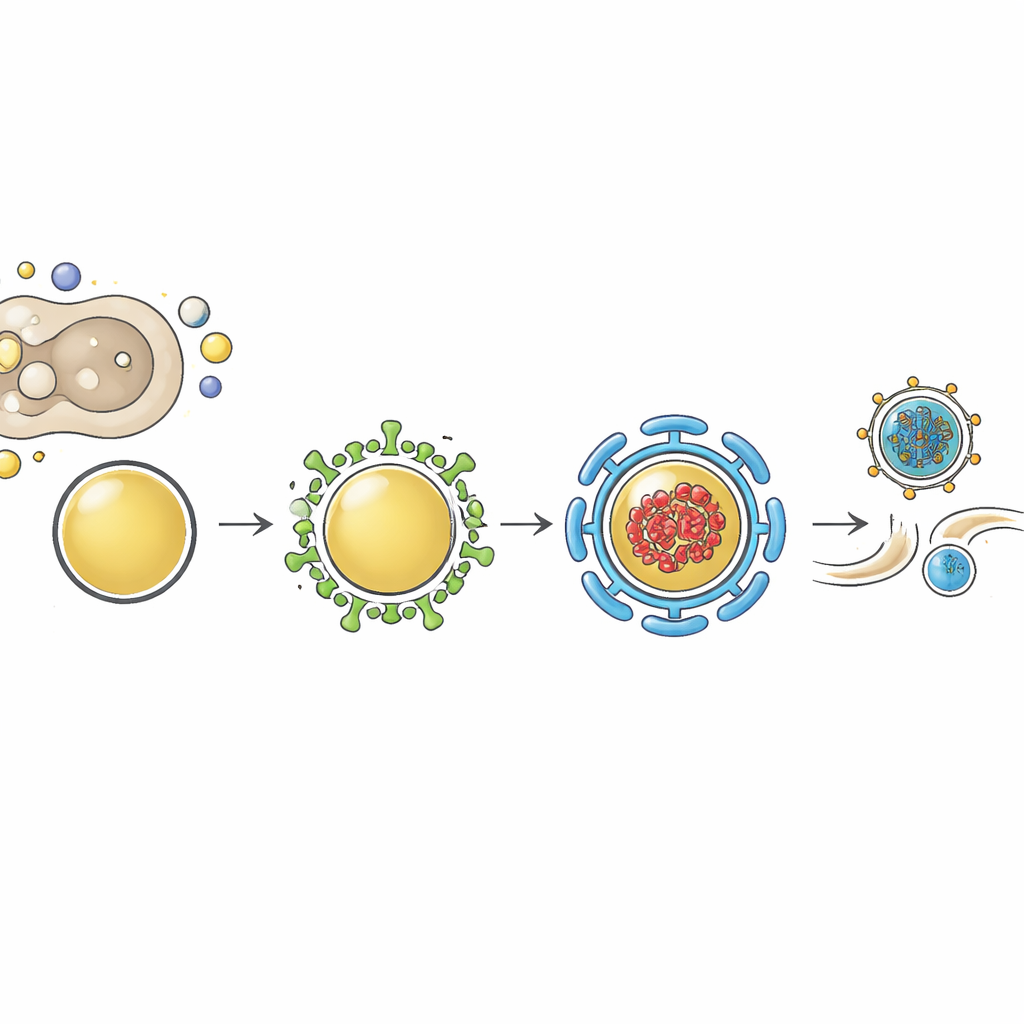
Общий узел для нескольких респираторных вирусов
Далее исследование проверило, уникальна ли эта зависимость от миоферлина для гриппа или же она более широко распространена. Понижение экспрессии миоферлина в легочных клетках, инфицированных RSV или вирусом Сендай, вновь привело к резкому снижению выпуска инфекционных вирусов, не снижая при этом уровней вирусной РНК. Съемка одиночных молекул показала, что геномы обоих вирусов собираются вместе с миоферлином и Rab11 в цитоплазматических точках, которые, вероятно, представляют собой транспортные узлы, а не фабрики репликации. Эта картина поддерживает единый взгляд: разные оболочечные респираторные РНК-вирусы, несмотря на различия в образе жизни, сходятся на той же системе везикул Rab11–миоферлин, когда приходит время переместить завершенные геномы к поверхности клетки для упаковки и выхода.
Как миоферлин формирует везикулы, несущие вирус
Миоферлин построен из нескольких доменов типа «C2», которые способны связываться с мембранами и партнёрными белками. Предыдущие работы показали, что один из этих доменов взаимодействует с семейством белков, реконфигурирующих мембраны, называемых EHD. В этом исследовании флуоресцентно меченые EHD1 и EHD2 были обнаружены в тех же перестроенных везикулах, которые переносят геномы гриппа и Rab11, особенно когда эти везикулы были экспериментально агрегированы. Снижение уровня EHD2, как и снижение миоферлина, уменьшало выход гриппа без влияния на репликацию генома. Более того, удаление миоферлина приводило к падению уровня белка EHD2, что свидетельствует о том, что миоферлин помогает стабилизировать или правильно позиционировать EHD2 на мембранах. Авторы предлагают, что миоферлин располагается на Rab11-положительных везикулах и привлекает белки EHD для формовки их мембран, завершая образование специализированных «везикул с неправильным покрытием», оптимизированных для транспорта вирусного груза к местам отпочковывания.
Что это означает для будущих антивирусных стратегий
В совокупности эти результаты выдвигают миоферлин в центральный организующий элемент пути рециркуляции хозяина, от которого в критический поздний этап зависят многие оболочечные респираторные вирусы. Поскольку нацеливание только на вирусные белки часто ведет к быстрому возникновению резистентности, факторы хозяина, используемые множеством вирусов, представляют собой привлекательные мишени для лекарств. Вмешательство в функцию миоферлина или в его взаимодействие с Rab11 и белками EHD теоретически могло бы замедлить или блокировать распространение различных патогенов — от гриппа и RSV до других Rab11-зависимых вирусов, например некоторых коронавирусов. Для превращения этой идеи в безопасную терапию предстоит еще много работы, но исследование предоставляет детальную карту общего пути ухода вирусов и выделяет миоферлин как перспективную «узкую» точку на этом пути.
Цитирование: Bonazza, S., Turkington, H.L., Sukumar, S. et al. Myoferlin is a component of late-stage vRNP trafficking vesicles for enveloped RNA viruses. Nat Commun 17, 2507 (2026). https://doi.org/10.1038/s41467-026-69386-0
Ключевые слова: грипп, респираторные вирусы, везикулярный транспорт, факторы хозяина, миоферлин