Clear Sky Science · ru
Инженерные экзосомные нановезикулы для доставки антител при лечении воспалительного заболевания кишечника
Новая надежда при упорном заболевании кишечника
Воспалительное заболевание кишечника (ВЗК) может превратить повседневную жизнь в постоянную борьбу с болью, диареей и усталостью, а также увеличивает долгосрочный риск развития рака толстой кишки. Многие существующие препараты подавляют обострения, но не устраняют коренные нарушения иммунного ответа, поэтому симптомы часто возвращаются. В этом исследовании представлен хитро сконструированный «умный» наночастичный препарат, который путешествует по кровотоку, находит воспалённые участки кишечника и доставляет комбинированную двухкомпонентную терапию, предназначенную как для подавления вредного воспаления, так и для восстановления долговременного иммунного равновесия.
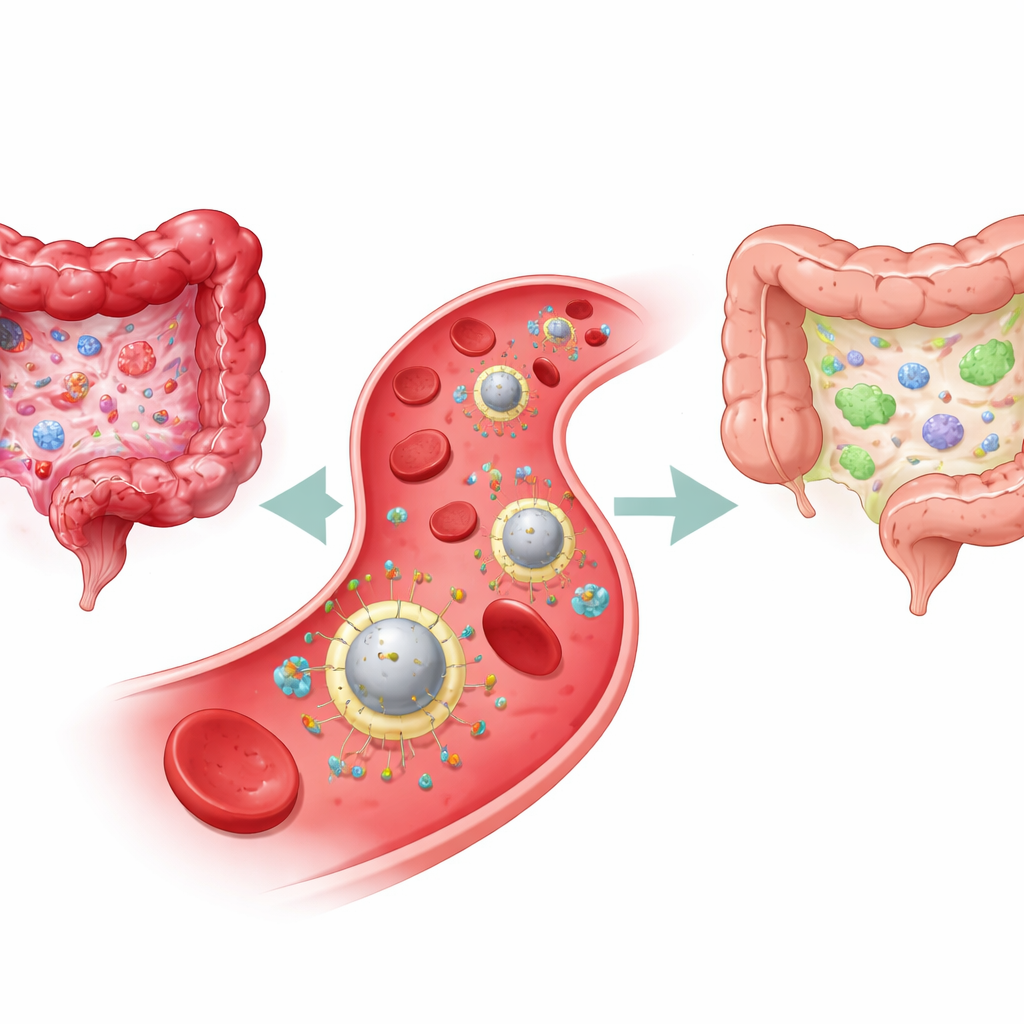
Почему текущие методы лечения недостаточны
ВЗК, в которую входят болезнь Крона и язвенный колит, возникает из-за хронической борьбы в иммунной системе кишечника. С одной стороны — агрессивные иммунные клетки и воспалительные молекулы, разрушающие слизистую оболочку кишечника; с другой — регуляторные клетки, которые обычно сдерживают эту реакцию. Стандартная терапия — стероиды, иммуносупрессанты и биологические препараты — в основном пытаются притупить воспаление по всему организму. Они могут облегчить симптомы, но часто мало способствуют восстановлению базового иммунного баланса, а широкое подавление иммунитета повышает риск инфекций. Даже более новые антитела, блокирующие ключевой воспалительный сигнал интерлейкин‑23 (IL‑23), помогают лишь части пациентов и всё равно циркулируют по всему организму, а не только в очагах поражения.
Создание нацеленного, меняющегося лекарства
Исследователи поставили цель разработать препарат, который вел бы себя скорее как живая клетка, чем как простое лекарство. Они начали с крошечных пузырьков, естественно выделяемых регуляторными Т‑клетками — иммунными клетками, способствующими толерантности и поддержанию порядка. Эти пузырьки, называемые экзосомами, переносят белки и генетический материал, которые могут подтолкнуть другие иммунные клетки к спокойному состоянию. Команда слила эти экзосомы с фрагментами мембраны тромбоцитов, заимствуя у тромбоцитов способность прилипать к повреждённым сосудам в воспалённой ткани. На поверхность этой гибридной оболочки прикрепили антитела, блокирующие IL‑23, с помощью молекулярной «струны», которую могут разрезать ферменты (матричные металлопротеиназы), обильные только в воспалённой ткани кишечника. Результат, названный PrEXO‑a23, — нановезикула, которая циркулирует в крови, прикрепляется к повреждённым сосудам кишечника и сбрасывает антительные молекулы только там, где активна болезнь.
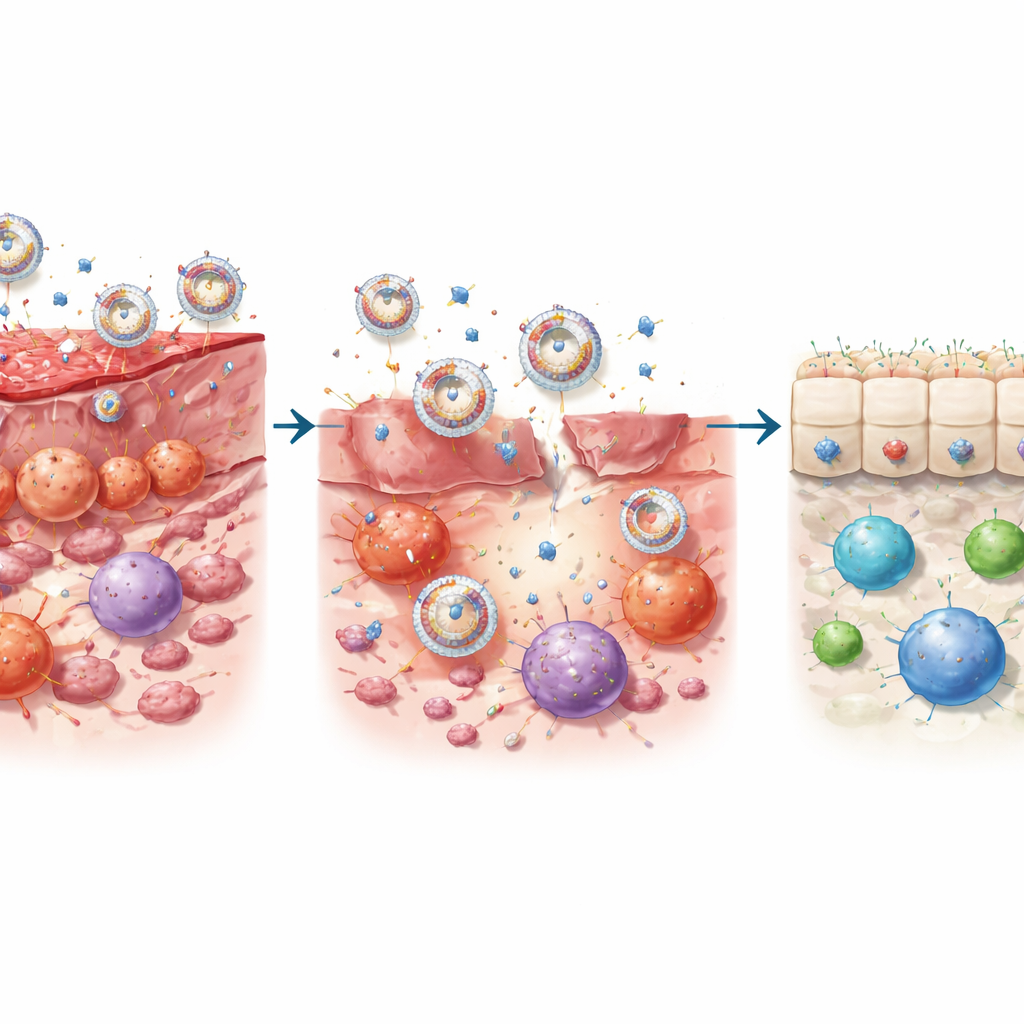
Перевоспитание иммунной среды кишечника
В клеточных исследованиях PrEXO‑a23 превзошёл по эффективности либо антитела, либо экзосомы по отдельности. Он значительно снижал образование воспалительных Т‑хелперов 17 (Th17) и выделение повреждающих цитокинов, разрушающих слизистую кишечника, одновременно защищая эпителиальные клетки кишечника человека от гибели. В то же время он переводил дендритные клетки — «ворота», обучающие Т‑клетки — из агрессивного, активирующего состояния в «толерантное», способствующее росту регуляторных Т‑клеток. В мышиных моделях колита нановезикулы эффективно направлялись в воспалённую ткань толстой кишки, захватывались различными типами иммунных клеток и высвобождали антитела в ответ на местную ферментную активность. Это двойное действие — блокирование воспаления, управляемого IL‑23, и усиление сигналов, способствующих толерантности — вернуло маркеры воспаления близко к норме и восстановило более здоровый баланс типов Т‑клеток.
Ремонт тканей и предотвращение долгосрочного ущерба
Мыши с химически индуцированным колитом, получавшие PrEXO‑a23, теряли меньше веса, имели более длинную и здоровую толстую кишку и реже показывали увеличение селезёнки — признак системного воспаления. Микроскопическое исследование выявило сохранённую архитектуру кишечника и более плотные контакты между эпителиальными клетками, что указывает на восстановленный барьер. Лечение также помогало восстановить баланс кишечной микробиоты, увеличивая семейства, связанные со здоровьем кишечника, и сокращая те, что ассоциируются с болезнью. В более тяжёлой модели, имитирующей переход от хронического колита к раку толстой кишки, PrEXO‑a23 не только ослаблял текущее воспаление, но и полностью предотвращал развитие опухолей и сдерживал утолщение и рубцевание стенки кишечника, характерные для фиброза. Молекулярные анализы указывали на восстановление защитной сигнализации p53 — ключевого «стража» против рака — что оказалось важным для противоракового эффекта.
К более умному, долговременному уходу при ВЗК
Для неспециалиста ключевая мысль такова: это исследование выходит за рамки простого «приглушения» воспаления. Объединив целевую доставку, локальный сброс антител и иммунно‑успокаивающий груз экзосом в одном крошечном пакете, PrEXO‑a23 одновременно успокаивает активную болезнь и помогает перенастроить иммунную систему на длительную толерантность. У мышей это привело не только к облегчению симптомов, но и к защите от рубцевания и рака толстой кишки — двух самых опасных осложнений хронического ВЗК. Хотя требуется ещё много испытаний, прежде чем такая терапия сможет дойти до пациентов, исследование демонстрирует, как биологически вдохновлённые наномедицины могут однажды предложить более точный и длительный контроль над сложными иммунными расстройствами, такими как ВЗК.
Цитирование: Cao, J., Luo, R., Miao, R. et al. Engineered exosome nanovesicles for delivery of antibodies to treat inflammatory bowel disease. Nat Commun 17, 2737 (2026). https://doi.org/10.1038/s41467-026-69382-4
Ключевые слова: воспалительное заболевание кишечника, наномедицина, иммунная толерантность, экзосомы, профилактика колоректального рака