Clear Sky Science · ru
Структурные дефекты в фибриллах амилоида-β запускают вторичную нуклеацию
Почему микроскопические дефекты в белках мозга имеют значение
При болезни Альцгеймера и родственных патологиях отдельные белки скапливаются в длинные нитевидные структуры, называемые амилоидными фибриллами. Эти фибриллы не только служат маркером болезни; они также способствуют образованию новых, сильно токсичных белковых частиц, способных повреждать нервные клетки. В этом исследовании поставлен простой, но важный вопрос: являются ли редкие структурные «дефекты» внутри амилоидных фибрилл основными очагами, где зарождается новое вредоносное образование? Ответ может указать на новые способы замедлить или остановить развитие болезни, воздействуя лишь на несколько критических участков, а не на всю поверхность белка. 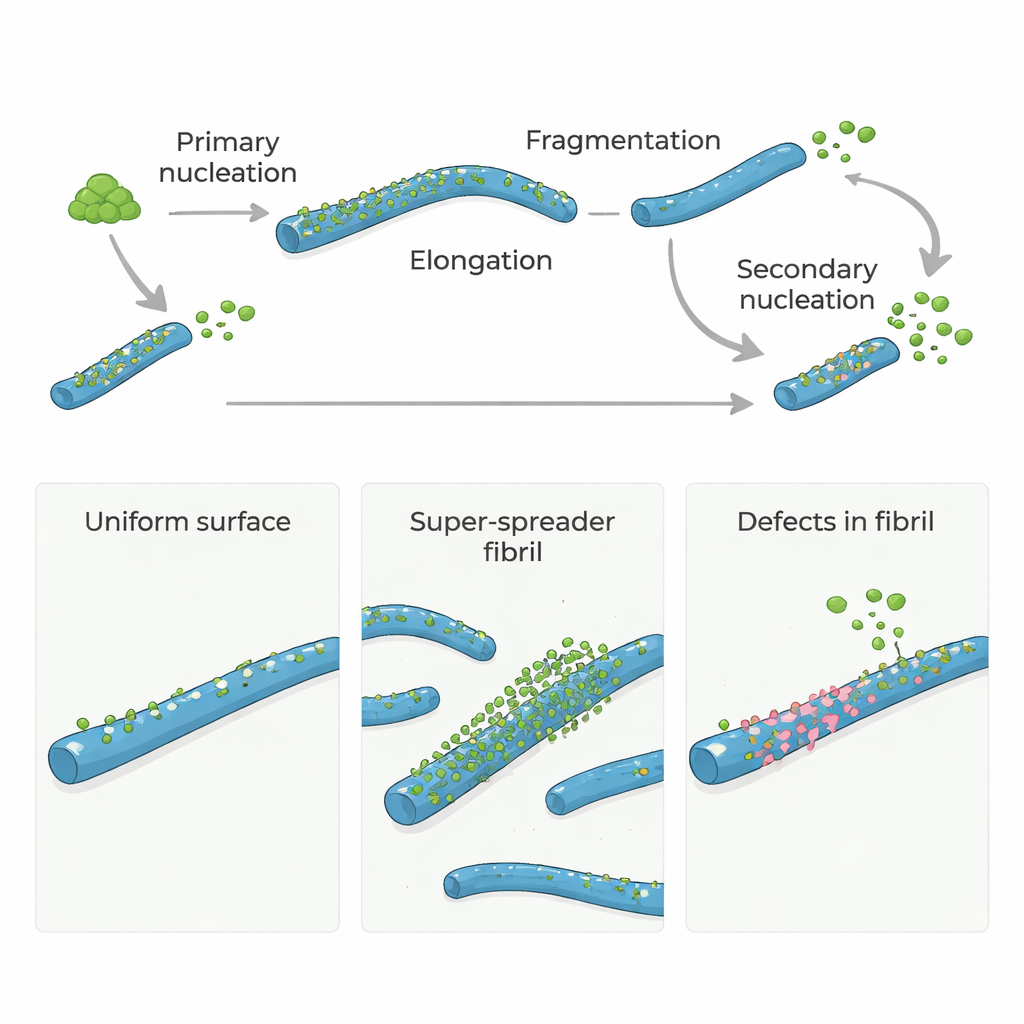
От спокойного белка к неконтролируемой цепной реакции
Белки амилоида-β (Aβ), центральные для болезни Альцгеймера, сами по себе обычно не образуют агрегации очень быстро. Для старта требуется, чтобы несколько мономеров медленно собрались в первые маленькие фибриллы — шаг, называемый первичной нуклеацией. Как только такие начальные фибриллы появились, они быстро растут за счёт присоединения мономеров к концам. И ещё важнее то, что существующие фибриллы могут вызывать появление новых фибрилл на своей поверхности в процессе, известном как вторичная нуклеация. Этот поверхностно-управляемый этап способен заполнить систему новыми фибриллами и малыми токсичными олигомерами, превратив медленную проблему в неконтролируемую цепную реакцию.
Все ли поверхности фибрилл одинаково опасны?
Во многих моделях предполагалось, что вся поверхность амилоидной фибриллы одинаково хороша в катализе вторичной нуклеации. Однако недавние эксперименты намекали, что активна лишь небольшая часть поверхности. Чтобы проверить это, авторы использовали природный молекулярный «шаперон» Brichos, известный тем, что блокирует вторичную нуклеацию Aβ40 и Aβ42 (двух ключевых форм амилоида-β). Тщательно измерив, сколько меченого флуоресцентно Brichos связывается с фибриллами, они обнаружили, что он связывается плотно, но в очень малом количестве: примерно один молекула Brichos на каждые 100–150 молекул Aβ в фибрилле. При этом такое редкое покрытие было достаточно, чтобы подавить более 90% вторичной нуклеации, что означает: именно редкие локализованные участки — а не вся поверхность — доминируют в образовании новых токсичных сборок.
Исследование роли скрытых дефектов
Эти результаты навели на мысль, что ключевые сайты нуклеации могут быть структурными дефектами — небольшими неправильностями, возникающими по мере роста фибрилл, такими как смещённые слои или частично оголённые внутренние ядра. Чтобы проверить эту идею непосредственно, исследователи вырастили фибриллы Aβ40 в двух разных условиях. Один набор, «контрольные» фибриллы, формировали в типичных, сильно пересыщенных условиях, которые благоприятствуют быстрому росту и кинетическому захвату дефектов. Другой набор создавали с помощью медленной протоколированной отжиговой анаилизации: фибриллы формировали при очень низом эффективном движущем факторе, близком к их пределу растворимости, где неправильные структуры могут растворяться или ремонтироваться прежде, чем зафиксируются. Рентгенокриоэлектронная микроскопия высокого разрешения показала, что оба набора фибрилл по форме и скрутке в целом выглядят практически одинаково, что указывает на то, что процесс отжига не изменил базальную морфологию. 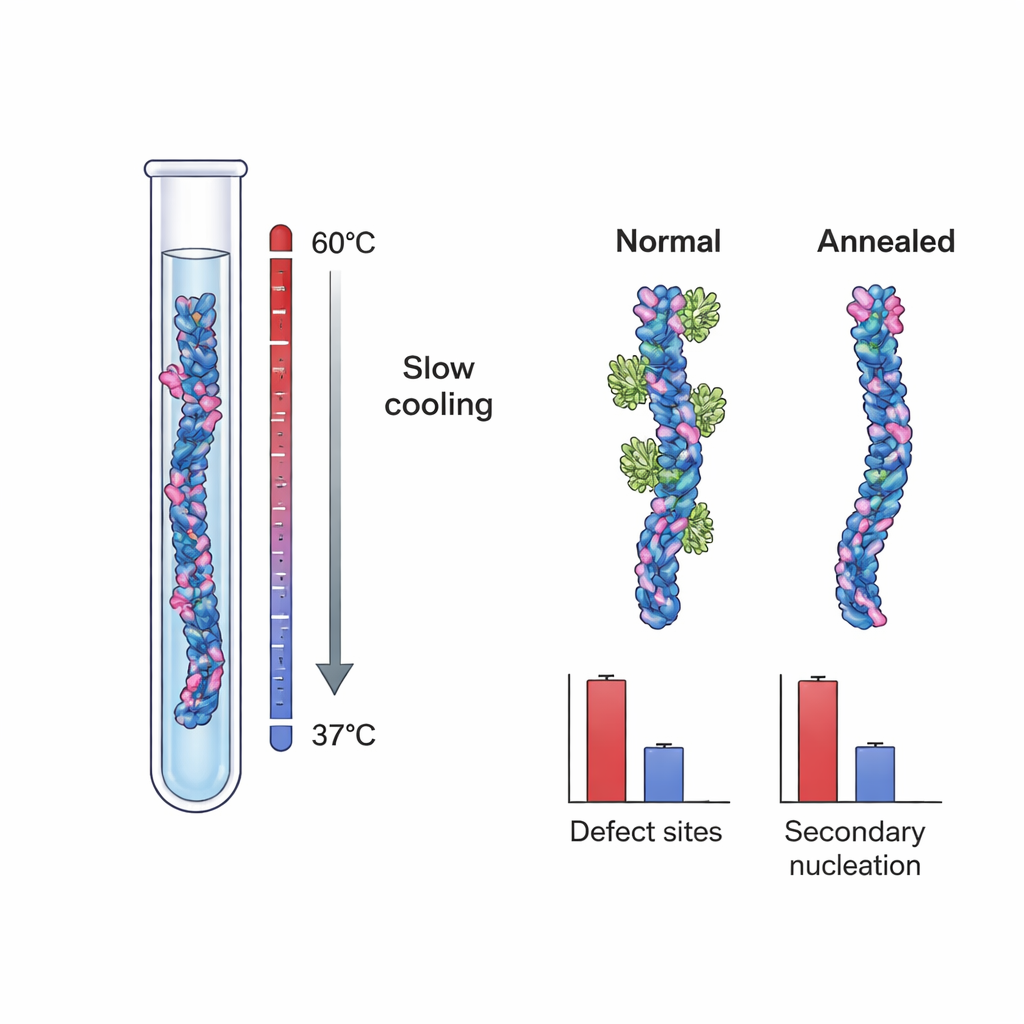
Меньше дефектов — меньше опасных участков роста
При измерении связывания Brichos с этими двумя типами фибрилл команда обнаружила поразительную разницу. Контрольные Aβ40-фибриллы имели примерно один сайт связывания Brichos на ~100 мономеров, снова указывая на редкие, но важные участки. Однако у отожжённых фибрилл было лишь около одного сайта на ~800 мономеров — почти 90% сокращение частоты сайтов. В отдельных тестах, где эти фибриллы добавляли в виде «затравок» в свежие растворы Aβ40, отожжённые фибриллы оказались значительно менее эффективными в инициировании новой агрегации, даже при равной общей массе фибрилл. Детальная кинетическая модель показала, что это падение силы затравки нельзя объяснить просто различиями в длине фибрилл. Вместо этого оно количественно согласуется с уменьшенным числом сайтов связывания Brichos, что сильно поддерживает идею о том, что дефекты роста действуют как основные двигатели вторичной нуклеации.
Общий принцип с терапевтическим потенциалом
Комбинируя термодинамические доводы, переанализ ранее опубликованных работ и сравнения между несколькими амилоидообразующими белками, авторы утверждают, что редкие дефекты роста, вероятно, имеют центральное значение для вторичной нуклеации во многих системах, а не только в случае Aβ, связанного с Альцгеймером. Эти дефекты частично оголяют плотно упакованное внутреннее ядро фибриллы, предлагая готовый каркас, на котором новые олигомеры и фибриллы могут формироваться гораздо легче, чем на гладкой поверхности. Признание дефектов ключевыми виновниками открывает новые направления в разработке лекарств. Вместо попыток блокировать все возможные взаимодействия на поверхности фибриллы, терапия могла бы быть направлена на прикрытие или ремонт лишь этих редких дефектных участков или на снижение условий их образования в первую очередь. На практике это может означать снижение эффективной концентрации амилоидообразующих белков в мозге или разработку молекул, вдохновлённых Brichos, которые распознают и нейтрализуют очаги нуклеации, вызванные дефектами. В случае успеха такие стратегии могли бы перекрыть основной источник токсичных олигомеров и замедлить прогрессирование заболеваний, связанных с амилоидом.
Цитирование: Hu, J., Scheidt, T., Thacker, D. et al. Structural defects in amyloid-β fibrils drive secondary nucleation. Nat Commun 17, 1933 (2026). https://doi.org/10.1038/s41467-026-69377-1
Ключевые слова: амилоидные фибриллы, болезнь Альцгеймера, вторичная нуклеация, агрегация белков, шаперон Brichos