Clear Sky Science · ru
Истощение кислорода в биомолекулярных конденсатах определяется плотностью макромолекул
Невидимые карманы внутри живых клеток
Внутри наших клеток многие химические реакции зависят от постоянного поступления кислорода. Но клетки — это не простые мешки с жидкостью: они содержат крошечные каплеобразные отделы, называемые биомолекулярными конденсатами, которые формируются без мембран. В этом исследовании задают обманчиво простой вопрос с большими последствиями: меняют ли эти капли доступность кислорода в разных частях клетки и, если да, почему? Ответ оспаривает устоявшиеся представления о поведении малых молекул в таких плотно заполненных микроокружениях.

Капли без стенок
Биомолекулярные конденсаты — это мягкие, похожие на жидкость скопления белков и нуклеиновых кислот, которые собираются и растворяются по требованию. Они помогают организовать биохимию, концентрируя одни молекулы и вытесняя другие, хотя у них нет окружающей мембраны. Предыдущие работы показали, что многие мелкие метаболиты и лекароподобные соединения проникают в эти капли, обычно потому, что их внутренняя среда по свойствам ближе к «масляному» растворителю по сравнению с водянистой клеточной жидкостью. Кислород же — особый случай: это маленькая газообразная молекула, питающая дыхание, но также запускающая вредные побочные реакции. То, обогащают ли конденсаты кислород или истощают его, может влиять на эффективность работы ферментов и на уровень окислительного повреждения рядом с этими каплями или внутри них.
Измерение кислорода в крошечных отсеках
Чтобы исследовать уровни кислорода внутри конденсатов, учёные создали простую, но настраиваемую модельную систему с искусственно спроектированными гибкими белками, которые легко формируют капли в солевом растворе. Сначала они получили крупные макроскопические фазы, центрифугируя образцы, а затем вводили тончайшие электрохимические микроэлектроды, чтобы напрямую считывать концентрации кислорода через границу между богатым белком и бедным белком слоями. Эти измерения показали, что уровень кислорода падает, когда зонд входит в белокоплотную фазу: капли частично вытесняют кислород, а не насыщаются им.
Освещение кислорода специальными красителями
Поскольку электроды нарушают маленькие капли, команда перешла к фосфоресцентной микроскопии времени жизни свечения — оптическому методу, использующему специальные красители, чьё свечение длится короче при большей концентрации кислорода. Отслеживая время свечения внутри и снаружи отдельных капель и тщательно корректируя влияние среды капли на базовое поведение красителя, они смогли вывести концентрации кислорода без физического вмешательства в конденсаты. В оптических данных, собранных при разных условиях, подтвердились результаты электродных измерений: кислород стабильно ниже внутри конденсатов, чем в окружающем растворе. Компьютерные симуляции с грубомодельной молекулярной моделью поддержали эту картину, показав, что кислород проводит относительно мало времени внутри плотных белковых областей.
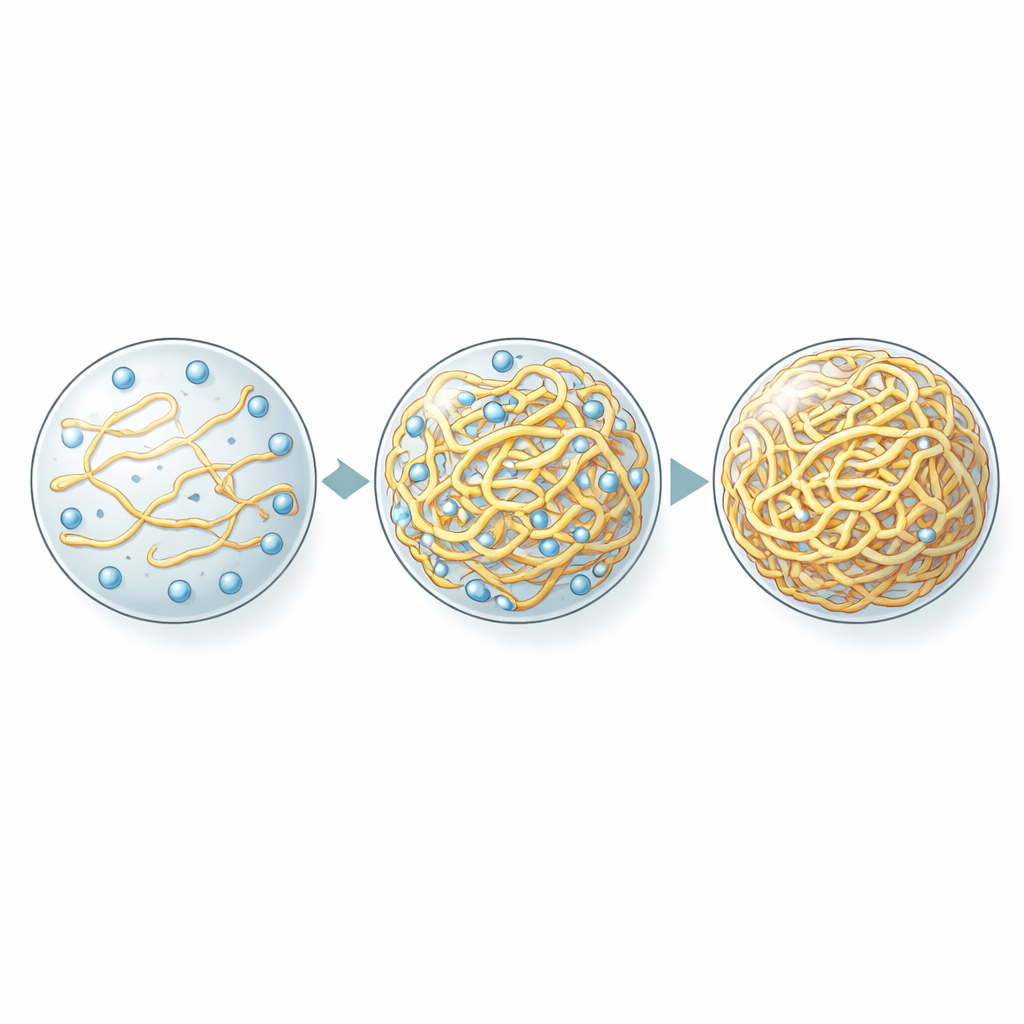
Уровень кислорода задаёт плотность, а не жирность
Очевидным подозреваемым в контроле захвата кислорода была гидрофобность — «жирность» внутренней среды капли — которую ранее считали ключевым фактором для распределения многих других малых молекул в конденсатах. Чтобы проверить это, авторы систематически изменяли последовательности белков, меняя число повторяющихся модулей и их гидрофобную характеристику, а затем измеряли кислород внутри полученных капель. На удивление, уровни кислорода не зависели от того, насколько «масляными» или «водянистыми» были капли. Вместо этого они сильно и обратно пропорционально коррелировали с тем, насколько плотно белок упакован в плотной фазе. Варианты, формировавшие более перегруженные конденсаты, содержали меньше кислорода, даже если в целом они были менее гидрофобными. Другие маленькие жирорастворимые красители вели себя иначе: они по-прежнему предпочитали более гидрофобные капли, что подтвердило, что кислород нарушает обычные правила распределения.
Новый взгляд на нано- и микромасштабные градиенты кислорода
Эти результаты приводят к пересмотру представлений о том, как конденсаты формируют своё химическое окружение. Для малых молекул, которые слабо адсорбируются на каркасных белках, доминирующим фактором становится простая плотность макромолекул: чем больше объёма занимают белки, тем меньше остаётся места для растворённого кислорода. Это означает, что клетки могут формировать градиенты кислорода на расстояниях от нанометров до микрометров просто за счёт образования или растворения конденсатов или изменения степени их уплотнения. В практическом плане работа показывает, что немембранные органеллы могут тонко настраивать доступность кислорода для соседних реакций — потенциально ускоряя одни процессы, замедляя другие или защищая чувствительные компоненты — через физический эффект заполнения пространства, а не через специфическое химическое связывание.
Цитирование: Garg, A., Brasnett, C., Marrink, S.J. et al. Oxygen depletion in biomolecular condensates is dominated by macromolecular density. Nat Commun 17, 2603 (2026). https://doi.org/10.1038/s41467-026-69376-2
Ключевые слова: биомолекулярные конденсаты, распределение кислорода, макромолекулярная перегруженность, фазовое разделение, клеточные микроокружения