Clear Sky Science · ru
Ультрабыстрый раствор-модулируемый механизм «бродяжничества» в бромоформе, выявленный с помощью фемтосекундной рентгеновской рассеяния в растворе
Почему важны крошечные молекулы в воде и воздухе
Бромоформ — небольшое природное соединение, имеющее значительное экологическое значение. Под действием солнечного света в атмосфере или в брызгах океана эта молекула может высвобождать атомы брома, которые способствуют разрушению озона — щита, защищающего нас от вредного ультрафиолета. В этом исследовании ставится на первый взгляд простейший вопрос с далеко идущими последствиями: изменяет ли жидкая среда вокруг бромоформа то, что происходит в первые триллионные доли секунды после воздействия света, и тем самым влияет ли на количество появляющегося озоноразрушающего брома?
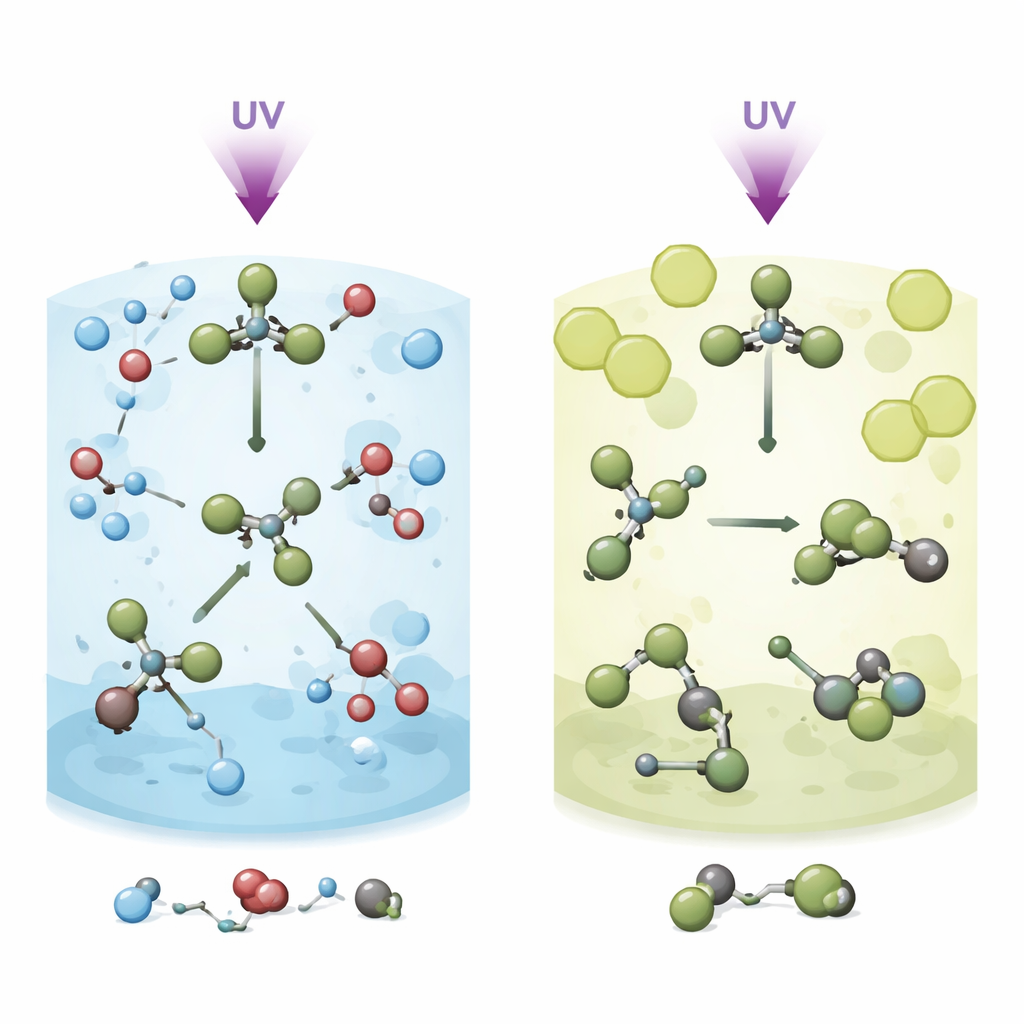
Свет, разрывающий молекулу
Исследователи начинают со вспышек ультракороткого ультрафиолетового света на бромоформ, растворённый в двух разных жидкостях: в метаноле, полярной и химически реакционноспособной среде, и в метилциклоhexане, неполярной и относительно инертной. Свет быстро ослабляет одну из связей углерод—бром в молекуле, заставляя её начинать распадаться. Но вместо того чтобы просто разлететься, один атом брома задерживается и «бродит» вокруг оставшейся части молекулы, CHBr2. Это бродяжничество порождает мимолётную, перестроенную форму — изомер. Главная загадка — что происходит с этим промежуточным состоянием в разных жидкостях и как этот выбор определяет, высвобождает ли бромоформ свободные атомы брома или же превращается в другие продукты.
Съёмка молекулярных фильмов рентгеном
Чтобы наблюдать эти события, команда использует фемтосекундную временноразрешённую рентгеновскую дифракцию в растворе на Европейском рентгеновском свободноэлектронном лазере. По сути, они записывают стробоскопический фильм о том, как меняются межатомные расстояния в реальном времени с пикосекундным и субпикосекундным разрешением. Сравнивая измеренные картины рассеяния с компьютерно‑сгенерированными шаблонами для множества возможных структур, они восстанавливают, как изменяются длины связей и углы внутри бромоформа после возбуждения. Передовые методы анализа и ускоренные машинным обучением симуляции помогают отделить перекрывающиеся реакционные пути и присвоить точные времена жизни короткоживущим промежуточным частицам.
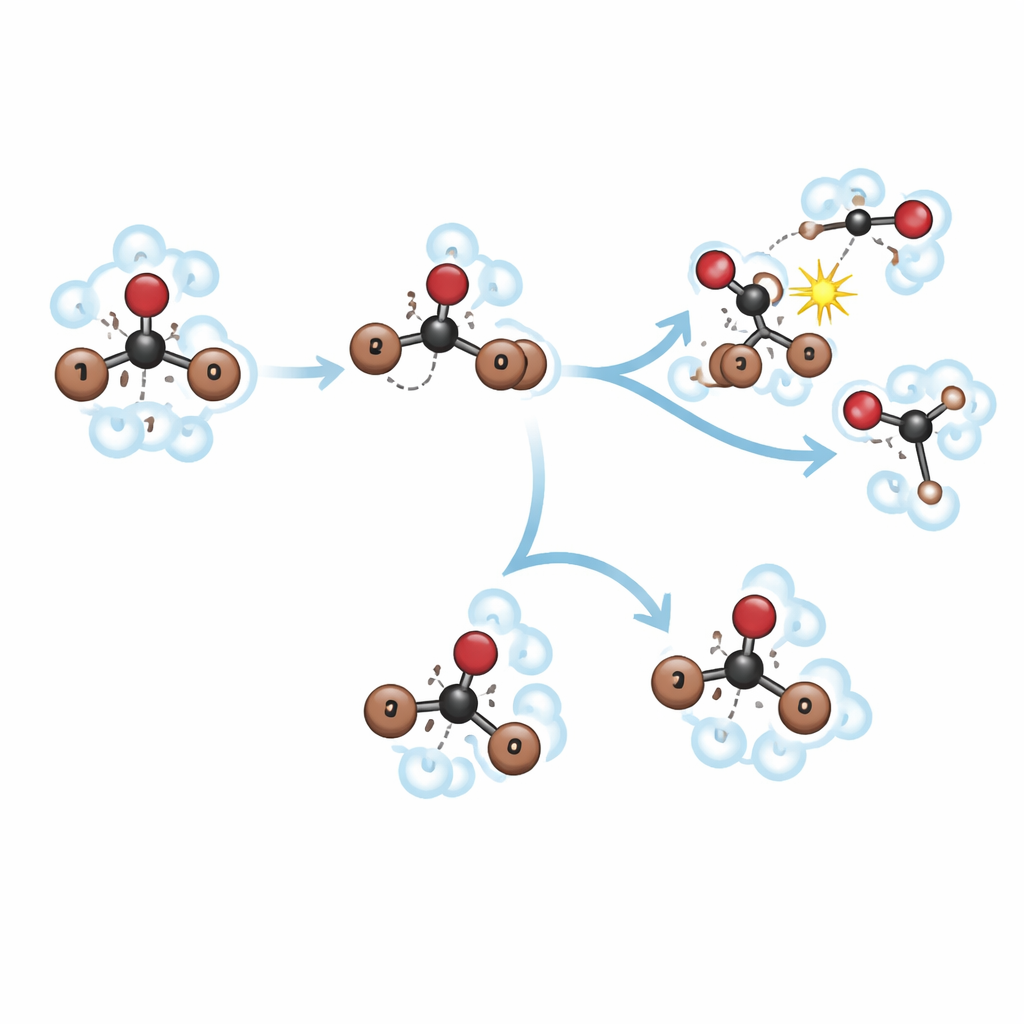
Две жидкости — две очень разные судьбы
В метаноле промежуточное бродяжничество проявляется, но недолговечно. Примерно за 150 фемтосекунд исходная связь углерод—бром разрывается, образуя CHBr2 и бродяжущий бром. В течение следующих ≈400 фемтосекунд этот «горячий», вибрирующий изомер неоднократно растягивается и сгибается, что приводит фрагменты в частые контакты с соседними молекулами метанола. Вместо того чтобы расслабиться в стабильную перестроенную форму, бродяжущая структура быстро перехватывается метанолом в реакции «метанолиза». Это даёт новые молекулы CH3OCHBr2 и HBr, тогда как свободные фрагменты CHBr2 и Br от параллельного, более прямого пути распада продолжают реагировать медленнее в течение нескольких пикосекунд. Плотная молекулярная «клетка» растворителя и его реакционноспособные гидроксильные группы действуют совместно, направляя бромоформ по этому химическому пути вместо образования долгоживущего изомера.
Когда жидкость отступает и даёт бродяжничеству развиться
В метилциклохексане картина меняется радикально. Тот же ультрафиолетовый импульс вновь вызывает бродяжничество примерно за 150 фемтосекунд, но неполярная среда окружает бромоформ более свободно и не склонна к быстрой реакции с ним. Здесь бродяжущий бром и кусок CHBr2 имеют пространство для перенаправления и стабилизации в устойчивую изомерную структуру вместо немедленного взаимодействия с молекулами растворителя. Прямой распад на отдельные фрагменты CHBr2 и Br по‑прежнему происходит и конкурирует с образованием изомера, но теперь перестроенный изомер выживает значительно дольше. Симуляции показывают, что большая, более мягкая «клетка» растворителя в метилциклохексане поощряет газоподобное бродяжничество, в то время как тесная, сильно взаимодействующая «клетка» в метаноле направляет тот же промежуточный продукт прямо в химическую реакцию.
Что это значит для озона и не только
Вместе эти эксперименты и расчёты показывают, что бродяжничество — универсальный ранний этап при поглощении бромоформом ультрафиолета в жидкой среде, но дальнейшую судьбу промежуточного состояния определяет окружающий растворитель. В условиях, подобных метанолу, бродяжничество в основном приводит к очень быстрым реакциям с жидкостью, ограничивая образование долгоживущих изомеров и формируя время и способ появления продуктов, содержащих бром. В средах, похожих на метилциклохексан, бродяжничество, напротив, питает долгоживущий перестроенный изомер, который позже может высвобождать бром в иные временные масштабы. Прямо снимая эти ультрабыстрые движения, работа показывает, что микроскопическая природа капель, аэрозолей и других конденсированных сред может сильно контролировать химические пути молекул, значимых для озона, помогая учёным создавать более точные модели атмосферной и растворнофазной фотохимии.
Цитирование: Su, P., Zhang, J., Wang, H. et al. Ultrafast solvent-modulated roaming mechanism in bromoform revealed by femtosecond X-ray solution scattering. Nat Commun 17, 2514 (2026). https://doi.org/10.1038/s41467-026-69374-4
Ключевые слова: бромоформ, механизм «бродяжничества», ультрабыстрая фотохимия, влияние растворителя, разрушение озона