Clear Sky Science · ru
Соперничающие упорядочения водородных связей определяют аномальную поверхностное натяжение воды
Почему поверхность воды страннее, чем кажется
Поверхность воды позволяет насекомым ходить по прудам, формирует капли дождя и управляет тем, как образуются и лопаются пузыри. Однако при измерении «натяжения» этой поверхности — поверхностного натяжения — учёные обнаруживают, что вода ведёт себя удивительно необычно при охлаждении, особенно когда её охлаждают ниже обычной точки замерзания. В этой статье с помощью продвинутых компьютерных моделирований показано, как скрытая организация молекул воды на поверхности объясняет эту давнюю загадку.
Два скрытых типа жидкой воды
Хотя мы воспринимаем воду как простую однородную жидкость, её молекулы локально могут упорядочиваться двумя контрастными способами. Одно расположение более плотное и беспорядочное; авторы называют его ρ-состоянием. Другое — более открытое и симметричное, когда каждая молекула окружена примерно в четырёхузловой тетраэдрической структуре; это S-состояние. Ранее предполагалось, что баланс между этими двумя локальными структурами помогает объяснить многие аномалии объёмных свойств воды. Здесь авторы исследуют, как та же двухсостоящая картина проявляется на границе воздух–вода, где и формируется поверхностное натяжение.
Как поверхность выстраивает молекулы в линию
На границе воздуха и воды молекулы уже не испытывают одинаковых тяг во всех направлениях. Эта нарушенная симметрия благоприятствует ρ-состоянию, в котором атомы водорода и молекулярные диполи легко наклоняются в предпочтительном направлении. Моделирование показывает, что ближе к комнатной температуре и несколько ниже, самый верхний слой воды заполняется выровненными молекулами ρ-состояния, тогда как S-состояния встречаются чаще немного под поверхностью и в объёме. Поскольку молекулы ρ-состояния сильно выстраиваются, они создают дисбаланс сил — анизотропию напряжений — который генерирует относительно большое поверхностное натяжение по сравнению с обычными жидкостями, такими как бензол.
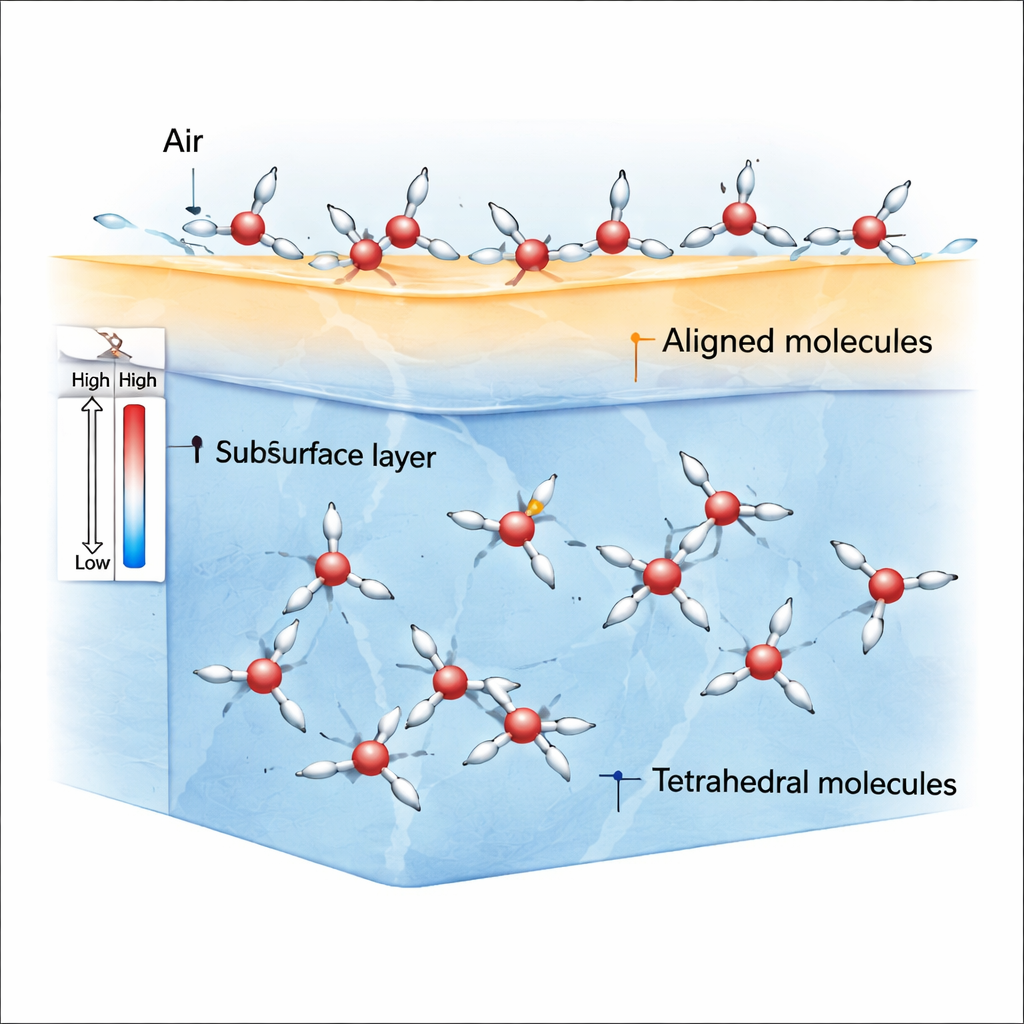
Почему при охлаждении поверхностное натяжение сначала замедляется, а затем ускоряется
В большинстве простых жидкостей охлаждение постепенно усиливает напряжение на поверхности, и поверхностное натяжение растёт почти линейно. Вода делает это только при более высоких температурах. По мере охлаждения к примерно −0,15 °C (275 K) рост поверхностного натяжения начинает замедляться. Моделирование показывает, что это замедление происходит потому, что молекулы ρ-состояния у поверхности уже максимально выровнены; дальнейшее охлаждение почти не меняет их вклад. Одновременно S-состояния в подсurface остаются преимущественно случайно ориентированными, поэтому они мало способствуют увеличению напряжения на поверхности. В результате получается своего рода плато: температура продолжает падать, но поверхностное натяжение растёт лишь вялo.
Глубокое сверхохлаждение вызывает второе усиление натяжения
Когда воду охлаждают значительно глубже, далеко ниже обычной точки замерзания, в область глубокого сверхохлаждения (приблизительно 250 K и ниже), её поведение снова меняется. Доля S-состояний с тетраэдрическими структурами резко возрастает, даже рядом с поверхностью. Существенно то, что эти S-молекулы перестают ориентироваться случайно. Их диполи начинают выравниваться вдоль направления, перпендикулярного поверхности, под действием взаимодействий между соседними молекулярными диполями и области отрицательного давления непосредственно под поверхностью. Как только это происходит, S-состояние воды, которое раньше смягчало поверхностное натяжение, начинает его усиливать. Этот дополнительный упорядоченный вклад даёт возобновлённый, более быстрый рост — «реентрантное» увеличение — поверхностного натяжения при низких температурах.
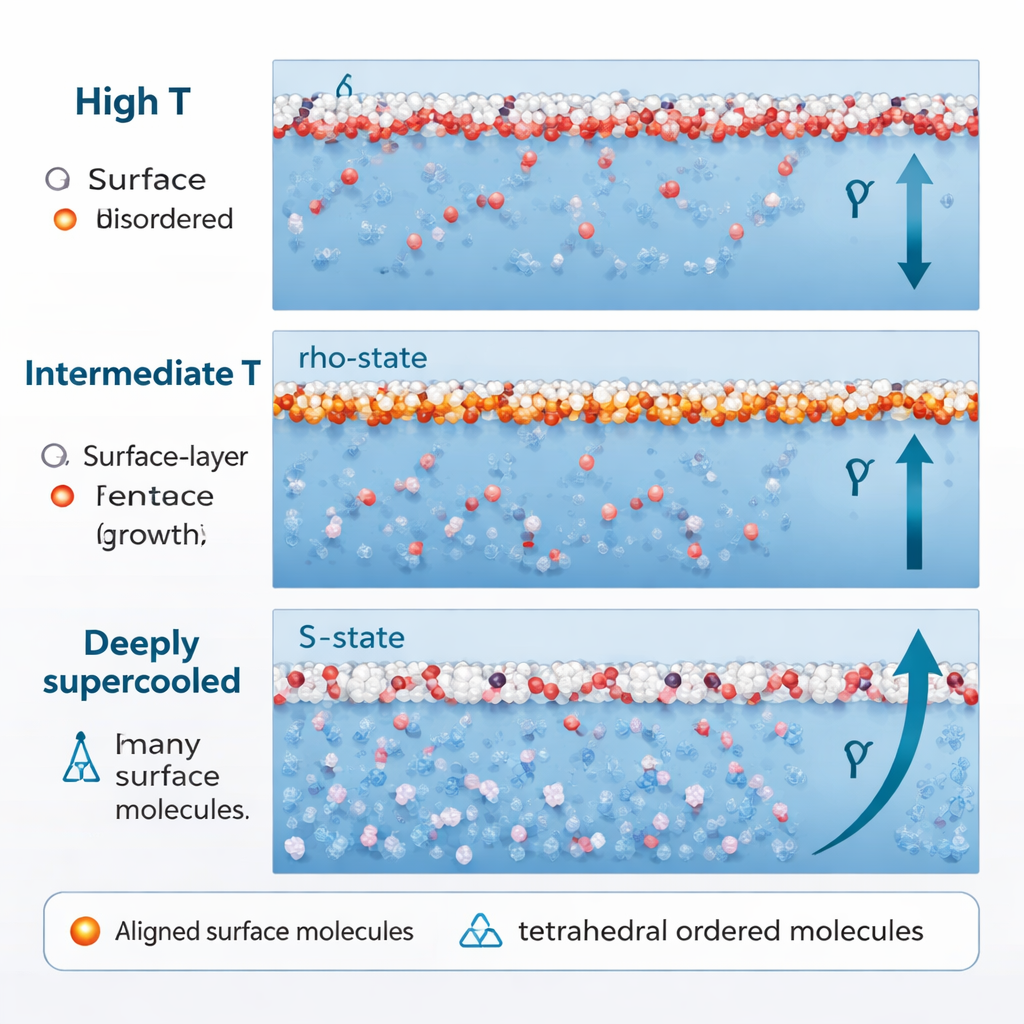
От загадок поверхности к льду и дальше
Те же тетраэдрические кластеры S-состояния, которые жёстчеют поверхность при низких температурах, также напоминают ранние строительные блоки некоторых форм льда, и моделирование показывает их обогащение у интерфейса. Это означает, что граница воздух–вода может служить колыбелью для зарождения льда, что помогает объяснить, почему замерзание часто начинается у поверхностей. В более широком смысле эта работа даёт конкретную молекулярную связь между тем, как молекулы воды организуются и ориентируются, и тем, насколько сильно поверхность тянется внутрь. Эта структурно-механическая картина не только разрешает странную температурную кривую поверхностного натяжения воды, но и предлагает дорожную карту для понимания и управления интерфейсными явлениями в других сеткообразующих жидкостях — от сверхохлажденной воды в облаках до материалов, используемых в технике и биологии.
Цитирование: Yuan, J., Qiu, K., Sun, G. et al. Competing hydrogen-bond orders drive water’s anomalous surface tension. Nat Commun 17, 1498 (2026). https://doi.org/10.1038/s41467-026-69356-6
Ключевые слова: поверхностное натяжение воды, водородная связь, сверхохлажденная вода, структура жидкости, нуклеация льда