Clear Sky Science · ru
STING взаимодействует с TOX, подавляя экспрессию HO-1 и вызывая ферроптоз в инфильтрирующих опухоль CD8+ Т-клетках и устойчивость к иммунотерапии
Почему это исследование важно для лечения рака
Современные иммунотерапии рака работают, освобождая собственные киллерные Т‑клетки организма, но многие опухоли по‑прежнему находят способы их подавлять. В этом исследовании раскрыт скрытый переключатель самоуничтожения внутри CD8+ «киллерных» Т‑клеток, которым пользуется опухоль, и показано, что его отключение может значительно повысить эффективность иммунотерапии.
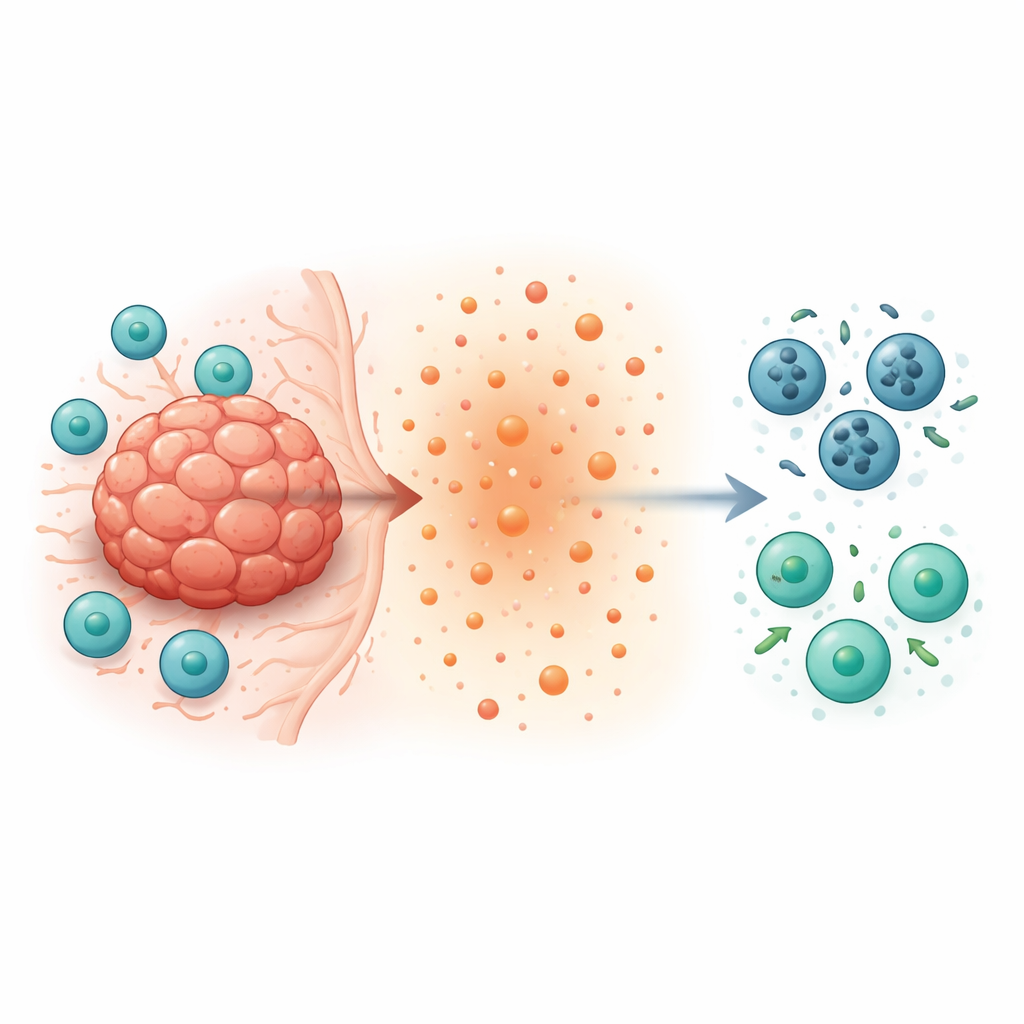
Скрытый путь гибели внутри Т‑клеток, борющихся с опухолью
Внутри опухоли CD8+ Т‑клетки должны выслеживать и уничтожать раковые клетки. Вместо этого они часто становятся редкими, вялыми и недолговечными. Авторы сосредоточились на двух молекулах внутри Т‑клеток — STING, сенсоре повреждений ДНК, и TOX, белке, связанном с истощением Т‑клеток. Они модифицировали мышей так, что у CD8+ Т‑клеток отсутствовал STING, TOX или оба белка, а затем имплантировали несколько типов опухолей. Удивительно, но мыши с Т‑клетками, лишёнными либо STING, либо TOX, намного лучше справлялись с опухолями. Их опухоли росли медленнее, содержали гораздо больше CD8+ Т‑клеток, и эти Т‑клетки продуцировали больше антикарциногенных молекул, таких как интерферон‑гамма и гранзим B. Это указывало на внутреннюю программу, тихо саботирующую Т‑клетки внутри опухолей.
Как железозависимая гибель клеток ослабляет иммунитет
Анализ активности генов в инфильтрирующих опухоль Т‑клетках показал, что нормальные Т‑клетки внутри опухолей были подготовлены к особой форме гибели — ферроптозу. В отличие от апоптоза, ферроптоз запускается перегрузкой железом и накоплением повреждённых липидов в клеточных мембранах. В обычных CD8+ Т‑клетках, подвергшихся воздействию опухолевых клеток, включались гены, способствующие накоплению железа и повреждению липидов, тогда как защитные гены были отключены. Напротив, у Т‑клеток, лишённых STING или TOX, наблюдалась обратная картина: они выражали больше защитных ферментов HO‑1 и GPX4, имели более низкие уровни железа, меньше перекисного окисления липидов, здоровые митохондрии и сопротивлялись ферроптозу. Эксперименты in vitro подтвердили: химическое блокирование ферроптоза сохраняло обычные Т‑клетки живыми, тогда как удаление STING или TOX делало их естественно устойчивыми.
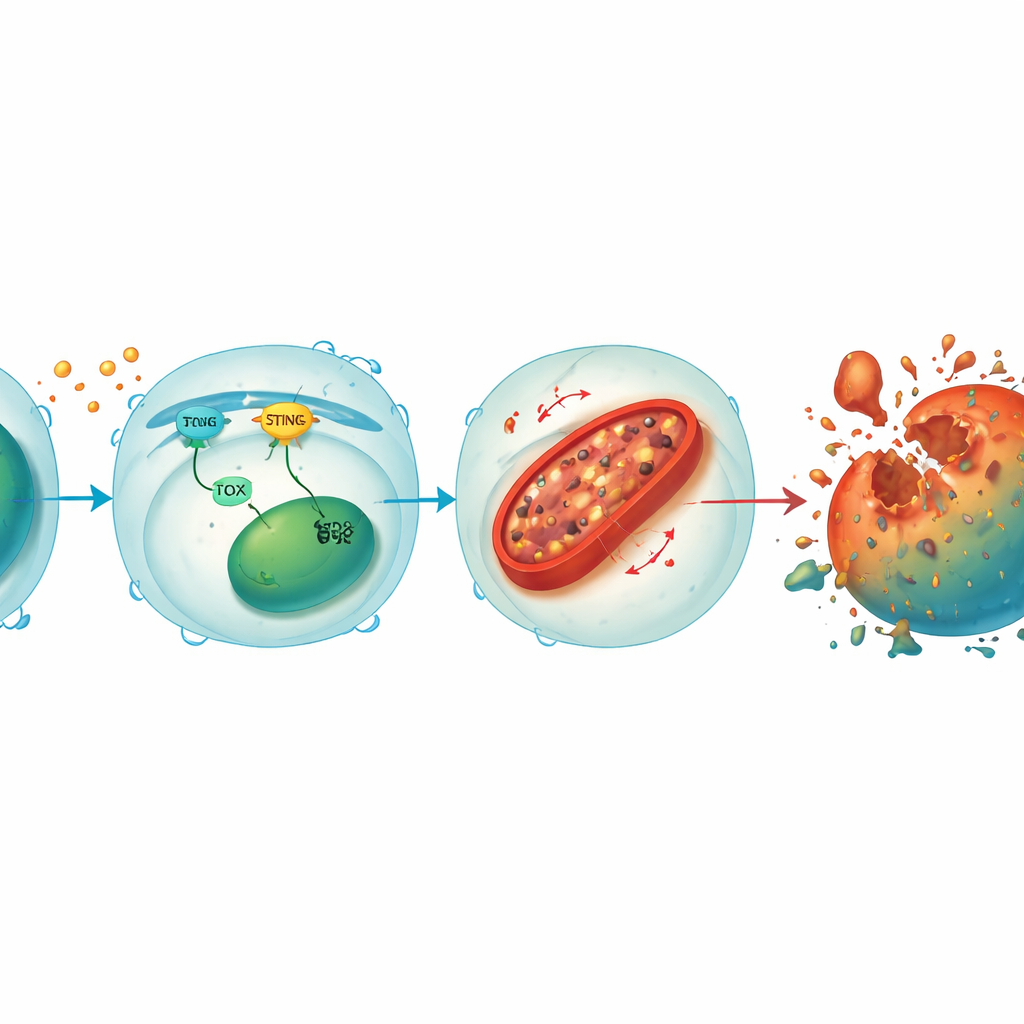
Контур, связывающий сигналы стресса с повреждением митохондрий
Глубже исследование показало, что STING и TOX формируют усиливающийся контур внутри CD8+ Т‑клеток. Когда опухолевые или вирусные сигналы активируют STING, это запускает факторы, повышающие уровень TOX, а TOX, в свою очередь, помогает поддерживать активность STING. Вместе они подавляют HO‑1, фермент, который обычно контролирует уровень клеточного железа. При подавленной экспрессии HO‑1 железо накапливается в митохондриях — «энергетических станциях» клетки — что приводит к росту уровней реактивных кислородных видов и окислению мембранных липидов. Такое митохондриальное повреждение истощает производство энергии и в конечном итоге толкает Т‑клетку в ферроптоз. Восстановление STING или TOX в клетках‑«нокаутах» возвращало перегрузку железом и гибель клеток, тогда как дальнейшее снижение HO‑1 снова делало даже защищённые Т‑клетки уязвимыми, подчёркивая роль HO‑1 как ключевого тормоза этого разрушительного пути.
Как лактат, образующийся в опухоли, нажимает на курок
Микроокружение опухоли богато лактатом — побочным продуктом изменённого метаболизма рака. Исследование показывает, что этот лактат — не просто метаболический мусор: он активно переключает ферроптоз в Т‑клетках. По сравнению с другими клетками CD8+ Т‑клетки особенно чувствительны к лактату. При поступлении в клетки через специфические транспортеры лактат вызывал накопление железа, сжатие митохондрий, потерю митохондриальной ДНК и усиление окислительного повреждения. Одновременно лактат усиливал активность STING и TOX и ещё сильнее подавлял HO‑1. Т‑клетки без STING или TOX гораздо лучше сопротивлялись повреждению, вызванному лактатом. Блокирование ключевого лактатного транспорта препаратом AZD3965 защищало CD8+ Т‑клетки от ферроптоза у мышей, увеличивало их количество внутри опухолей и замедляло рост опухолей, воспроизводя эффект удаления STING в Т‑клетках.
Преобразование уязвимости в терапевтическое преимущество
Эти механистические выводы имеют практическое значение. При применении адоптивной клеточной терапии — введении мышам лабораторно активированных Т‑клеток — исследователи обнаружили, что Т‑клетки, спроектированные без STING или TOX, обеспечивали гораздо лучшую контроль над опухолью по сравнению с обычными Т‑клетками. Более того, сочетание этих «устойчивых к ферроптозу» Т‑клеток с существующими методами, такими как блокаторы контрольных точек PD‑1 или TIM‑3, химиотерапия цисплатином или препарат-активатор STING, давало значительно лучшее уменьшение опухолей, чем любая монотерапия. Наконец, в образцах опухолей пациентов с раком шейки матки более высокий уровень TOX и более низкий уровень HO‑1 в инфильтрирующих лимфоцитах был связан с худшей выживаемостью, что указывает на то, что этот путь влияет и на клинические исходы у людей.
Что это означает для будущей онкологической помощи
Проще говоря, исследование показывает, что опухоли могут заставлять наши лучшие антираковые Т‑клетки «ржаветь» изнутри, вызывая железозависимую форму гибели клеток. Контур лактат–STING–TOX снижает защиту, которую даёт HO‑1, повреждает митохондрии и приводит к ферроптозу, истощая ряды эффективных CD8+ Т‑клеток. Нарушение этого контура — путём создания Т‑клеток без STING или TOX, усиления HO‑1 или блокирования входа лактата — сохраняет Т‑клетки живыми, энергичными и готовыми к атаке. Эта работа указывает путь к терапии следующего поколения, которая сочетает метаболическую и генетическую перенастройку Т‑клеток с существующими препаратами, чтобы преодолеть резистентность и обеспечить более длительный контроль над раком.
Цитирование: Zhu, Q., Zhang, Jb., Nie, Cp. et al. STING synergizes with TOX suppressing HO-1 expression to trigger ferroptosis in tumor-infiltrating CD8+ T cell and immunotherapy resistance. Nat Commun 17, 2543 (2026). https://doi.org/10.1038/s41467-026-69350-y
Ключевые слова: иммунотерапия рака, CD8 T‑клетки, ферроптоз, микроокружение опухоли, путь STING TOX HO-1