Clear Sky Science · ru
Seq-Scope-eXpanded: пространственная омics за пределами оптического разрешения
Видеть клетки в более чётких деталях
Наши тела состоят из бесчисленных крошечных клеток, в каждой из которых кипит жизнь, обычно невидимая даже при мощных микроскопах. В этой работе представлен Seq-Scope-X — метод, который позволяет исследователям приблизиться к внутренней организации тканей с беспрецедентной точностью, картируя, какие гены и белки активны в конкретных точках внутри и между клетками. Такой уровень детализации может изменить подход к изучению развития, иммунной системы и заболеваний, например рака или поражения печени.
Зачем картировать молекулы на месте?
Клетки не функционируют в изоляции: они живут в «районах», образуют слои и специализируются в зависимости от местоположения. Традиционные методы секвенирования разрушают ткань, теряя этот пространственный контекст. Новые инструменты «пространственной омки» сохраняют молекулы на месте, но приходится идти на компромисс. Методы на основе визуализации дают очень тонкую детализацию, но обычно отслеживают ограниченный набор генов. Методы на основе секвенирования могут прочитать почти все гены одновременно, но размывают мелкие детали, часто распространяют сигнал на несколько микрометров — больше, чем многие субклеточные структуры. Авторы поставили цель закрыть этот разрыв: сохранить богатый, неискажённый считываемый объём секвенирования, при этом достичь или превзойти разрешение современных микроскопов.
Растягивание ткани, чтобы превзойти оптические лимиты
Ключевая идея Seq-Scope-X проста на вид: аккуратно увеличить саму ткань, чтобы каждый исходный нанометр структуры стал легче различим. Команда сначала закрепляет молекулы РНК — или специальные ДНК-метки, прикреплённые к антителам — в мягком гидрогеле, формируемом вокруг среза ткани. Затем они расщепляют исходную ткань и набухают гель в солевом растворе, физически увеличивая всё примерно в три раза и при этом сохраняя относительные положения. Этот расширенный гель укладывают на сверхплотную секвенирующую пластину, покрытую захватывающими зондами. При аккуратном нагреве связанные молекулы высвобождаются из геля и перенаправляются на пластину, которую затем секвенируют, чтобы определить, какие гены или белки присутствовали в каждой крошечной координате. 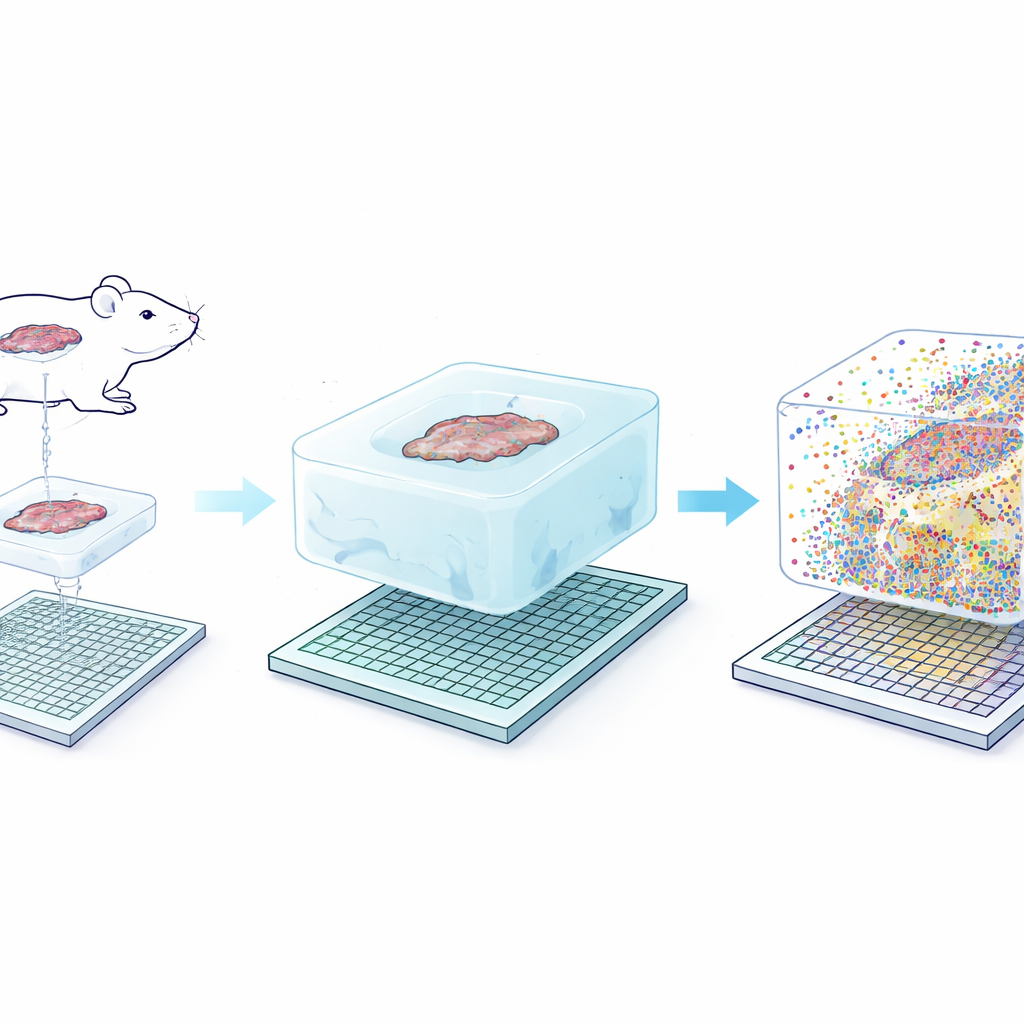
От размытых клеток к субклеточным картам
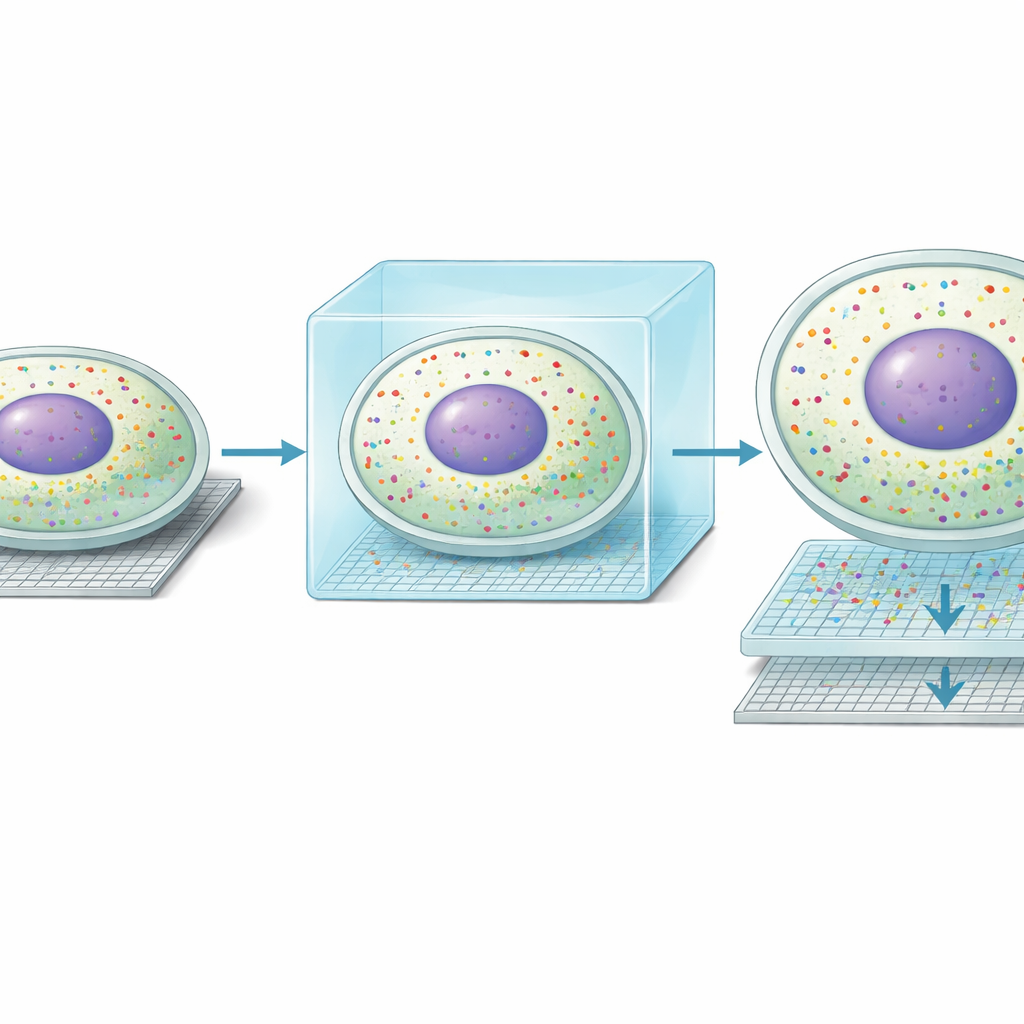
Когда исследователи применили Seq-Scope-X к печёночной ткани мыши, они обнаружили, что метод улучшил пространственное разрешение примерно с 0,6 микрометра до ~0,2 микрометра и увеличил количество измеряемых позиций на квадратный миллиметр почти в десять раз. На практике то, что раньше выглядело как неясные пятна сигнала, теперь разрешилось в чёткие контуры отдельных клеток. Ещё более поразительно то, что кластеры незрелой (несплайсированной) РНК оказались плотно сосредоточены в центрах ядер, тогда как зрелая (сплайсированная) РНК прослеживала окружающую цитоплазму. Это позволило авторам выделять границы клеток, опираясь только на РНК, и разделять ядерные и цитоплазматические экспрессии генов почти для каждого гепатоцита в ткани — то, чего предыдущие методы на базе секвенирования могли лишь косвенно намекать.
Клетки с раздвоенной «личностью»
При такой новой ясности команда обнаружила неожиданную форму молекулярной «двойственности» внутри печёночных клеток. Вдоль известного градиента от сосудов в портальной зоне долек печени к центральной зоне гепатоциты специализируются на разных метаболических задачах. Seq-Scope-X показал, что в многих клетках профиль генов в ядре не совпадал с профилем в окружающей цитоплазме. Примерно у трети гепатоцитов ядерный профиль соответствовал одной зоне, а цитоплазматический — соседней. Независимые методы визуализации, включая MERFISH и одно-молекулярные флуоресцентные РНК-ассайлы, подтвердили, что отдельные транскрипты могут концентрироваться либо в ядре, либо в цитоплазме. В совокупности эти результаты предполагают, что гепатоциты динамически смещают свои метаболические роли во времени: ядро может готовить будущее состояние, тогда как цитоплазма отражает текущий.
Не только печень: мозг, кишечник и иммунные ткани
Затем авторы проверили, работает ли Seq-Scope-X в других органах. В мозге метод чисто разделял разные типы нейронов и вспомогательных клеток и выявлял субклеточные паттерны РНК вокруг ядер. В толстой кишке он разрешал разные подтипы бокаловидных клеток и слои колоноцитов вдоль оси крипта—поверхность, снова фиксируя ядерные подписи. Возможно наиболее впечатляюще, команда адаптировала метод для белков, используя антитела с ДНК-штрихкодами в селезёнке мыши и человеческом миндалине. Seq-Scope-X смог одновременно картировать более сотни различных маркеров на поверхности клеток на разрешении одной клетки, отличая плотно упакованные подмножества Т- и В-клеток и миелоидных клеток. Переключившись на более расширяемую хемию геля, они приблизили эффективное разрешение к истинному наномасштабу, при этом сохранив архитектуру ткани достаточно хорошо для детального картирования.
Что это значит для будущих исследований
Seq-Scope-X показывает: физическое увеличение тканей перед секвенированием помогает преодолеть давние ограничения разрешения, обеспечивая детализацию почти на уровне микроскопа при одновременном считывании тысяч генов или белковых меток. Для непрофессионального наблюдателя это означает, что учёные теперь могут создавать «молекулярные атласы», которые не только указывают, где находятся клетки, но и показывают, что происходит внутри разных частей каждой клетки. Такие карты могут помочь объяснить, как ткани реагируют на повреждение, как организуются иммунные клетки в лимфоидных органах и опухолях, или как тонкие внутренние сдвиги в клетках предвещают болезнь. Хотя нужны дальнейшие улучшения для расширения покрытия и оптимизации некоторых панелей окрашивания, Seq-Scope-X открывает мощное новое окно в микроскопические ландшафты, лежащие в основе здоровья и болезни.
Цитирование: Anacleto, A., Cheng, W., Feng, Q. et al. Seq-Scope-eXpanded: spatial omics beyond optical resolution. Nat Commun 17, 2564 (2026). https://doi.org/10.1038/s41467-026-69346-8
Ключевые слова: пространственная транскриптомика, расширение тканей, омика одиночных клеток, пространственная протеомика, зонация печени