Clear Sky Science · ru
Производимый микробиотой IPA защищает от колита, регулируя кишечный HMGCS2‑опосредованный кетогенез для содействия заживлению слизистой
Почему бактерии кишечника важны при повреждениях слизистой
Когда слизистая оболочка кишечника повреждена, как при воспалительных заболеваниях кишечника (ВЗК) или после агрессивных медицинских вмешательств, организму необходимо быстро восстановить эту внутреннюю «кожу», чтобы предотвратить утечку вредного содержимого в кровь. В этом исследовании раскрывается, как одна молекула, производимая доброжелательными кишечными бактериями, помогает кишечнику самовосстанавливаться, указывая на новые подходы к лечению хронических заболеваний кишечника без глобального подавления иммунной системы.
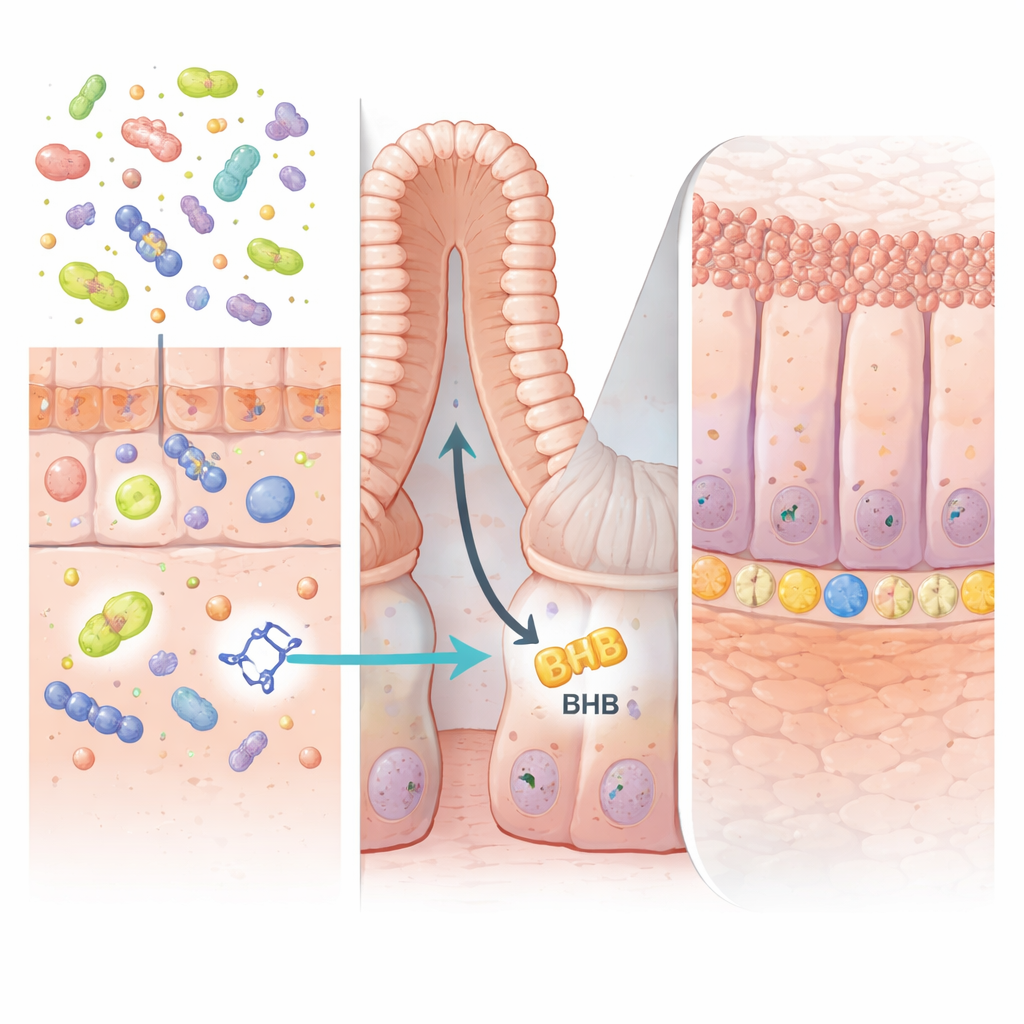
Полезный сигнал от дружелюбных микробов
Исследователи начали с сопоставления химических отпечатков в пробах стула пациентов с ВЗК и здоровых добровольцев, а также в нескольких мышиных моделях колита. Среди сотен молекул выделялась одна: индол-3-пропионовая кислота (IPA), продукт распада пищевой аминокислоты триптофана, синтезируемый некоторыми кишечными бактериями. Уровни IPA систематически были ниже у больных болезнью Крона и у мышей с колитом по сравнению со здоровыми контрольными группами. Это позволило предположить, что потеря IPA может быть частью того, что идет не так, когда слизистая воспаляется и не может восстановиться.
Укрепление защитной стенки кишечника
Чтобы проверить, является ли IPA простым маркером болезни или действительно защищает от нее, команда вводила IPA мышам до индуцирования разных типов повреждений кишечника, включая химический колит и радиационную травму. У мышей, получавших адекватные дозы IPA, были более длинные и здоровые толстые кишки, меньше воспалительных изменений при микроскопии и более толстый слой слизи с плотными клеточными контактами. Они демонстрировали меньшую утечку воспалительных маркеров и больше бокаловидных клеток, вырабатывающих защитный слизистый слой. Важно, что эти преимущества наблюдались даже у безмикробных животных, лишенных собственной микробиоты, что показывает: присутствие IPA само по себе способно напрямую действовать на слизистую кишечника без участия других микробов.
Питание стволовых клеток особым видом энергии
Ключ действия IPA находился глубоко в кишечных «криптах» — крошечных карманах, где располагаются стволовые клетки и постоянно обновляют эпителий. Авторы показали, что IPA включает белок PPARα в кишечных эпителиальных клетках. Это, в свою очередь, усиливает производство фермента HMGCS2, который запускает кетогенез — процесс синтеза энергетически богатой молекулы β‑гидроксибутирата (BHB). Повышенный уровень BHB в стенке кишечника стимулировал расширение LGR5‑положительных стволовых клеток и ускоренное восстановление поврежденных тканей. Когда фермент HMGCS2 или PPARα селективно удаляли из кишечных клеток у мышей, IPA уже не мог усиливать активность стволовых клеток или защищать от колита, что подтверждает, что этот путь производства кетонов необходим для эффекта.
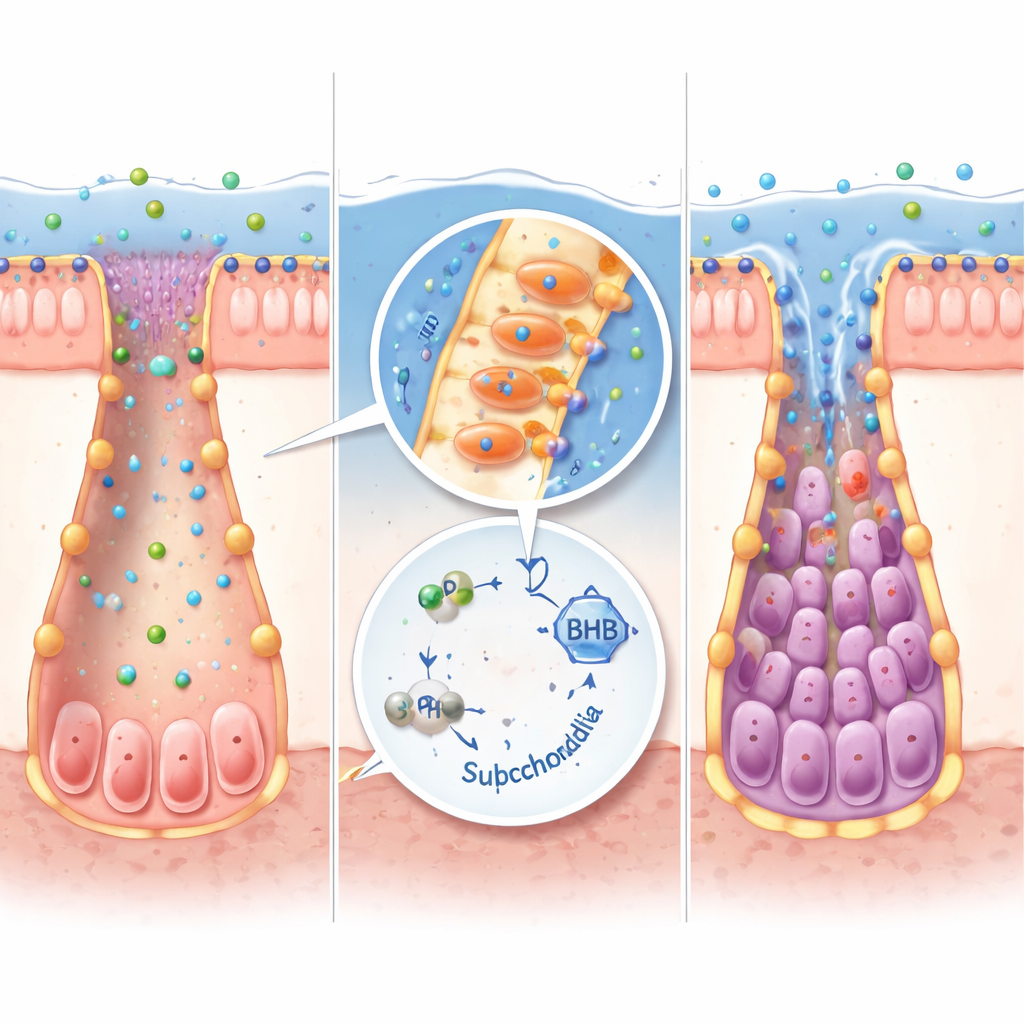
От бактериальных «фабрик» к человеческим тканям
Не все кишечные бактерии способны синтезировать IPA. Повторно проанализировав крупные наборы данных по микробиомам, исследователи выделили Peptostreptococcus russellii как ключевого производителя IPA, который истощен в нескольких когортах пациентов с ВЗК. В лабораторных культурах эта бактерия эффективно превращала триптофан в IPA. Когда безмикробые мыши были заселены P. russellii, их уровни IPA повышались, включались гены кетогенеза, увеличивались маркеры стволовых клеток, и тяжесть колита снижалась по сравнению с мышами, получившими обычную микробную трансплантацию. Тот же путь IPA→кетоны работал и в мини‑органоидах кишечника, выращенных из мышиных и человеческих тканей: добавление IPA или BHB помогало стволовым клеткам восстановиться после воспалительного повреждения и одновременно снижало провоспалительные сигналы.
Что это может значить для будущего лечения
В совокупности работа описывает простую, но мощную цепочку событий: определенные кишечные бактерии превращают пищевой триптофан в IPA; IPA активирует метаболический переключатель в кишечных клетках; этот переключатель усиливает выработку BHB; а BHB, в свою очередь, оживляет стволовые клетки, которые восстанавливают слизистую. Для людей с ВЗК или другими состояниями, повреждающими кишечный барьер, терапии, восстанавливающие IPA или безопасно имитирующие его эффект — через диету, таргетированные пробиотики или специально разработанные препараты — могут способствовать истинному заживлению слизистой без широкого подавления иммунитета. Хотя необходимы дополнительные клинические исследования, ось «микроб→метаболит→стволовая клетка» предлагает многообещающий новый подход к восстановлению кишечника изнутри.
Цитирование: Zhang, Y., Tu, S., Shao, X. et al. Microbiota-derived IPA protects against colitis by regulating intestinal HMGCS2-mediated ketogenesis to facilitate mucosal healing. Nat Commun 17, 2437 (2026). https://doi.org/10.1038/s41467-026-69341-z
Ключевые слова: микробиота кишечника, кишечные стволовые клетки, воспалительное заболевание кишечника, метаболиты микробов, заживление слизистой