Clear Sky Science · ru
CD38 разрушает MAVS через митофагию, подавляя секрецию интерферона типа I в клетках назофарингеальной карциномы и ослабляя противоопухолевый ответ CD8+ T-клеток
Почему это важно для лечения рака
Назофарингеальная карцинома — злокачественная опухоль в носоглотке, особенно распространённая в Восточной и Юго‑Восточной Азии. Иммунотерапия, высвобождающая возможности собственных Т‑клеток организма, изменила прогноз некоторых пациентов, но большинство по‑прежнему не получает выгоды. В этом исследовании выявлен скрытый «тормоз» внутри самих опухолевых клеток: молекула CD38, которая тихо отключает внутреннюю систему тревоги и ослабляет атаку опухоль‑убивающих CD8 T‑клеток. Понимание и блокирование этого тормоза может сделать существующие иммунотерапии эффективными для гораздо большего числа пациентов.
Скрытый переключатель на опухолевых клетках
Исследователи сосредоточились на CD38 — белке, найденном на многих иммунных клетках, но также присутствующем на клетках назофарингеальной карциномы. Предыдущие работы связывали CD38 с сопротивляемостью популярным препаратам, нацеленным на контрольные точки PD‑1 и PD‑L1. Здесь команда поставила вопрос, меняет ли CD38 внутри опухолевых клеток способность CD8 T‑клеток распознавать и уничтожать эти клетки. Выращивая человеческие опухолевые клетки с CD38 или без неё в присутствии активированных человеческих CD8 T‑клеток, они обнаружили, что удаление CD38 из раковых клеток делало Т‑клетки значительно более эффективными: те выделяли больше ключевых молекул атаки, лучше выживали и уничтожали больше опухолевых клеток. При восстановлении CD38 функции Т‑клеток ослабевали, что указывает на CD38 как на внутриклеточный супрессор иммунной атаки.
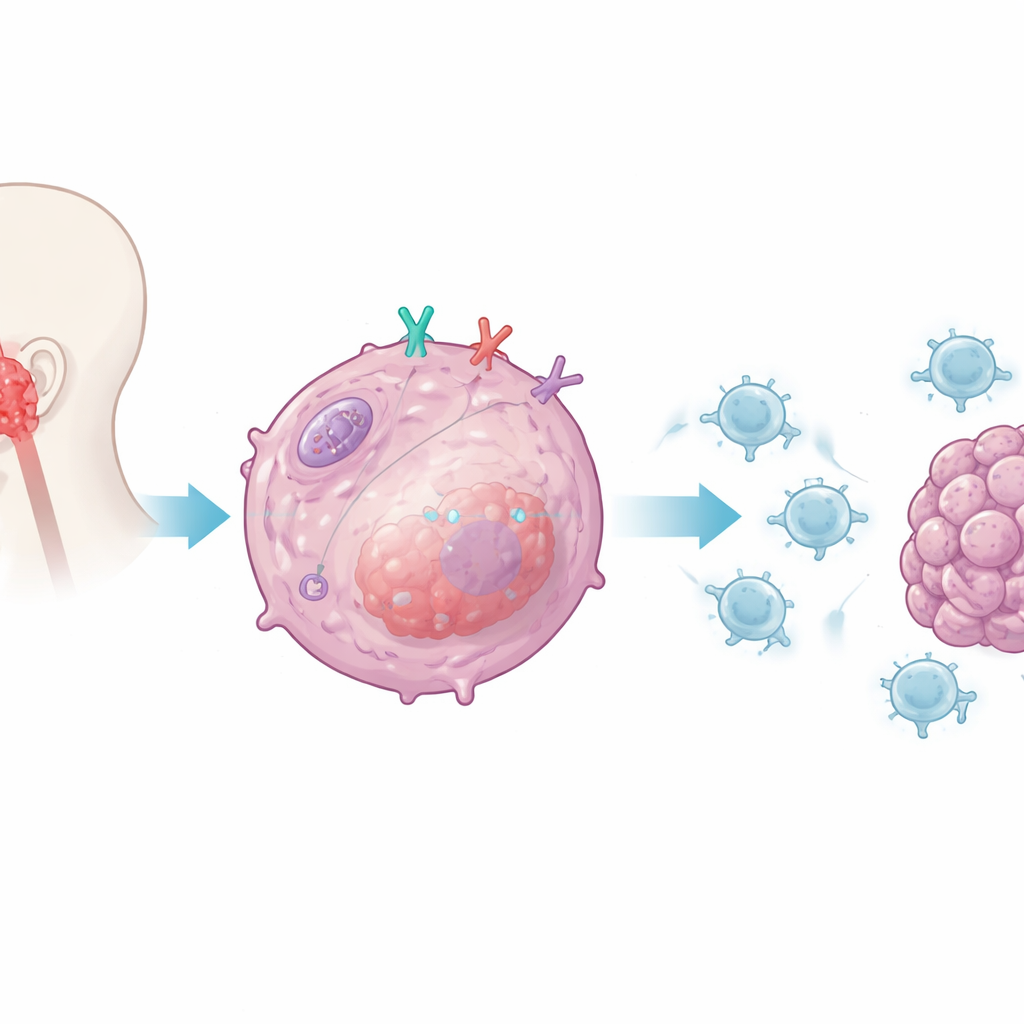
Понижение внутренней системы тревоги клетки
Затем команда изучила, как CD38 передаёт этот подавляющий сигнал. Они сфокусировались на врождённой системе тревоги опухолевой клетки, которая обычно распознаёт вирусоподобный генетический материал и запускает синтез интерферонов типа I — мощных иммуностимулирующих медиаторов. В опухолевых клетках без CD38 исследователи зафиксировали сильный рост интерферона‑бета и хемокинов, привлекающих CD8 T‑клетки в опухоль. Они показали, что CD38 избирательно притупляет путь, контролируемый внутренним сенсором RIG‑I и его адаптерным белком MAVS, который располагается на митохондриях — энергетических станциях клетки. При наличии CD38 активация этого пути и downstream‑сигнальные молекулы была подавлена; при удалении CD38 сигнализация и выработка интерферона резко возрастали, повышая «видимость» опухоли для иммунной системы.
Как CD38 уничтожает ключевой сигнальный узел
Углубляясь, учёные обнаружили, что CD38 физически ассоциируется с MAVS на митохондриях и нарушает взаимодействие MAVS с RIG‑I, ослабляя передачу сигнала. Ещё более показательно, при повышенном уровне CD38 наблюдалось снижение количества белка MAVS без изменений его генетической экспрессии, что указывает на активное разрушение. Тесты с различными ингибиторами показали, что эта потеря зависит от механизмов утилизации внутри клетки, известных как аутофагия, и в частности от формы аутофагии, направленной на митохондрии. CD38 повышал маркеры митохондриального «самопоедания», снижал уровни ряда митохондриальных белков и способствовал упаковке MAVS в аутолизосомные структуры, подвергаемые последующему разрушению. Блокирование митохондриальной аутофагии сохраняло MAVS и восстанавливало интерферонную сигнализацию, что указывает на то, что CD38 отключает тревогу, направляя MAVS в поток клеточных отходов.
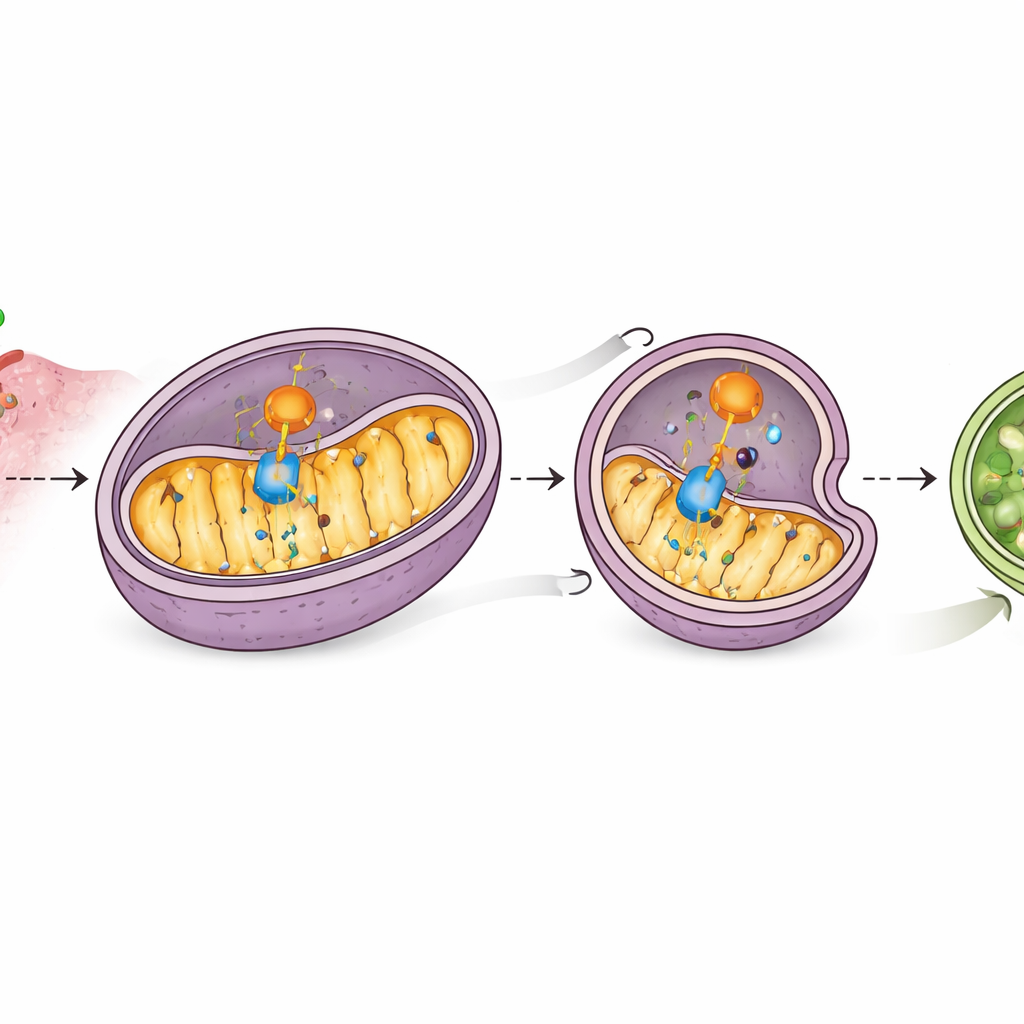
Помощник, направляющий митохондрии к самоуничтожению
Исследование выявило ещё одного участника — PHB2, белок внутри митохондрий, выступающий рецептором для целенаправленного удаления митохондрий. Масс‑спектрометрия и эксперименты по связыванию показали, что CD38 взаимодействует с PHB2 и увеличивает присутствие PHB2 в митохондриях, где PHB2 в свою очередь привлекает основную аутофагическую аппаратуру. PHB2 также связывается с MAVS, и CD38 усиливает этот контакт. При уменьшении уровня PHB2 CD38 уже не мог эффективно вызывать митохондриальную аутофагию, уровни MAVS восстанавливались, и гены, связанные с интерфероном, снова активировались. Это раскрывает цепочку событий: CD38 вовлекает PHB2, PHB2 связывает MAVS, и вместе они направляют MAVS в митохондрии, предназначенные для деградации, заглушая интерфероновую тревогу.
Данные на животных моделях
Чтобы проверить влияние в живом организме, исследователи использовали мышиные опухоли, спроектированные без CD38. В иммунокомпетентных мышах такие опухоли росли медленнее, содержали больше CD8 T‑клеток и имели более высокую долю клеток, продуцирующих интерферон‑гамма — маркер активного противоопухолевого ответа. Блокада рецептора интерферонов типа I устраняла это преимущество, подтверждая, что интерфероновая сигнализация необходима для усиленного иммунного ответа. У гуманизированных мышей с назофарингеальными опухолями снижение CD38 аналогично замедляло рост и увеличивало инфильтрацию CD8 T‑клеток, но этот эффект исчезал, когда в опухолевых клетках одновременно снижали MAVS. Эти in vivo‑результаты подтверждают идею о том, что ось CD38–PHB2–MAVS внутри опухолевых клеток формирует силу Т‑клеточного ответа организма.
Что это значит для будущих терапий
В целом работа показывает, что CD38 в клетках назофарингеальной карциномы действует как внутренний саботёр анти‑опухолевого иммунитета. Посредством избирательной формы митохондриальной утилизации CD38 истощает MAVS, ослабляет продукцию интерферонов типа I, снижает презентацию антигенов и в конечном итоге притупляет атаку CD8 T‑клеток. Существующие препараты‑ингибиторы CD38 в основном нацелены на его ферментативную активность и не удаляют сам белок и не восстанавливают MAVS. Авторы полагают, что новые стратегии, направленные на снижение уровней CD38 или разрыв его взаимодействия с PHB2 либо MAVS, могут повторно включить интерфероновую тревогу внутри опухолей. В сочетании с текущими ингибиторами контрольных точек такие подходы могли бы превратить многие назофарингеальные — и, возможно, другие — опухоли из иммунно‑холодных в иммунно‑реактивные.
Цитирование: Liang, L., Li, W., Liu, S. et al. CD38 degrades MAVS through mitophagy to inhibit type I interferon secretion in nasopharyngeal carcinoma cells and impairs CD8+T cell-mediated anti-tumor immunity. Nat Commun 17, 2544 (2026). https://doi.org/10.1038/s41467-026-69339-7
Ключевые слова: назофарингеальная карцинома, раковая иммунотерапия, интерферон типа I, CD8 T-клетки, митофагия