Clear Sky Science · ru
Оценка методов восстановле́ния пути передачи сигналов EGF с использованием фосфопротеомики и взаимодействий киназа–субстрат
Почему это важно за пределами лаборатории
Наши клетки постоянно воспринимают и реагируют на сигналы из окружения. Один из важнейших таких сигналов — эпидермальный фактор роста (EGF), который регулирует рост, деление и выживание клеток. Когда эта система связи нарушается, это может приводить к развитию рака и другим заболеваниям. В исследовании поставлен на первый взгляд простой, но важный вопрос: если использовать современные мощные методы измерений и вычислительные модели, насколько глубже мы сможем понять путь передачи сигналов EGF по сравнению с тем, что показано в учебниках?
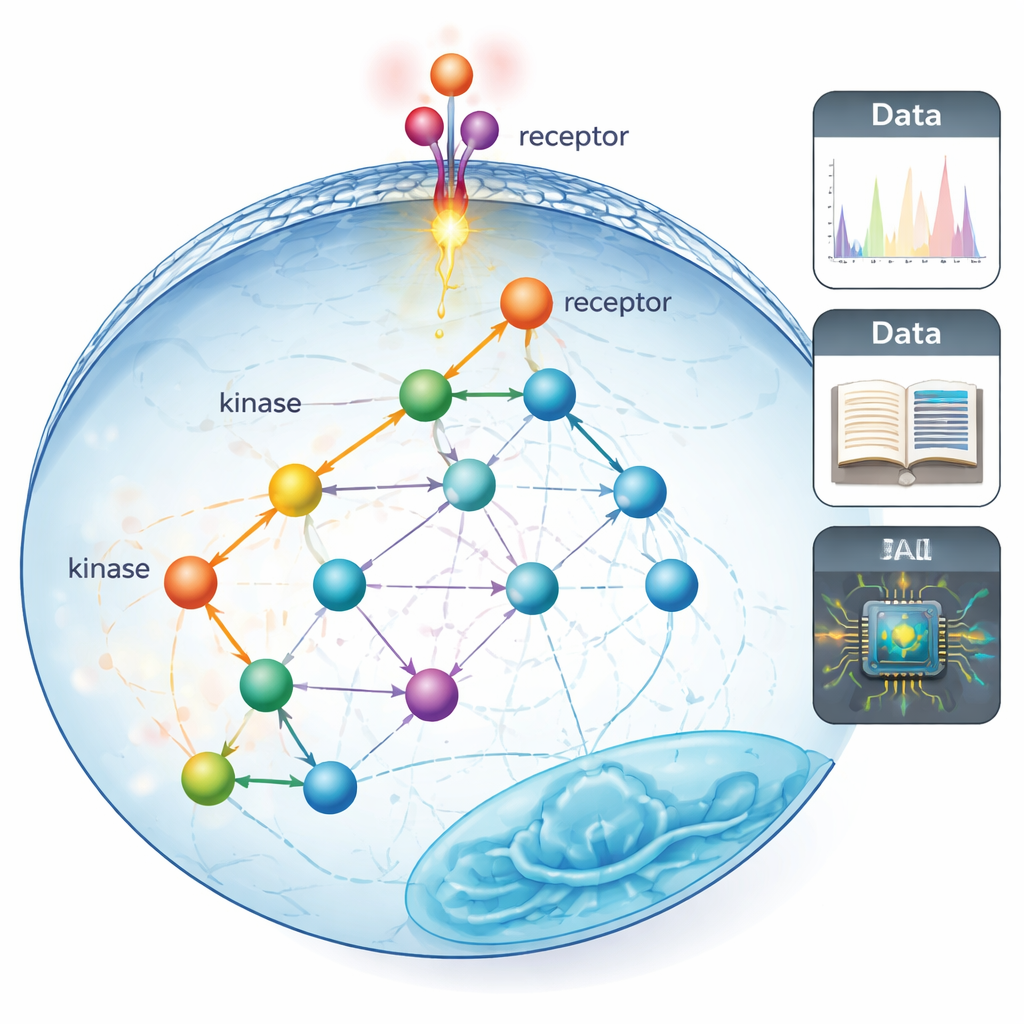
От прямых линий к реалистичным схемам проводки
Традиционные «сигнальные пути» часто изображают в виде аккуратных, почти линейных цепочек белков, передающих сообщение от поверхности клетки к ядру. Эти карты создавались десятилетиями с помощью медленных таргетных экспериментов, которые могли изучать лишь по несколько белков за раз. Авторы утверждают, что это дало узкое, «под фонарем» представление: мы хорошо знаем немногих белков, которые было легко исследовать, и гораздо меньше — о широкой сети связей, которая, вероятно, существует в реальных клетках.
Слушая тысячи молекулярных переключателей одновременно
Чтобы выйти за рамки этого ограниченного взгляда, команда использовала фосфопротеомику — метод массовой спектрометрии, способный одновременно отслеживать десятки тысяч небольших химических меток, фосфатных групп, на белках. Эти метки наносятся ферментами — киназами — и действуют как быстрые выключатели сигнала. Исследователи сначала собрали наиболее полные на сегодняшний день карты «кто может фосфорилировать кого», объединив три вида информации: отобранные данные из литературы, прогнозы искусственного интеллекта, анализирующего последовательности белков, и крупномасштабные экспериментальные скрининги предпочтений киназ. Это существенно расширило покрытие известных или предполагаемых связей киназа–субстрат с примерно 5% измеряемых сайтов до примерно 70–80%.
Тестирование устойчивости сигнала EGF в множестве экспериментов
Далее они сфокусировались на ответе на EGF — классическом пути, играющем ключевую роль при раке легких, молочной железы, кожи и мозга. Группа объединила три передовые опубликованные выборки данных с тремя новыми, очень глубокими временными измерениями в клетках, происходящих из почки, а также двумя контрольными исследованиями с иными стимулами. В сумме эти эксперименты измеряли более 40 000 сайтов фосфорилирования в каждом наборе данных и отслеживали, как их уровни менялись в первые минуты после стимуляции EGF. Хотя общие шаблоны немного различались между типами клеток и технологиями, ключевые сайты фосфорилирования в пути EGF многократно активировались, подтверждая, что основной сигнал стабилен даже в разнотипных экспериментах.
Восстановление скрытого диалога между киназами
Выяснив, какие киназы стали более или менее активными, авторы затем попытались воссоздать лежащий в основе «диалог» между ними: какие киназы, вероятно, активируют или влияют на другие. Они преобразовали карты киназа–субстрат в сети киназа–киназа и применили три вычислительных подхода — от простых схем ранжирования до более сложного метода, который заставляет результат выглядеть как направленное дерево, корнем которого является рецептор EGF. Полученные восстановленные пути сравнивали с несколькими видами «эталонов»: тщательно курируемой картой EGF из базы данных, крупномасштабными экспериментами с сверхэкспрессией отдельных киназ и парами сайтов киназ, поведение которых сильно коррелировало во времени.
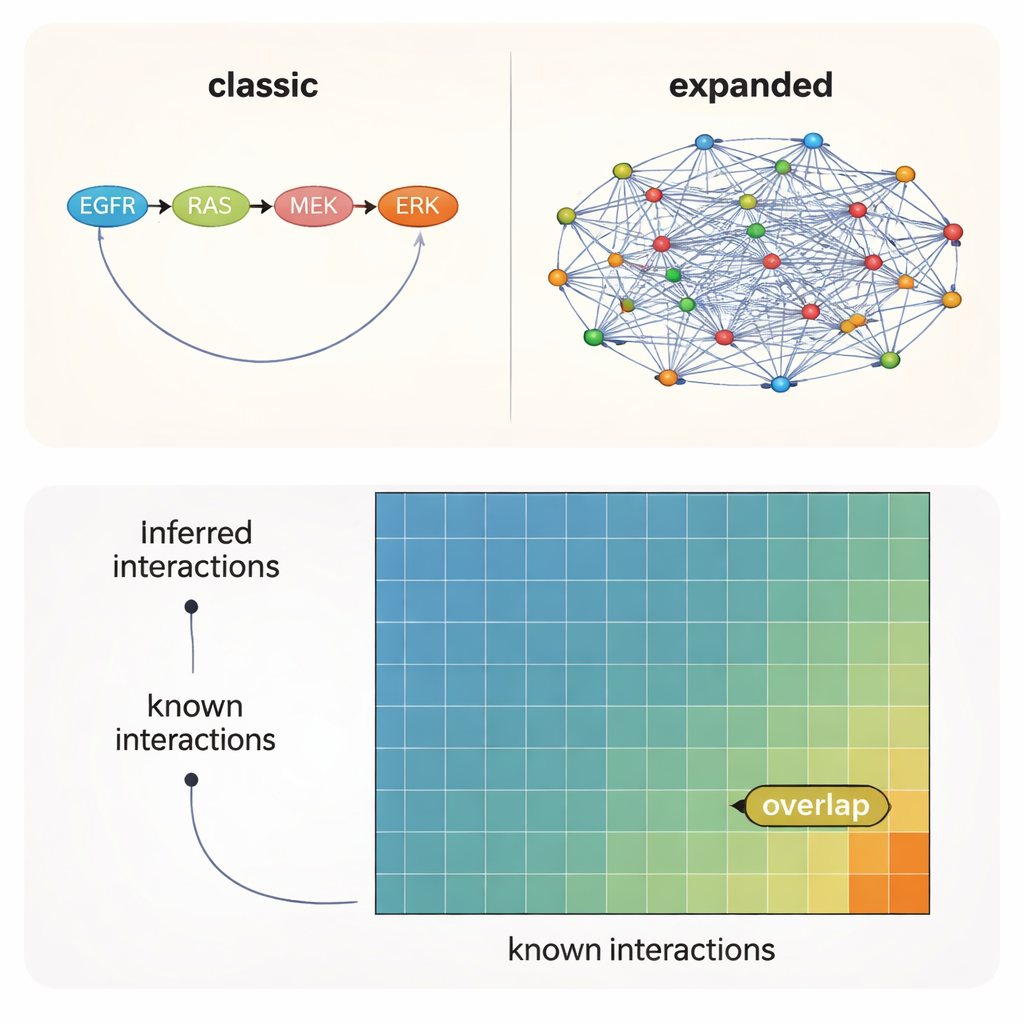
Наиболее правдоподобные связи всё ещё отсутствуют на официальной карте
Во всех тестах один вывод был очевиден: выбор априорных знаний — сети, которую вы подаёте в алгоритм — имел большее значение, чем конкретный метод или даже экспериментальный контекст. Сети, построенные на основе литературы, восстанавливали наибольшее число известных взаимодействий, тогда как более широкие предиктивные ресурсы указывали на множество дополнительных правдоподобных связей, которые ещё не задокументированы официально. Даже в лучших условиях только около 10–12% взаимодействий, предложенных данными и моделями, присутствовали в каких-либо эталонных наборах. Другими словами, примерно 90% поддерживаемых связей киназа–киназа остаются в неизведанной области.
Что это значит для будущих терапий
Для неспециалистов главный вывод таков: известная схема пути EGF в учебниках, вероятно, лишь вершина айсберга. Современная фосфопротеомика в сочетании с продвинутыми вычислительными методами раскрывает гораздо более богатую и запутанную сеть сигнализации. Многие из этих новых предложенных связей могут быть упущенными путями, которыми клетки рака перенаправляют сигналы, чтобы уклониться от лекарств, или новыми возможностями для разработки более умных комбинаций препаратов. Исследование не доказывает, что каждая новая связь реальна, но оно предоставляет дорожную карту и открытые инструменты для проверки этих идей, с конечной целью — более точных и эффективных терапий при заболеваниях, где сигнализация EGF играет ключевую роль.
Цитирование: Garrido-Rodriguez, M., Potel, C., Burtscher, M.L. et al. Benchmarking EGF signaling pathway inference using phosphoproteomics and kinase-substrate interactions. Nat Commun 17, 2071 (2026). https://doi.org/10.1038/s41467-026-69332-0
Ключевые слова: сигнализация EGF, фосфопротеомика, протеинкиназы, сети клеточной сигнализации, онкобиология