Clear Sky Science · ru
Mycobacterium tuberculosis модулирует фосфорилирование субъединицы хоста ATP6V1E1, чтобы способствовать внутриклеточному выживанию
Почему это важно в борьбе с туберкулезом
Туберкулез по-прежнему остаётся одним из самых смертоносных инфекционных заболеваний в мире, убивая более миллиона человек ежегодно. Наши клетки иммунной системы оснащены мощными «кислыми мусоросборниками», которые обычно переваривают проникающие микроорганизмы. В этой работе показано, как бактерия туберкулёза, Mycobacterium tuberculosis (Mtb), саботирует систему ацидификации внутри наших клеток, и что препарат, нацеленный на этот приём, может помочь инфицированным животным эффективнее очищать инфекцию.
Кислотная ванна клетки для микробов
Когда бациллы туберкулёза вдыхаются в лёгкие, их быстро поглощают иммунные клетки — макрофаги. Бактерии оказываются в мембранных пузырах, которые должны сливаться с лизосомами — маленькими мешочками, заполненными пищеварительными ферментами, действующими лучше всего в сильно кислой среде. Эта кислотность создаётся молекулярным насосом, вакуолярной ATPазой (V-ATPase), которая использует клеточное топливо, чтобы загонять протоны в лизосомы и понижать внутренний pH. Правильная ацидификация важна для разрушения Mtb, однако десятилетия исследований показывают, что этот патоген каким-то образом удерживает свои компартменты менее кислыми и выживает.
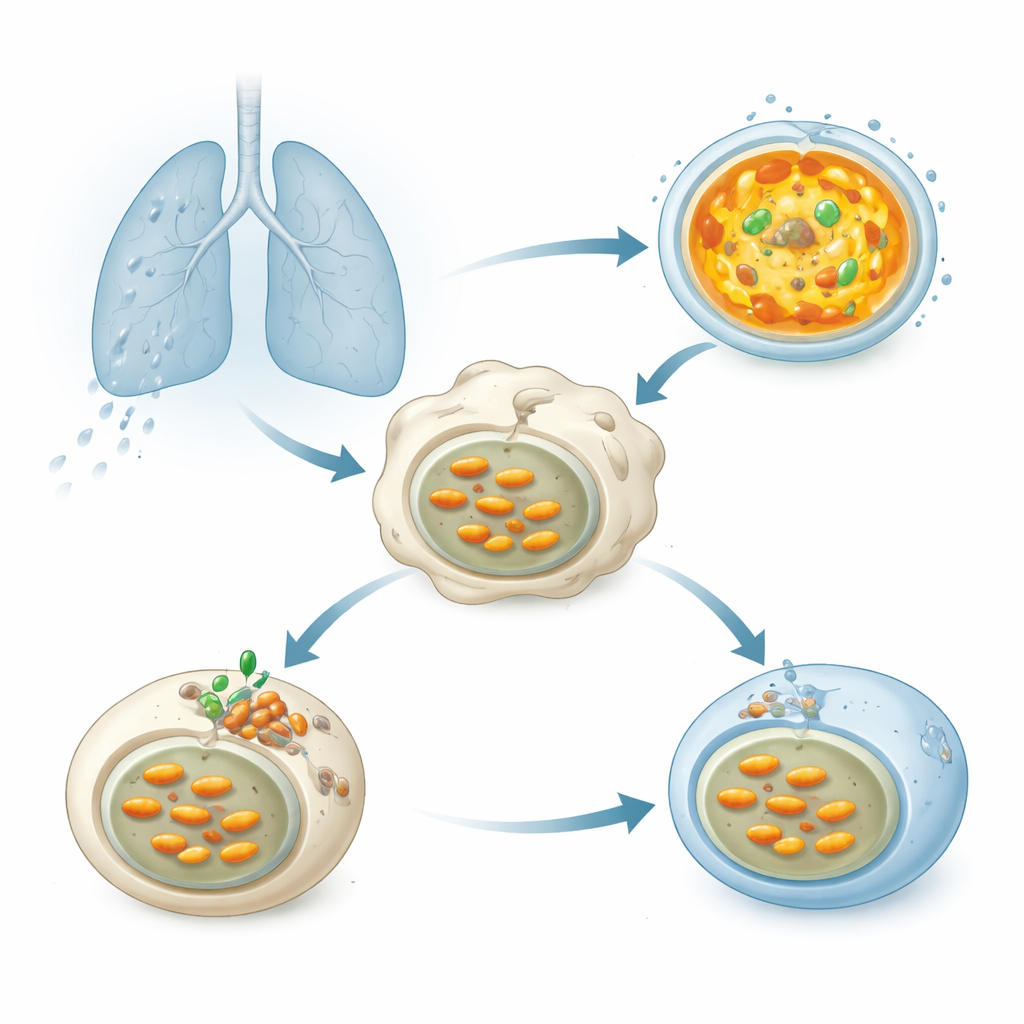
Секретный бактериальный помощник, блокирующий ацидификацию
Исследователи проверили более 200 белков, которые Mtb может выделять, чтобы выяснить, какие из них ослабляют ацидификацию лизосом в человеческих клетках. Один белок выделялся особенно: фермент, названный Chp2 (также известный как Rv1184). Когда клетки экспрессировали Chp2, их лизосомы слабее окрашивались кислотно-чувствительными красителями, что указывает на более высокий, менее враждебный pH. Штаммы Mtb, генетически модифицированные с удалением Chp2, больше не подавляли ацидификацию; в инфицированных макрофагах и у мышей эти мутантные бактерии очищались эффективнее и вызывали меньше повреждений лёгких. Восстановление Chp2 в мутантном штамме возвращало и блок ацидификации, и повышенную бактериальную нагрузку, идентифицируя Chp2 как фактор вирулентности, который помогает Mtb персистировать внутри клеток хозяина.
Субъединица насоса хозяина, выступающая в роли переключателя
Чтобы понять, как Chp2 мешает ацидификации, команда искала компоненты хозяина, с которыми он может связываться. Они обнаружили, что Chp2 напрямую прикрепляется к определённой части V-ATPase — субъединице ATP6V1E1 (сокращённо E1), которая помогает стабилизировать структуру насоса. Увеличение количества E1 в клетках усиливало ацидификацию лизосом и затрудняло выживание Mtb, тогда как снижение E1 имело противоположный эффект. Мыши, у которых оставалась только одна рабочая копия гена E1, имели менее кислые лизосомы, более высокие бактериальные нагрузки в лёгких и более тяжёлые повреждения тканей после инфекции, что показывает, что E1 — важный фактор защиты хозяина против туберкулёза.
Киназная метка на насосе, которая ослабляет кислоту
Авторы затем спросили, не регулируют ли активность E1 химические «метки». Они обнаружили, что добавление фосфатных групп к двум специфическим тирозинам (Tyr56 и Tyr57) на E1 действует как тормоз: имитация фосфорилирования снижала ацидификацию и препятствовала полной сборке V-ATPase, тогда как предотвращение фосфорилирования давало противоположный эффект. Путём скрининга набора ферментов они идентифицировали киназу BMX как белок хозяина, который ставит эту метку. Когда BMX блокировали генетически или малым молекулярным ингибитором, фосфорилирование E1 снижалось, насос собирался более эффективно на мембранах лизосом, лизосомы становились более кислыми, а выживаемость Mtb внутри макрофагов уменьшалась.
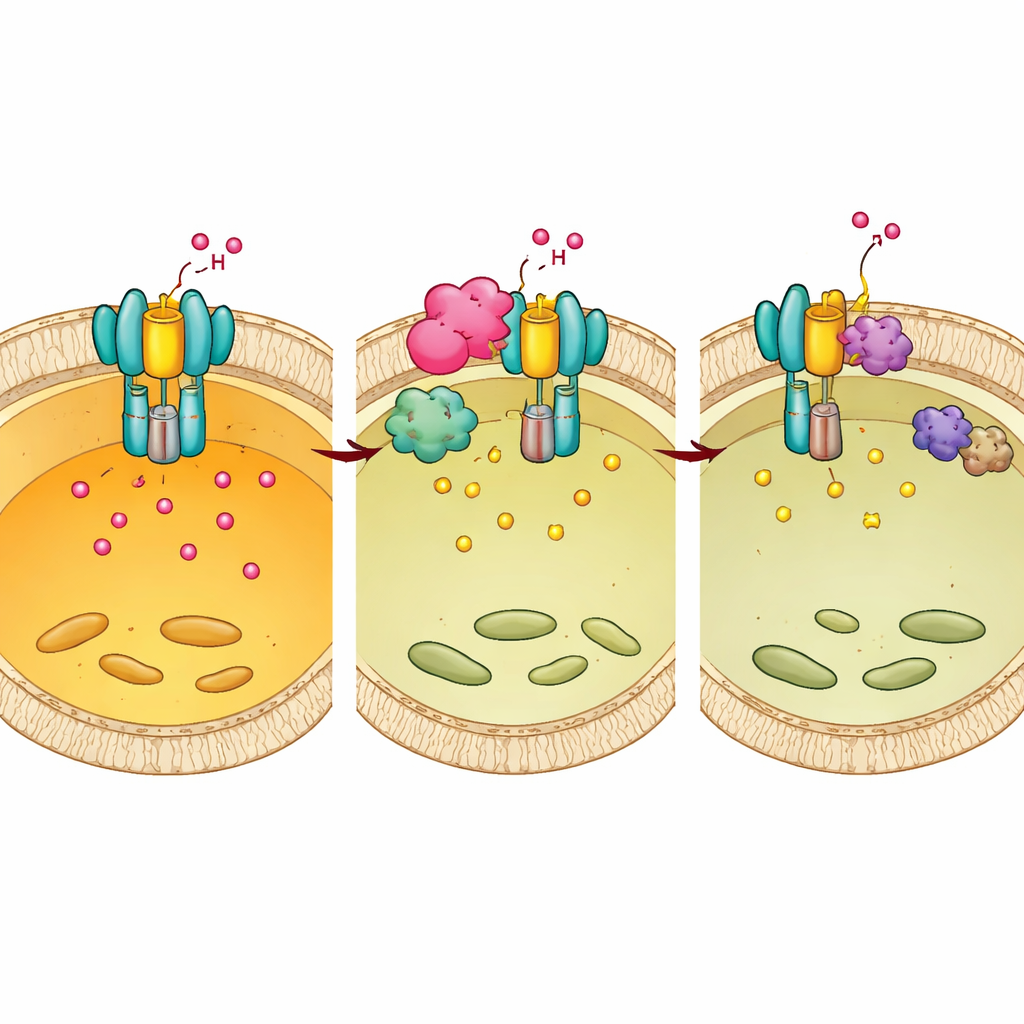
Как Mtb перенастраивает переключатель хозяина в свою пользу
Оказалось, что Chp2 и BMX действуют совместно. Структурные и биохимические эксперименты показали, что Chp2 служит каркасом, который сближает E1 и BMX на поверхности лизосомы, повышая фосфорилирование E1 на Tyr56/57. Это дополнительное помечание нарушает полную сборку насоса, повышает pH лизосом и создаёт более мягкую среду, в которой Mtb может персистировать. Когда BMX ингибировали, преимущество в выживании, обеспечиваемое Chp2, исчезало как в культуре клеток, так и у инфицированных мышей. Важно, что лечение мышей ингибитором BMX после инфекции уменьшало бактериальную нагрузку и патологию лёгких у нормальных животных, но не у мышей с ослабленным E1, что указывает на то, что препарат действует за счёт восстановления эффективной E1-опосредованной ацидификации.
Преобразование трюка патогена в идею для лечения
Проще говоря, это исследование показывает, что бактерии туберкулёза вводят в наши клетки вспомогательный белок, который вмешивается в «кислотный насос» на мусороперерабатывающем агрегате, чуть приглушая его работу, чтобы микробы могли переждать разрушение. Выявив субъединицу насоса, служащую ключевым регулятором (E1), и фермент хозяина, который её модифицирует (BMX), авторы описывают точную мишень для лекарственного вмешательства. Ингибирование BMX у мышей эффективно реактивирует внутриклеточную «кислотную ванну» и улучшает очищение от бактерий. Эти результаты открывают путь к терапиям, направленным на хозяина, которые делают наши собственные клетки более враждебными для Mtb, потенциально дополняя антибиотики и помогая бороться с лекарственно-устойчивым туберкулёзом.
Цитирование: Chen, J., Tang, F., Qin, L. et al. Mycobacterium tuberculosis modulates phosphorylation of host ATP6V1E1 to promote intracellular survival. Nat Commun 17, 2434 (2026). https://doi.org/10.1038/s41467-026-69331-1
Ключевые слова: туберкулез, лизосомы, терапия, направленная на хозяина, Mycobacterium tuberculosis, V-ATPase