Clear Sky Science · ru
Преоптическая сеть нейронов kisspeptin‑nNOS‑GnRH (KiNG) регулирует ритмичность ЛГ через активацию и торможение у мышей
Почему эта история о мозге важна для фертильности
Овуляция и фертильность зависят от небольшой группы клеток мозга, которые выделяют главный гормон пульсами и периодическими всплесками. Когда этот временной рисунок нарушается, репродукция может дать сбой. В этом исследовании показано, как два типа сигнальных молекул в мозге мыши — один включающий активность и другой тихо её гасíšий — работают вместе, формируя эти гормональные ритмы. Понимание этой скрытой схемы управления временем может в итоге помочь объяснить некоторые формы бесплодия и предложить новые пути лечения нарушений репродуктивной системы.
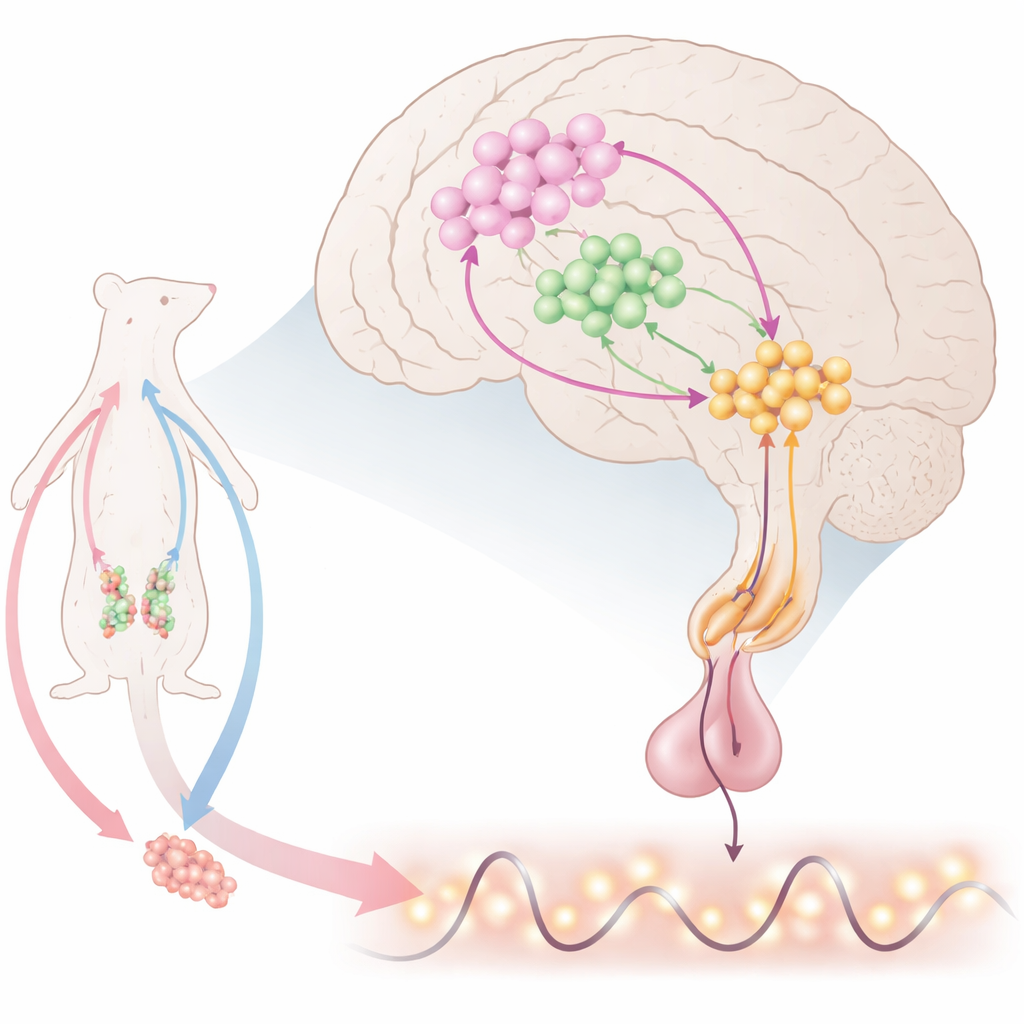
Внутренние часы мозга для воспроизведения
Глубоко в мозге особые нервные клетки выделяют гонадолиберин (GnRH), который заставляет гипофиз выпускать лютеинизирующий гормон (ЛГ) и фолликулостимулирующий гормон. Те, в свою очередь, контролируют яичники и семенники. GnRH не выделяется равномерно; он появляется в виде регулярных пульсов и, у самок, крупного предовуляторного всплеска. Ученым известно, что много сигналов поступают к GnRH‑клеткам, но точное сочетание, порождающее и пульсы, и всплески, оставалось неясным. В этой работе внимание сосредоточено на небольшой области в передней части гипоталамуса, где клетки GnRH соседствуют с двумя другими важными участниками: нейронами, продуцирующими киссептин, который возбуждает GnRH, и нейронами, синтезирующими оксид азота (NO) — газовый сигнал, который может диффундировать на короткие расстояния.
Партнёрство «включи–выключи» между двумя сигналами
Исследователи предлагают трехчастную сеть «KiNG», состоящую из киссептина, NO‑продуцирующих (nNOS) нейронов и GnRH‑клеток. Киссептин — мощный активатор, способный стимулировать выделение GnRH и ЛГ, но постоянная стимуляция на самом деле выключает систему, что указывает на необходимость внутреннего тормоза. С помощью чувствительных молекулярных зондов, генетических инструментов и записей в срезах мозга у мышей команда показывает, что киссептин делает больше, чем просто напрямую возбуждает GnRH‑нейроны. Он также активирует соседние nNOS‑нейроны в преоптической области, особенно в зоне, называемой OV/MePO. Когда уровень киссептина растет, эти nNOS‑клетки генерируют всплески NO, которые запускают образование второго мессенджера cGMP в окружающих клетках, включая сами GnRH‑нейроны. Этот сигнал NO–cGMP ослабляет генерацию импульсов у GnRH, обеспечивая встроенный выключатель для действия киссептина.
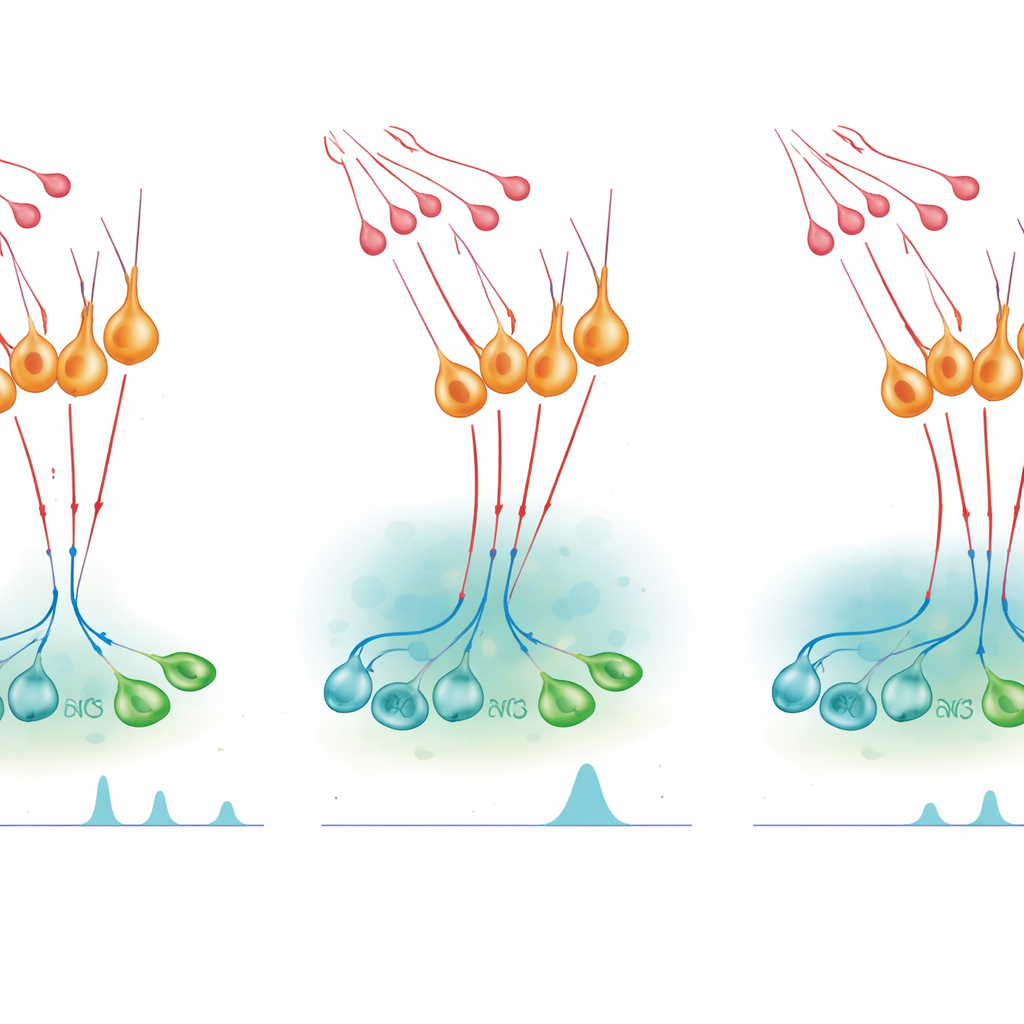
Запуск гормональных всплесков и их коррекция
Чтобы проверить, как эта микросхема влияет на выделение гормонов, команда использовала химогенетические переключатели — сконструированные рецепторы, активируемые иначе инертным препаратом — чтобы включать или выключать nNOS‑нейроны у живых мышей. Искусственная активация nNOS‑клеток в обычно тихую фазу женского цикла была достаточной, чтобы вызвать всплескообразное повышение уровня ЛГ в крови; то же наблюдалось у самцов. Блокирование синтеза NO устраняло этот эффект, показывая, что NO из этих нейронов необходим для всплеска. Тем не менее, когда ученые ингибировали nNOS‑нейроны или снижали их чувствительность к киссептину, инъекция киссептина вызывала чрезмерное и продолжительное повышение ЛГ. Фармакологические препараты, блокирующие синтез NO, вызывали похожее усиливающее действие, тогда как препарат, продлевающий сигналы cGMP, укорачивал ответ на киссептин и снижал последующий выброс ЛГ. В совокупности эти эксперименты указывают, что NO помогает синхронизировать GnRH‑нейроны для создания всплесков и одновременно ограничивает продолжительность их возбуждения под действием киссептина.
Гибкий ритм в течение яичникового цикла
Исследование также показывает, что этот баланс «включи–выключи» меняется в ходе женского цикла. С помощью чувствительного метода обнаружения РНК авторы обнаружили, что напередодне овуляции, когда уровни эстрогена высоки и происходит всплеск ЛГ, большее число nNOS‑нейронов экспрессируют рецептор к киссептину. В более спокойные фазы меньше nNOS‑нейронов реагируют на киссептин, вырабатывая лишь небольшие локальные количества NO, которые мягко сдерживают пульсы GnRH, не останавливая их. В день всплеска более сильные входы киссептина и повышенная экспрессия рецептора резко увеличивают выброс NO, позволяя ему распространяться дальше и кратковременно заглушать многие GnRH‑нейроны одновременно. По мере угасания сигнала NO эти клетки синхронно восстанавливают активность, генерируя большой скоординированный всплеск ЛГ, необходимый для овуляции.
Что это означает для человеческого здоровья
Проще говоря, работа показывает, что тот же сигнал, который запускает GnRH‑нейроны — киссептин — также привлекает замедляющую систему через NO, обеспечивая, чтобы гормональные всплески были сильными, но не бесконтрольными. Сеть KiNG действует как акселератор и тормоз репродуктивного тайминга, настраивая пульсы GnRH в течение большей части цикла и формируя всплеск, вызывающий овуляцию. Поскольку генетические изменения в путях киссептина и NO обнаруживались у людей с нарушениями репродукции, понимание этой тонко сбалансированной схемы может помочь разработать новые подходы к диагностике и лечению бесплодия и родственных состояний.
Цитирование: Delli, V., Moulinier, M., Lazaridou, AM. et al. Preoptic kisspeptin-nNOS-GnRH (KiNG) neuronal network regulates LH rhythmicity through activation-inhibition in mice. Nat Commun 17, 2558 (2026). https://doi.org/10.1038/s41467-026-69316-0
Ключевые слова: репродуктивные гормоны, гипоталамус, киссептин, оксид азота, время овуляции