Clear Sky Science · ru
Лактиляция гистонов повышает экспрессию CXCL1, способствуя инфильтрации нейтрофилов и иммунному уклонению при раке поджелудочной железы
Почему это исследование рака важно
Рак поджелудочной железы — один из самых смертоносных видов рака, отчасти потому, что он часто устойчив к современным иммунотерапиям, которые эффективны при других опухолях. В этом исследовании показано, как опухоли поджелудочной железы перепрограммируют собственный углеводный обмен, чтобы тайно дезактивировать иммунную систему, и как блокирование этого процесса может вновь открыть путь для защитных сил организма — и для уже существующих лекарств — в борьбе с опухолью.
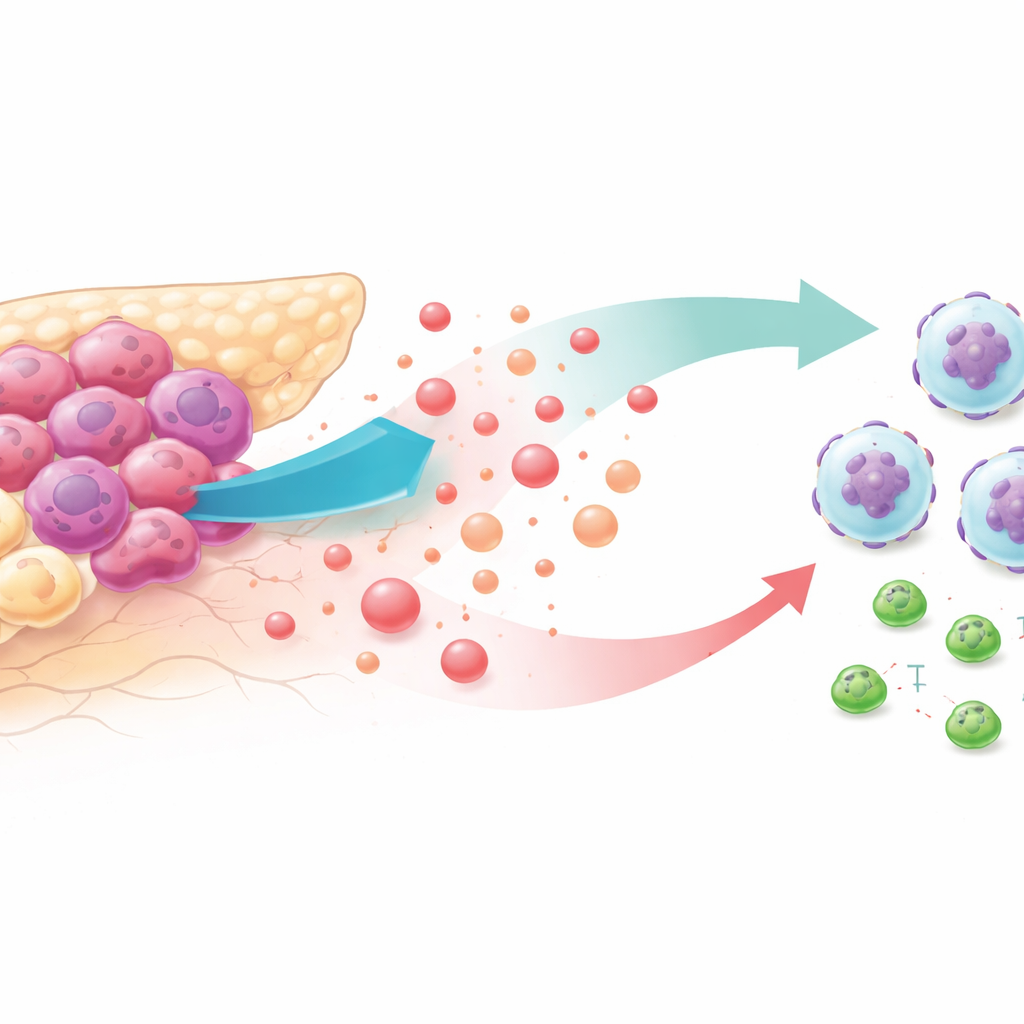
Жадные до сахара опухоли и враждебное окружение
Раковые клетки известны тем, что интенсивно сжигают глюкозу, даже когда кислорода предостаточно. Такой образ жизни с высокой гликолизом наполняет окрестности опухоли лактатом — побочным продуктом, который раньше считали метаболическим отходом. Анализ баз данных опухолей пациентов и мышиных моделей показал, что при наиболее интенсивном гликолизе в опухолях поджелудочной железы наблюдалась значительная инфильтрация нейтрофилов — клеток крови, которые в данном контексте способствуют росту опухоли — и уменьшение числа убивающих рак CD8 T-клеток. У пациентов с таким профилем опухоли выживаемость была ниже, что указывает на тесную связь между изменённым метаболизмом и иммунным уклонением.
Как опухоли используют лактат, чтобы призвать «неправильную» помощь
Чтобы понять, как гликолиз привлекает нейтрофилы, исследователи подавляли гликолиз опухоли с помощью лекарств или генетических приёмов в линиях клеток рака поджелудочной железы и у мышей. При блокировании расщепления сахара опухолевые клетки выделяли значительно меньше химического сигнала CXCL1, а циркулирующие уровни этого сигнала снижались у мышей и в образцах пациентов. В миграционных тестах в лаборатории нейтрофилы активно двигались в сторону среды от высокогликолитических раковых клеток, но не в сторону среды от клеток с подавленным гликолизом — если только исследователи не добавляли обратно очищенный CXCL1. В живых мышах восстановление CXCL1 в опухолях с пониженным гликолизом вновь увеличивало число нейтрофилов и ослабляло противоопухолевый эффект ингибирования гликолиза.
Новый эпигенетический переключатель, управляемый лактатом
Далее исследование сосредоточилось на упаковке ДНК. Наши гены обернуты вокруг белковых «катушек» — гистонов, химические метки на которых действуют как переключатели активности генов. Авторы показывают, что при раке поджелудочной железы лактат, образующийся при гликолизе, добавляет специфическую «лактильную» метку на одно положение гистона, известное как H3K18. Эта модификация, называемая лактиляцией гистона H3K18, была заметно выше в опухолевых тканях по сравнению с нормальной поджелудочной железой. При блокировании гликолиза лактиляция на H3K18 уменьшалась, особенно вблизи регуляторной области гена CXCL1, и выработка CXCL1 падала. Добавление лактата восстанавливало как гистоновую метку, так и экспрессию CXCL1. В образцах пациентов опухоли с более высокой H3K18-лактиляцией также демонстрировали более высокий уровень CXCL1, связывая этот молекулярный знак с проопухолевым иммунным ландшафтом.
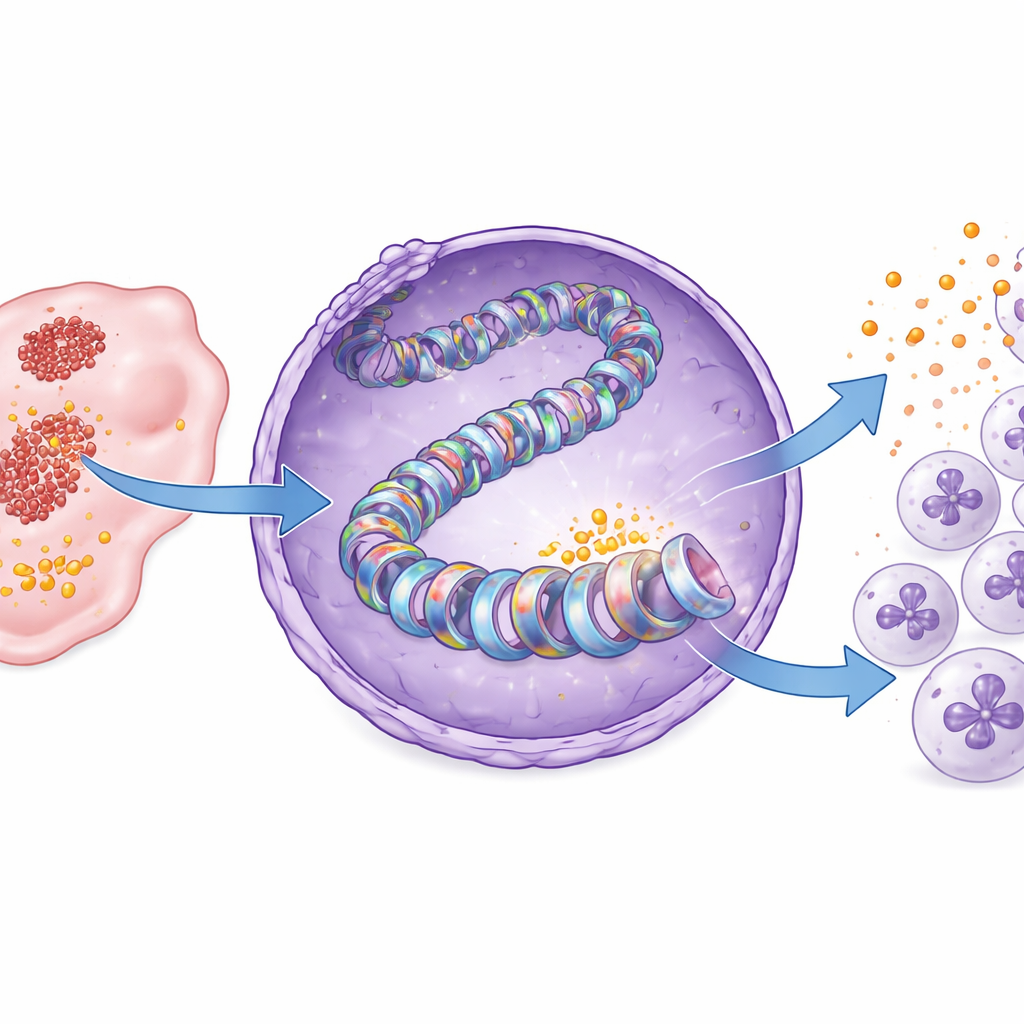
Идентификация фермента и «лекаримой» уязвимости
Гистоновые метки наносятся специализированными ферментами. При скрининге ингибиторов известных модифицирующих белков исследователи выявили фермент PCAF как ключевого «писателя» метки H3K18-лактиляции в раке поджелудочной железы. Структурное моделирование показало, что PCAF способен связывать лактил-КоА — активированную форму лактата, используемую для метки, — а биохимические анализы подтвердили, что очищенный PCAF может напрямую добавлять лактильные группы к гистону H3. Блокирование PCAF малой молекулой бромоспорином снижало H3K18-лактиляцию и выработку CXCL1 в раковых клетках и в мышиных опухолях. В результате в опухоли проникало меньше нейтрофилов, накапливалось больше CD8 T-клеток, и рост опухолей замедлялся, при этом у мышей не наблюдалось явной потери веса или токсичности.
Превращение «холодной» опухоли в «горячую» с помощью комбинационной терапии
Поскольку стандартные препараты блокировки иммунных контрольных точек, такие как антитела против PD-1, показали ограниченный успех при раке поджелудочной железы, команда проверила, может ли разрушение пути лактат–PCAF–CXCL1 сделать эти опухоли более отзывчивыми. В подкожной и ортотопной панкреатической модели у мышей сочетание бромоспорина с анти–PD-1-терапией сокращало опухоли сильнее, чем любое из лечений по отдельности, уменьшало инфильтрацию нейтрофилов, усиливало число активных CD8 T-клеток и значительно продлевало выживаемость. Это указывает на то, что отключение метаболического «сирены» опухоли для нейтрофилов помогает превратить иммунологически «холодную» опухоль в «более тёплую», с которой блокаторы контрольных точек справляются лучше.
Что это значит для будущего лечения
Проще говоря, исследование выявляет цепочку событий: опухоли поджелудочной железы сжигают сахар, выделяют лактат, используют этот лактат, чтобы переключить эпигенетическую маркировку своих белков упаковки ДНК, повышают экспрессию CXCL1 и тем самым привлекают нейтрофилы, которые помогают им укрываться от цитотоксических T-клеток. Прерывание этой цепочки на этапе PCAF с помощью лекарства не только замедляет рост опухолей, но и делает существующую иммунотерапию более эффективной у мышей. Хотя необходимы дополнительные исследования для оценки безопасности и оптимизации подхода у людей, эти результаты подчёркивают перспективную стратегию: перепрограммировать метаболизм и генетические переключатели опухоли, чтобы дать иммунной системе равные шансы в борьбе с раком.
Цитирование: Zhang, P., Ma, J., Wan, Y. et al. Histone lactylation increases CXCL1 expression for neutrophil infiltration and immune escape in pancreatic cancer. Nat Commun 17, 2526 (2026). https://doi.org/10.1038/s41467-026-69311-5
Ключевые слова: рак поджелудочной железы, метаболизм опухоли, лактиляция гистонов, микроокружение опухоли, иммунотерапия рака