Clear Sky Science · ru
Активация STING вызывает цитотоксические и иммунные ответы при менингиомах через пути воспалительной гибели клеток
Включение внутренних «сигналов тревоги» организма против опухолей мозга
Менингиомы — одни из самых частых опухолей мозга: хирургия и радиотерапия часто помогают, но некоторые образования рецидивируют. Эти упорные новообразования вызывают судороги, головные боли и нарушение функций, при этом общепринятых лекарственных методов лечения нет. В этом исследовании изучают способ заставить сами опухолевые клетки и соседние иммунные клетки подать мощный внутренний сигнал тревоги с помощью молекулы, активирующей врожденную систему распознавания опасности, известную как STING. Цель — не только напрямую уничтожить опухолевые клетки, но и пробудить иммунную систему и ослабить жесткий каркас опухоли.
Опухоль, скрытая в тихом иммунном «районе»
Авторы сначала картировали клеточное «окружение» в человеческих менингиомах с помощью одноядерного секвенирования и пространственного визуализации. Они обнаружили, что в этих опухолях много клеток врожденного иммунитета, особенно макрофагов, тогда как классические противоопухолевые Т-клетки и натуральные киллеры (NK) редки и часто истощены. Вокруг опухолевых клеток образована плотная оболочка из коллагена и других матричных белков, формирующая бронезащитную слоистую структуру. Многие макрофаги в этих областях экспрессируют ингибирующие рецепторы, активируемые коллагеном, создавая сильно подавленную среду, где иммунные клетки присутствуют, но их сдерживают, а не активируют против рака.
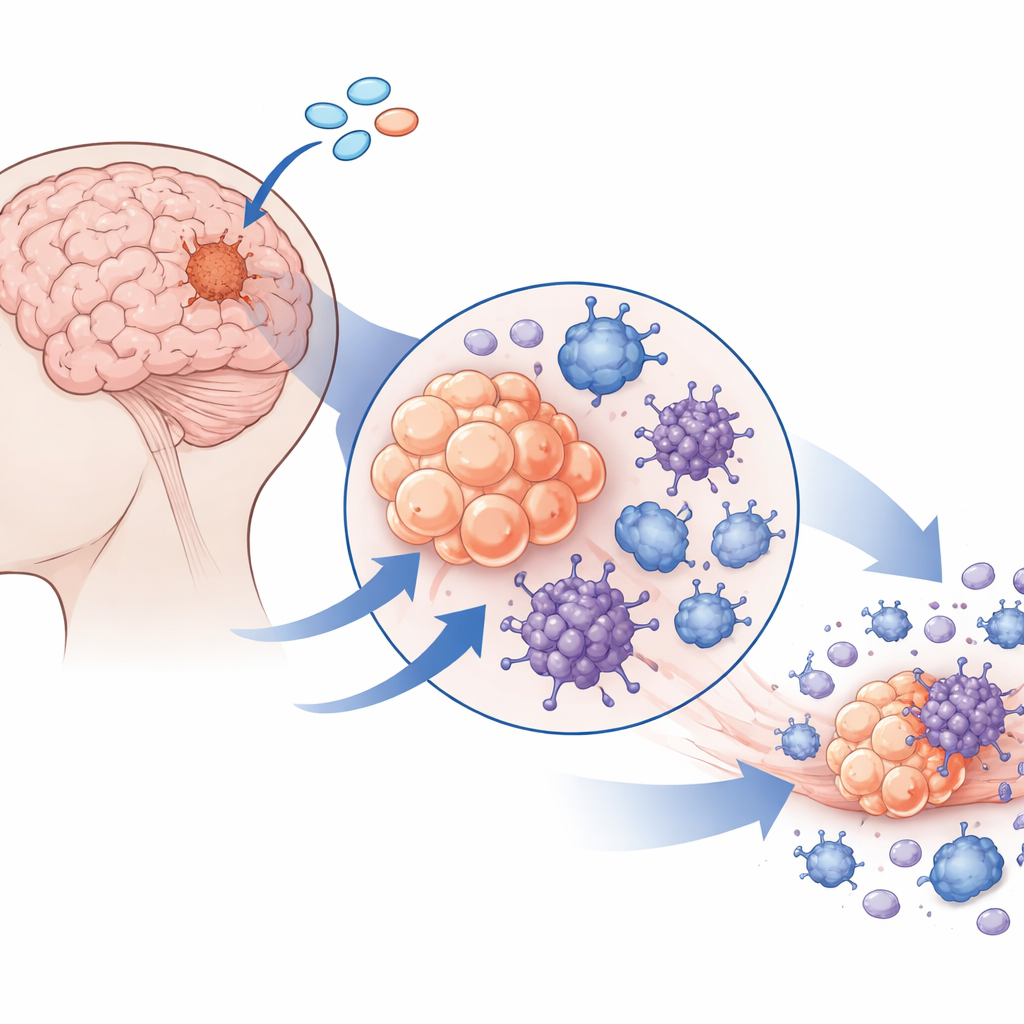
Обнаружение переключателя, который все еще есть у опухолевых клеток
Далее команда искала пути, которые могли бы перевернуть это подавленное состояние в воспаленное, враждебное опухоли. Они сосредоточились на STING — сенсоре, который обычно реагирует на неправильно локализованную ДНК в клетке и вызывает противовирусные и воспалительные ответы. В отличие от многих других опухолей мозга, клетки менингиомы демонстрировали необычно высокий уровень STING. Это объяснялось открытой хроматиновой структурой и низкой метиляцией ДНК в гене STING, что означает эпигенетическую готовность гена к активности. STING был обнаружен не только в опухолевых клетках, но и в клетках сосудов и макрофагах поблизости, что предполагает, что один препарат может одновременно воздействовать на многих ключевых участников опухолевого микроокружения.
Вынужденное «пламя» самоуничтожения опухолевых клеток
Исследователи обработали свежеразрезанные образцы менингиом пациентов сильным агонистом STING под названием 8803. Даже при удаленных иммунных клетках опухолевые клетки умирали, что доказывает прямое действие. Добавляя препараты, селективно блокирующие разные пути гибели клеток, и анализируя активность генов, они показали, что 8803 не вызывает просто тихую апоптозу. Вместо этого он толкал клетки менингиомы в несколько воспалительных форм гибели — пироптоз, некроптоз и ферроптоз — при которых клетки разрываются, а не аккуратно расщепляются. Ключевым этапом была активация и разрезание белка газдермин D, формирующего поры в мембране клетки. Электронная микроскопия показала опухолевые клетки с множеством отверстий в мембране и поврежденными митохондриями; блокирование реактивных форм кислорода снижало гибель, связывая митохондриальный стресс с этой «пламенной» гибелью.
От обломков опухоли к пробуждению иммунитета и размыванию матрицы
Когда опухолевые клетки гибнут так драматично, они выбрасывают «молекулы опасности», которые могут пробудить иммунные клетки. Команда подвергла мышиные макрофаги лизированным клеткам менингиомы и зафиксировала всплеск воспалительных факторов и ферментов, разрушающих коллаген, особенно металлопротеиназы матрицы‑3 (MMP‑3). Работая с мышами, лишенными определенных сигнальных адаптеров, они показали, что толл‑подобные рецепторы, другая система распознавания опасности, критичны для этого ответа, в то время как активация STING с помощью 8803 добавляет собственный уровень стимуляции иммунитета. В моделях менингиомы у мышей прямая инъекция 8803 в опухоли уменьшала или стабилизировала рост, продлевала выживание и превращала участок опухоли из тихой, богатой коллагеном массы в участок, заполненный активными макрофагами, NK‑клетками, T‑клетками и с заметно уменьшенным окрашиванием на коллаген.
Почему этот подход может изменить лечение пациентов
В целом исследование показывает, что менингиомы имеют встроенную уязвимость: их опухолевые клетки сохраняют доступный переключатель STING, который при активации 8803 толкает их в взрывную, воспалительную гибель. Этот процесс одновременно убивает раковые клетки и заливает окружающее пространство сигналами тревоги, привлекающими и энергизирующими иммунные клетки, а также помогает разрушать коллагеновый каркас, способствующий массе опухоли. Поскольку менингиомы обычно локализованы, а не широко метастазируют, и поскольку стандартные опции ограничены при рецидивирующей болезни, локально доставляемый агонист STING, такой как 8803, может предложить новый целенаправленный способ как уменьшать объем опухоли, так и перепрограммировать ее иммунное окружение для длительного контроля.
Цитирование: Youngblood, M.W., Tripathi, S., Najem, H. et al. STING activation induces cytotoxic and immune responses in meningiomas via inflammatory cell death pathways. Nat Commun 17, 2685 (2026). https://doi.org/10.1038/s41467-026-69296-1
Ключевые слова: менингиома, путь STING, иммунотерапия опухолей мозга, воспалительная гибель клеток, опухолевое микроокружение