Clear Sky Science · ru
Генетический фактор острого некротизирующего энцефалита, RANBP2, регулирует воспалительную реакцию при инфекции вирусом гриппа A
Когда грипп вредит мозгу
Большинство людей воспринимают грипп как неделю лихорадки, кашля и постельного режима. Однако в редких случаях, особенно у детей, обычная инфекция гриппа может внезапно перерасти в угрожающее жизни заболевание мозга — острый некротизирующий энцефалит (АНЭ). Семьи и врачи давно подозревали, что гены могут определять, у кого развивается это катастрофическое осложнение. В этом исследовании показано, как один белок‑«страж» клеточных ворот, RANBP2, обычно сдерживает вирус гриппа и предотвращает выход воспалительной реакции организма из под контроля.
Редкое, но разрушительное осложнение гриппа
АНЭ возникает внезапно после лихорадочного заболевания, часто вызванного гриппом, и может быстро привести к судорогам, коме и длительному неврологическому ущербу. Примерно половина известных случаев АНЭ в мире связана с вирусом гриппа A, в частности штаммом H1N1. Дети, наследующие определённые изменения в гене RANBP2, подвергаются значительно более высокому риску — это состояние называют ANE1. До настоящего времени учёные не понимали, что именно делает этот белок при инфекции гриппа и почему его изменение усиливает воспаление в мозге.
Клеточные ворота и вирусные геномы
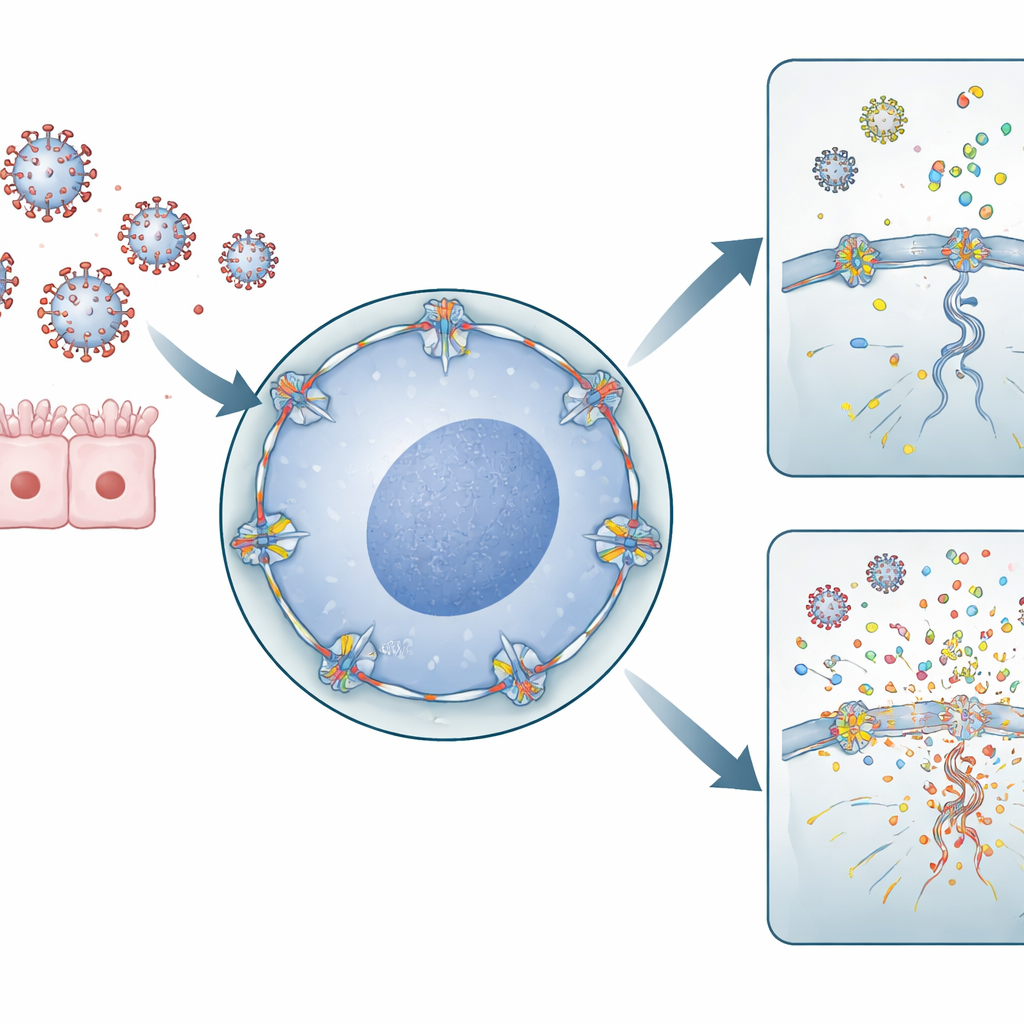
Вирус гриппа A ведёт себя необычно для РНК‑вируса: ему необходимо проникать в ядро клетки, чтобы копировать свой генетический материал. Для этого он проходит через ядерные поры — крупные ворота в ядерной оболочке, контролирующие трафик между ядром и цитоплазмой. RANBP2 является важным компонентом на внешней стороне этих пор. Авторы работы использовали клетки человеческого происхождения из лёгких и иммунные клетки, чтобы снизить уровни RANBP2 или ввести связанную с АНЭ мутацию. Они обнаружили, что при отсутствии или неправильном расположении RANBP2 геномы гриппа интенсивнее копировались в ядре, а вирусные сегменты генетического материала экспортировались в цитоплазму в несбалансированном виде. Удивительно, но избыток вирусной РНК не приводил к большему числу инфекционных частиц, однако изменялось место и способ накопления вирусного материала внутри клетки.
Когда вирусный мусор подкармливает систему тревоги
Иммунная система опирается на молекулярные сенсоры, которые обнаруживают брошенные в цитоплазме фрагменты вирусной РНК как сигналы опасности. Команда показала, что в клетках без нормального RANBP2 в цитоплазме накапливались дополнительные вирусные РНК‑сегменты, формируя именно те структуры, на которые настроены эти сенсоры. В клетках лёгочного происхождения это вызывало повышенное образование провоспалительных молекул, таких как IL‑6 и IL‑1β. В первичных человеческих макрофагах — передовых иммунных клетках из донорской крови — потеря RANBP2 привела к заметному всплеску провоспалительных хемокинов, включая CXCL8, CXCL10, CCL2, CCL3 и CCL4. Эти химические посланники привлекают и активируют дополнительные иммунные клетки, усиливая общую реакцию на инфекцию.
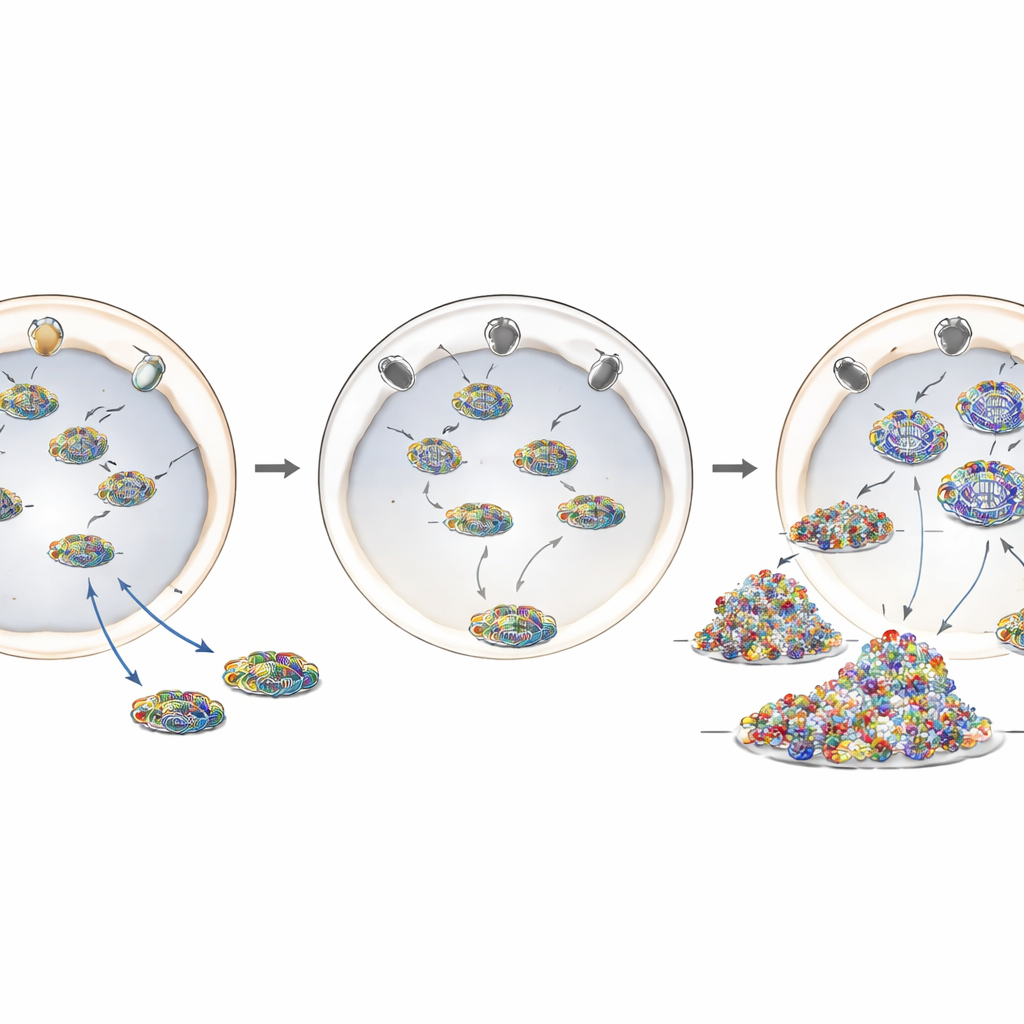
Мутация болезни, неправильно размещающая стража
Чтобы ближе смоделировать ANE1, исследователи использовали редактирование генома CRISPR‑Cas9, чтобы ввести наиболее распространённое связанное с заболеванием изменение T585M в человеческий ген RANBP2. В этих отредактированных клетках уровни белка RANBP2 в целом оставались близкими к нормальным, но его локализация нарушалась: вместо того чтобы образовывать яркий ободок вокруг ядерной оболочки, большая часть белка смещалась в цитоплазму. Клетки с этой мутацией, независимо от того была она в одной или обеих копиях гена, вели себя похоже на клетки с истощённым RANBP2. Они поддерживали повышенную репликацию генома гриппа, демонстрировали больше вирусного материала в цитоплазме и вызывали усиленную воспалительную реакцию после инфекции. Это указывает на то, что правильное размещение RANBP2 в ядерных порах — а не только его общее количество — критично для его защитной функции.
Почему это важно для детей из группы риска
В совокупности результаты рисуют RANBP2 как клеточного стража, тонко регулирующего перемещение генетического материала гриппа в ядро и из него. Когда RANBP2 отсутствует или неправильно локализован, вирусная РНК пере реплицируется и экспортируется хаотично, засоряя цитоплазму молекулярным мусором, который сильно усиливает иммунную сигнализацию. Для большинства тканей это может означать более тяжёлое, но переносимое течение гриппа. У уязвимых детей с ANE1 такая неконтролируемая воспалительная реакция — особенно если она достигает мозга — может помочь объяснить внезапное, тяжёлое неврологическое повреждение, наблюдаемое после, казалось бы, обычных инфекций. Понимание этого пути может помочь в разработке стратегий ранней идентификации пациентов в группе риска и в подборе противовоспалительных подходов до того, как иммунный ответ превратится из защитного в разрушительный.
Цитирование: Desgraupes, S., Decorsière, A., Perrin, S. et al. The genetic driver of Acute Necrotizing Encephalopathy, RANBP2, regulates the inflammatory response to Influenza A virus infection. Nat Commun 17, 2427 (2026). https://doi.org/10.1038/s41467-026-69288-1
Ключевые слова: грипп, острый некротизирующий энцефалит, RANBP2, гипервоспаление, ядерная пора