Clear Sky Science · ru
Сборка асимметричных 4‑алкил‑бутенолидов, катализируемая трифункциональным флавоэнзимом, в биосинтезе avenolide
Почему маленькие кольца у бактерий важны для нас
Многие жизненно важные лекарства — от препаратов против паразитов до средств защиты растений — зависят от небольшой химической структуры, называемой бутенолидом. В наши дни эти кольца в основном синтезируют из углеводородного сырья в многоступенчатых промышленных процессах, которые требуют энергии и создают отходы. В этом исследовании показано, как почвенные бактерии собирают одно такое кольцо — гормон avenolide, который запускает производство широко используемых антипаразитных препаратов авермектинов. Понимание этого природного пути указывает на более чистые и дешёвые способы получения полезных химикатов и может помочь в открытии новых антибиотиков.
Особое кольцо в основе многих лекарств
Бутенолиды — компактные пятичленные кольца, которые ценят химики за их реактивность и широкое распространение в природных продуктах и современных лекарствах. Они участвуют в формировании молекул с антираковыми, противогрибковыми, противовоспалительными и инсектицидными свойствами, применяемыми в медицине и сельском хозяйстве. Однако традиционные синтетические методы получения этих колец обычно требуют нескольких строго контролируемых этапов, дорогих катализаторов и нефтехимического сырья. Такое сочетание удорожает процесс и увеличивает экологический след, что заставляет исследователей искать биологические сокращения путей, которые природа уже отточила.
Бактериальный гормон, включающий производство блокбастера
В почвенной бактерии Streptomyces avermitilis молекула с бутенолидом — avenolide — действует как микрогормон. При крайне низких концентрациях она связывается с регуляторным белком и снимает молекулярный «тормоз» с генов, ответственных за синтез авермектинов — мощных средств, парализующих паразитических червей и некоторых насекомых. Предыдущие генетические исследования намекали, что два фермента, названные SavA и SavB, собирают avenolide, но конкретные шаги были неизвестны. Авторы перенесли соответствующие гены в более удобный для работы родственный штамм, Streptomyces albidoflavus, и оптимизировали условия культивирования, пока модифицированная штамм не стал продуцировать миллиграммовые количества чистого avenolide — достаточно, чтобы подробно расшифровать путь. 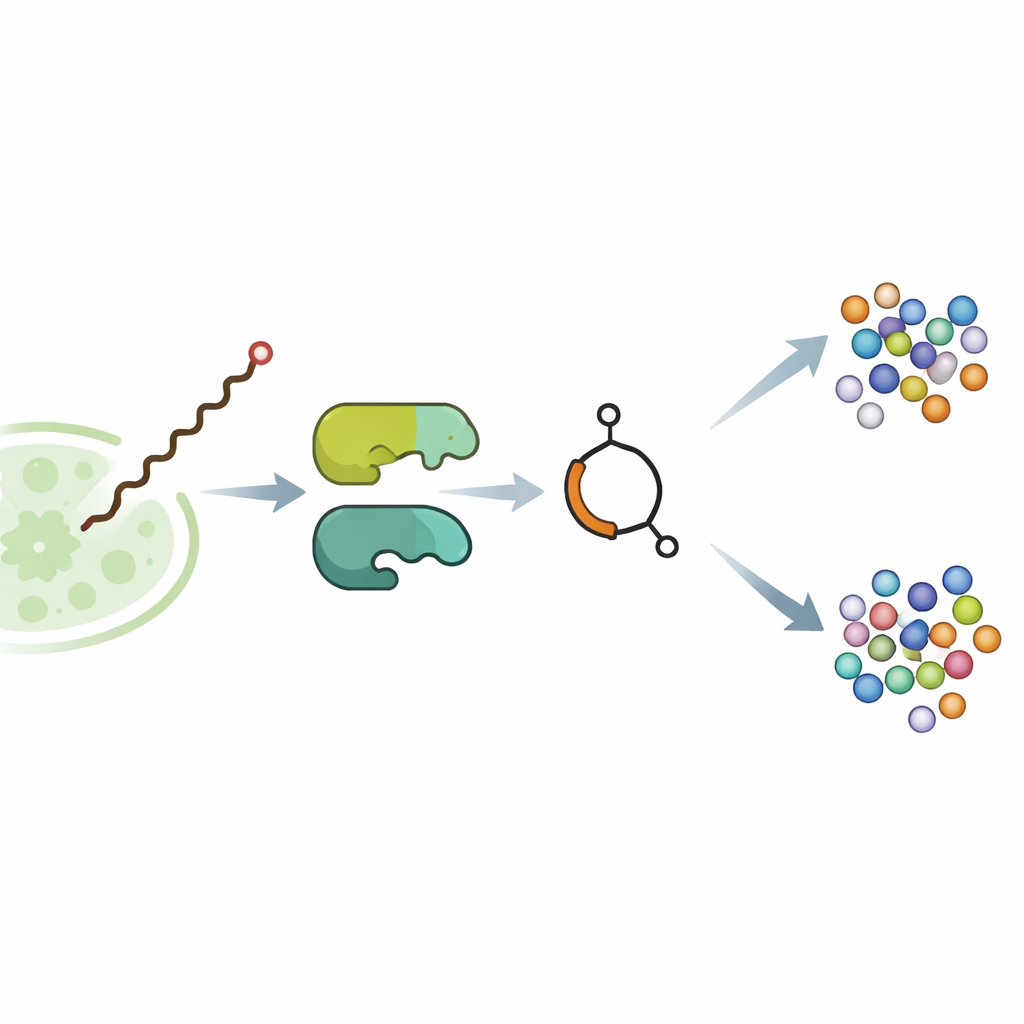
Один фермент, выполняющий три последовательные задачи
Ключевой сюрприз работы — SavA, флавинсодержащий фермент, который осуществляет три различных химических превращения с исходным звеном, похожим на жирную кислоту, взятым из обычного клеточного метаболизма. В реакциях в пробирке с тщательно синтезированными имитаторами субстратов исследователи показали, что SavA сначала отнимает атомы водорода для введения двойной связи, затем вводит кислородсодержащее звено в определённую позицию и, наконец, способствует замыканию цепи в бутенолидное кольцо. Эксперименты с изотопами, использующие молекулярный кислород, обогащённый более тяжёлым изотопом, подтвердили, что кислород в кольце происходит прямо из воздуха. Структурное моделирование и направленные мутации указали на одну аминокислоту в роли основания, запускающего реакцию, и показали, как связанный флавиновый кофактор циклирует между окислённой и восстановленной формами, не расходуясь.
Финиширующий фермент, уточняющий боковую цепь
После того как SavA создал хиральный бутенолидный скелет, SavB — фермент семейства цитохромов P450 — вступает в игру, чтобы «украшать» присоединённую углеродную цепь. В присутствии своих редоксных партнёров и обычного клеточного кофактора SavB выполняет точную серию окислений в двух соседних атомах углерода. Временной анализ выявил два промежуточных молекулы: сначала моно‑гидроксилированный продукт, затем кетонная форма, прежде чем появляется полностью функциональный avenolide. ЯМР‑измерения подтвердили позиции и трёхмерное расположение введённых групп. Работа показывает, что SavB вводит эти кислородные атомы в определённом порядке и с жёстким контролем ориентации, что важно для биологической активности гормона. 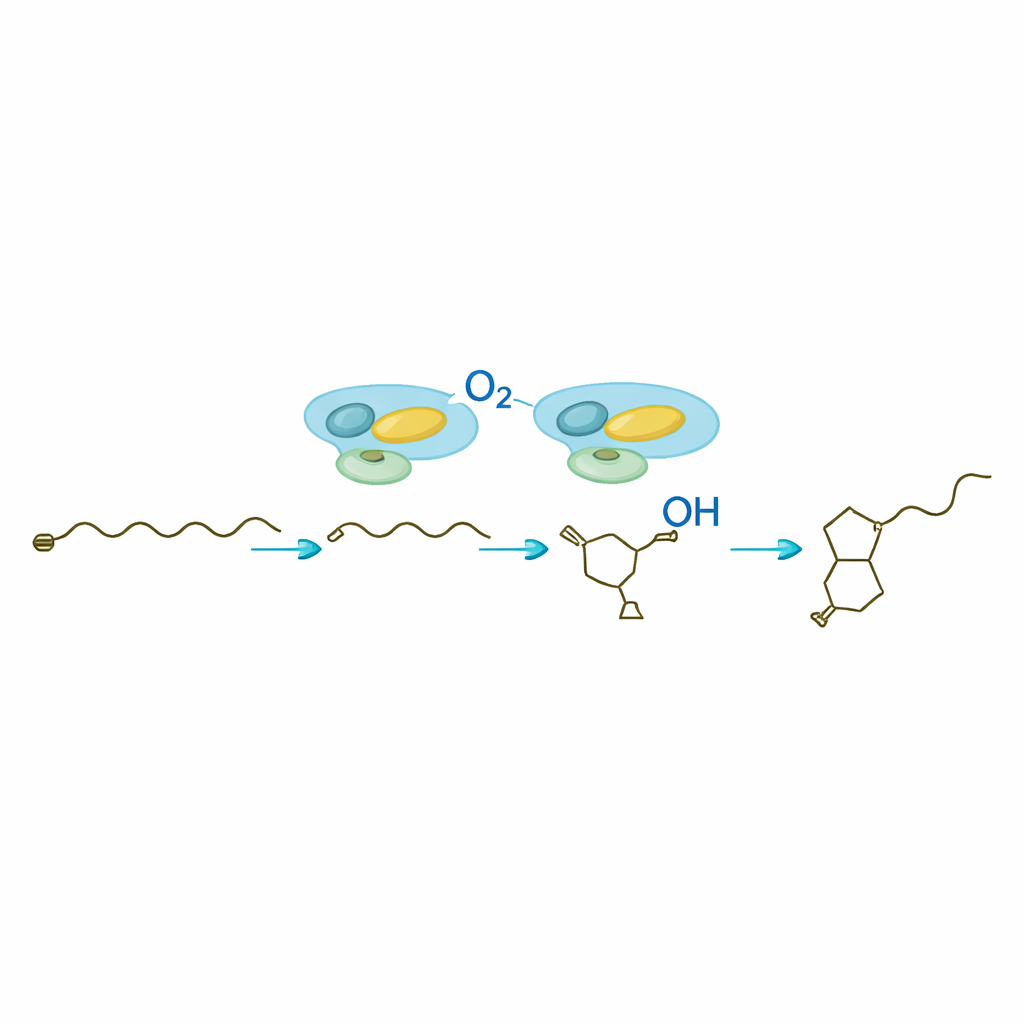
Уроки «зелёной химии» от бактериальных ферментов
Вместе SavA и SavB превращают обычный блок, происходящий от жирных кислот, в точно настроенную сигнальную молекулу, используя только кислород из воздуха и стандартные клеточные помощники. В отличие от многих промышленных процессов, SavA не требует дополнительных восстановителей или расходных реагентов: его флавиновый кофактор просто перекачивает электроны, в то время как сам субстрат обеспечивает движущую силу реакции. Авторы выделяют SavA как новый тип многозадачного флавоэнзима с большим потенциалом в качестве биокатализатора для устойчивого производства бутенолидов и родственных структур. В практическом плане использование или инженерия таких ферментов теоретически позволят фабрикам — или генетически модифицированным микроорганизмам — когда‑нибудь производить важные фрагменты лекарств и агрохимикатов из возобновляемого сырья при мягких условиях, сокращая расходы и экологический след.
Цитирование: Li, W., Zhao, J., Zeng, W. et al. Trifunctional flavoenzyme-catalyzed asymmetric 4-alkyl-butenolide assembly in avenolide biosynthesis. Nat Commun 17, 2459 (2026). https://doi.org/10.1038/s41467-026-69265-8
Ключевые слова: биосинтез бутенолидов, флавоэнзим SavA, гормон avenolide, биокатализ, сигнализация Streptomyces