Clear Sky Science · ru
Деградеры белка капсида вируса денге проявляют отличную фармакологию по сравнению с ингибиторами капсида
Обратить оболочку вируса против него самого
Лихорадка денге заражает сотни миллионов людей каждый год, однако у врачей по‑прежнему нет надёжных противовирусных препаратов для её лечения. В этом исследовании рассматривается новый способ обезвредить вирус денге — уничтожать один из его ключевых строительных компонентов внутри инфицированных клеток, а не просто пытаться блокировать его функцию. Работа показывает, что тщательно сконструированные молекулы могут метить важный вирусный белок для утилизации собственной системой «утилизации» клетки, снижая продукцию вируса и ослабляя его способность скрываться от защитных механизмов иммунной системы.
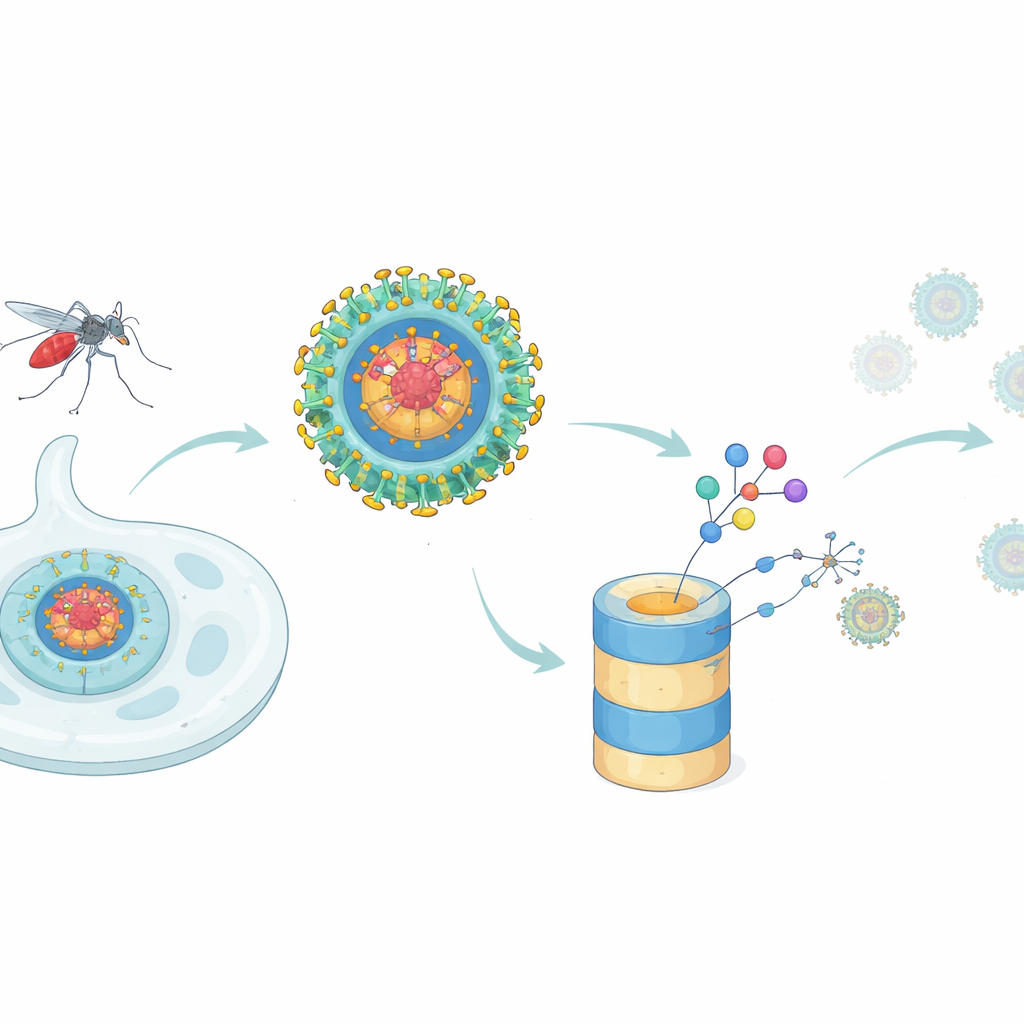
Новая тактика для остановки денге
Большинство противовирусных препаратов действуют как пробки в механизме: они садятся на одну функциональную позицию вирусного белка и пытаются её заблокировать. Такой подход испытывает трудности, когда один вирусный белок выполняет множество разных задач или когда небольшие мутации ослабляют связывание препарата. Белок капсида денге — яркий пример. Он формирует сердцевинную оболочку, которая упаковывает генетический материал вируса в новые частицы, но также взаимодействует с множеством белков хозяина и подавляет интерфероновый ответ — передовую систему оповещения против вирусов. Авторы поставили вопрос, может ли более современная концепция лекарств — таргетированная деградация белков — пойти дальше классических ингибиторов, фактически удаляя белок капсида из инфицированных клеток.
Создание молекулярного «охотника за наградой»
Чтобы создать такой деградер, исследователи использовали ST148 — известную малую молекулу, которая связывается с капсидом денге и мешает сборке новых вирусных частиц. Они химически связали ST148 со второй модулем, который рекрутирует человеческий ферментный комплекс, отвечающий за пометку белков для разрушения. Получившиеся химерные молекулы, называемые PROTAC, устроены так, чтобы одной частью захватывать капсид, а другой — комплекс E3‑лигазы, сближая их для пометки капсида убиквитином и направления в протеасому — основной «шредер» белков в клетке. Тестируя разные длины линкера и группы, рекрутирующие лигазу, они выявили один выдающийся компаунд, обозначенный RPG‑01‑132, который надёжно снижал уровни капсида в инфицированных клетках в зависимости от формы лигазы CRBN и от нормальной функции протеасомы.
Остановка производства вируса и подавления иммунитета
Обладая рабочим деградером, команда изучила, как он влияет на инфекцию денге. В клетках печени, инфицированных вирусом денге, RPG‑01‑132 вызывал резкое снижение числа инфекционных частиц, выпускаемых из клетки, при концентрациях, при которых он лишь частично уменьшал общий уровень капсида. Важно, что другие вирусные белки и вирусная РНК оставались без изменений, что показывает: соединение не отравляет общую репликацию, а действует специфически через потерю капсида. Электронная микроскопия дала визуальное подтверждение: клетки, обработанные исходным ингибитором ST148, накапливали стопки частично сформированных вирусных частиц в эндоплазматическом ретикулуме, что согласуется с блоком сборки, тогда как в клетках, обработанных деградером, видимых вирионов практически не было. Деградер также ослаблял способность капсида подавлять сигналинг интерферона‑β в репортерной системе, что указывает на то, что неструктурная роль капсида в подрыве врождённого иммунитета может быть обращена посредством его деградации.
Превосходство над вирусным разнообразием и лекарственной устойчивостью
Вирус денге существует в четырёх основных серотипах, которые по‑разному реагируют на ингибиторы, нацеленные на капсид, а устойчивость может появляться из‑за одиночных мутаций. Авторы сравнили действие деграпера и ST148 на репрезентативных штаммах всех четырёх серотипов и на варианте вируса с мутацией (S34L в капсиде), ранее показавшей, что ST148 становится неэффективен. Как и ожидалось, ST148 лучше всего работал на одном серотипе и терял активность против резистентного мутанта. RPG‑01‑132, напротив, показал схожую противовирусную активность во всех серотипах и сохранил активность против мутанта S34L, при этом по‑прежнему действуя через тот же путь деградации, зависимый от CRBN. Это иллюстрирует ключевое преимущество «событий‑ориентированной» фармакологии: деградеру не нужно постоянно крепко держаться за каждую молекулу капсида, достаточно инициировать достаточное число событий деградации, чтобы нарушить равновесие.
Что это значит для будущих методов лечения денге
Это исследование демонстрирует, что на белок капсида денге можно воздействовать не только как на структурный компонент вируса, но и как на съёмный узел, который поддерживает несколько этапов инфекции и подавления иммунитета. Превратив традиционный ингибитор в деградер, исследователи получили соединение, которое блокирует производство вируса, снимает часть подавления врождённого иммунитета и остаётся эффективным против разных штаммов и против известной мутации, дающей устойчивость. Сам RPG‑01‑132 требует оптимизации — лучшего проникновения в клетки, более сильной активности в модельных животных и тщательной проверки безопасности — но он представляет убедительное доказательство концепции. В более широком плане работа указывает, что захват клеточной системы утилизации может открыть новые пути для создания противовирусных препаратов, которым вирусам труднее уклоняться, и которые способны нейтрализовать белки с множественными функциями внутри инфицированных клеток.
Цитирование: Chakravarty, A., Wang, LN., Golden, R.P. et al. Degraders of the dengue virus capsid protein exhibit differentiated pharmacology relative to capsid inhibitors. Nat Commun 17, 2594 (2026). https://doi.org/10.1038/s41467-026-69263-w
Ключевые слова: вирус денге, белок капсида, таргетированная деградация белков, проектирование противовирусных препаратов, PROTACs