Clear Sky Science · ru
Кооперативная активация анионов в центре кобальта через ионную пару и дизайн лиганда
Почему важны крошечные партнёры вокруг металлов
Химики часто сосредотачиваются на главном «актере» в реакции — атоме металла, который способствует разрыву и образованию связей. Но в этой работе показано, что тихие партнёры, находящиеся поблизости и невидимые невооружённым глазом, могут полностью изменить роль металла. Тщательно сформировав пространство вокруг атома кобальта, авторы демонстрируют, как два почти взаимозаменяемых аниона, которые обычно считают пассивными свидетелями в химии и батареях, могут приводить к резко разным исходам. 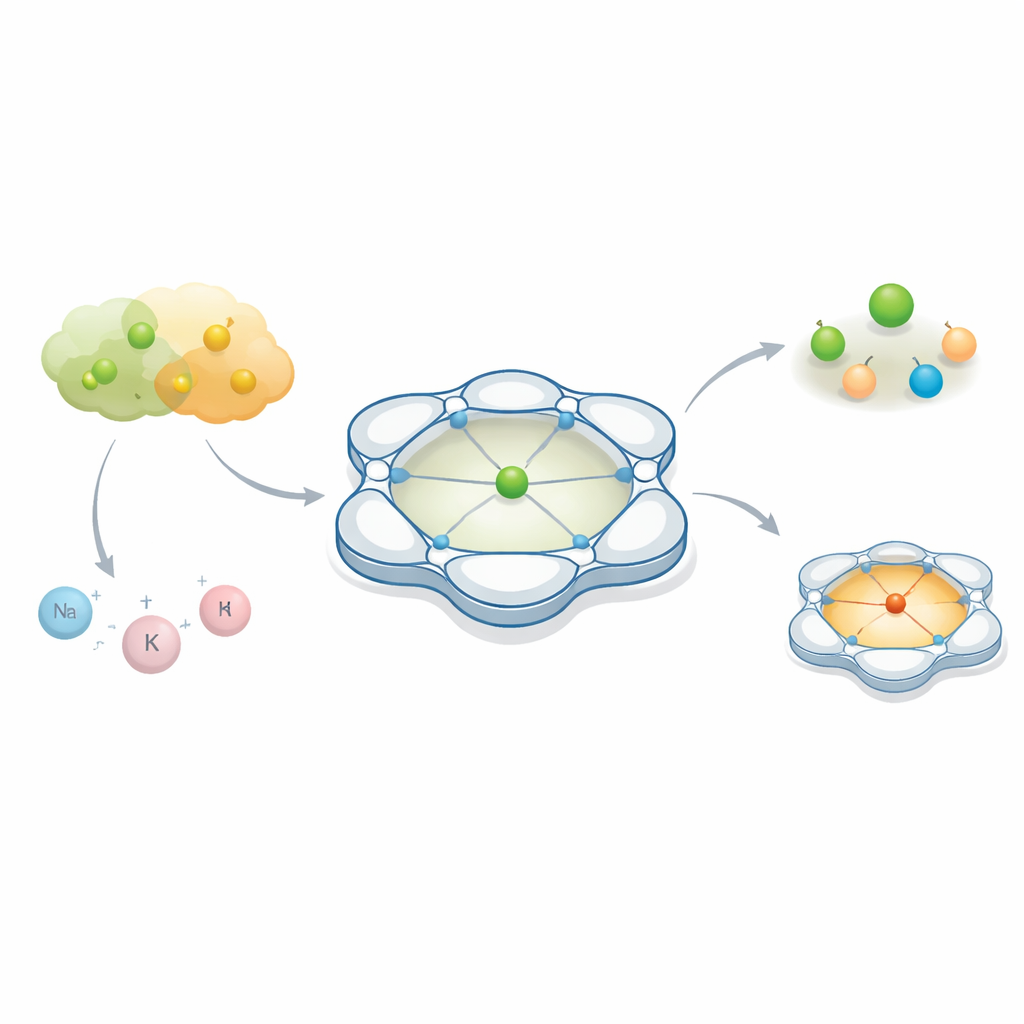
Создание подогнанной полости вокруг кобальта
Исследователи спроектировали органическую каркасную «клетку» под названием Py4Im, которая плотно охватывает ион кобальта. Эта рамочная молекула состоит из нескольких связанных пиридиновых колец и имидазолидинового фрагмента, вместе образующих жёсткую, чашеобразную полость с одной N–H группой. Эта маленькая полость является «протической», то есть способна образовывать водородные связи, и направлена в определённую сторону, подобно крошечной причальной камере для входящих анионов. Когда кобальт собирают с этим лигандом, получается семейство положительно заряженных комплексов, чья общая форма и внутренний карман остаются постоянными, в то время как контраион — отрицательно заряженный партнёр — можно заменять. Это делает систему идеальной платформой для изучения поведения разных анионов в одинаковой контролируемой среде.
Два похожих аниона — два очень разных поведения
Команда сравнила два широко используемых аниона, тетрафторборат (BF4−) и гексафторфосфат (PF6−), которые часто рассматривают как слабо координирующие анионы. Их предпочитают за то, что они обычно держатся на расстоянии от центров металлов, стабилизируя сильно заряженные виды, не вмешиваясь напрямую. Удивительно, но внутри полости Py4Im они ведут себя по‑разному. В мягких условиях PF6− отдаёт ион фтора кобальту, разрывая прочную связь P–F и образуя чётко определённый комплекс кобальт–фторид. В отличие от этого, BF4−, который обычно считают более «хрупким», отказывается отдавать фторид в тех же условиях. Вместо этого он располагается в устойчивой конфигурации, связанной с центром кобальта, не завершая этапа разрыва связи.
Наблюдая, как ионы спариваются и перемещаются
Чтобы понять эти контрастные поведения, авторы использовали сочетание высокоразрешающей ЯМР‑спектроскопии и квантово‑химических расчётов. Эксперименты по диффузионной ЯМР измеряли скорость движения положительных и отрицательных видов в растворе, что даёт представление о степени их спаривания. Эти измерения показали, что BF4− формирует более тесную и более долговременную ионную пару с комплексом кобальта, чем PF6−. Полость Py4Im располагает анион прямо под имидазолидиновым кольцом, где водородные связи от N–H и соседних C–H групп удерживают его на месте. Расчёты подтвердили, что такое более сильное и направленное спаривание с BF4− стабилизирует начальное состояние настолько, что разрыв связи B–F становится немного невыгодным, даже несмотря на то, что сама B–F связь по природе слабее, чем P–F в PF6−. PF6−, спариваясь менее плотно, может подойти, передать фторид кобальту и уйти как PF5, что приводит к образованию фторидсодержащего комплекса кобальта, термодинамически доступного. 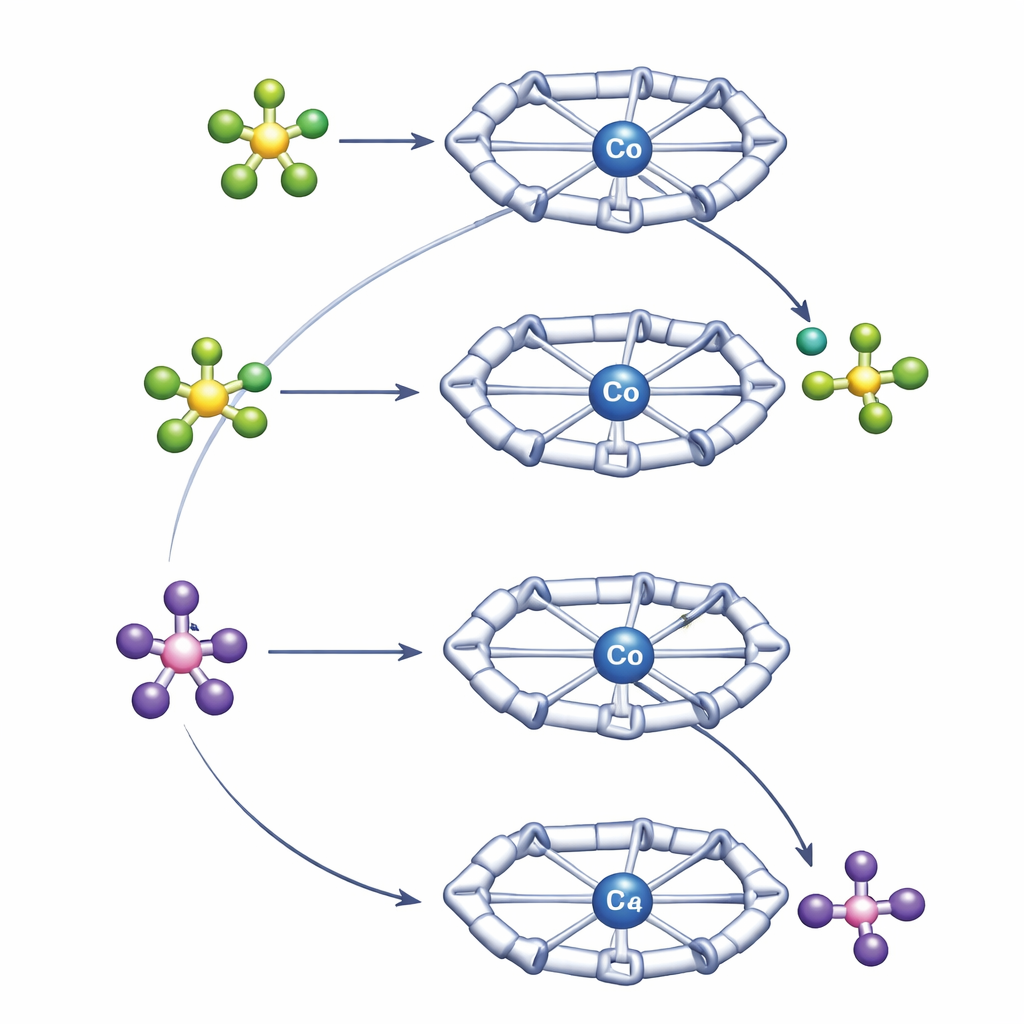
Преобразование связанного фторида в полезный инструмент
Оказавшись сформированным, комплекс кобальт–фторид не является тупиковой ветвью. Авторы показывают, что он ведёт себя как нуклеофильный источник фторида — проще говоря, может доставлять фторид к положительно заряженным или электронодефицитным партнёрам. В растворе этот вид чисто передаёт фторид реактивным углеродным центрам, кремнию в хлорсилиланах и ацилированным хлоридам, генерируя органические фториды, в то время как комплекс кобальта возвращается в хлоридную форму или связывает новый партнёр. В изящном приёме команда также демонстрирует, что BF4− можно побудить отдать фторид при наличии отдельной базы, которая «улавливает» оставшийся фрагмент BF3. Это превращает в противном случае неохотный путь BF4− в путь, который также даёт тот же продукт — комплекс кобальт–фторид.
Что это значит для проектирования более умных катализаторов
Для неспециалиста ключевое послание состоит в том, что ионы, ранее рассматриваемые как инертные фоновые соли, на самом деле могут активно направлять химические реакции. С помощью формовки точной полости вокруг металлического центра и контроля степени ионного спаривания с анионами авторы изменили ожидаемую реактивность двух почти идентичных видов. PF6−, обычно считающийся очень стабильным, становится более лёгким источником фторида, тогда как BF4− фиксируется более сильным спариванием, если систему не поддержать дополнительно. Эта работа даёт шаблон для совместного использования дизайна лиганда и выбора контраионов с целью настройки реактивности металлического комплекса — идея, которая может повлиять на области от гомогенного катализа до проектирования электролитов для передовых батарей, где «молчаливые партнёры» в растворе могут быть вовсе не пассивными.
Цитирование: Tarifa, L., Cano-Asensio, J., López, J.A. et al. Cooperative anion activation at a cobalt center through ion pairing and ligand design. Nat Commun 17, 2469 (2026). https://doi.org/10.1038/s41467-026-69257-8
Ключевые слова: комплексы кобальта, слабо координирующие анионы, перенос фторида, ионное спаривание, дизайн лиганда