Clear Sky Science · ru
Гепатоциты функционально перепрограммируются клетками колоректального рака с высоким уровнем KIAA1199 и способствуют накоплению про‑метастатических нейтрофилов Egr1+
Когда рак толстой кишки нацеливается на печень
Большинство людей представляет себе распространение рака как просто отрывающиеся и уносимые в другие органы бродячие клетки. Это исследование рассказывает более тревожную историю: опухоли колоректального тракта способны тихо перенастраивать печень задолго до появления самих раковых клеток, создавая гостеприимную «почву», в которой будущие опухоли легко укореняются. Понимание этой скрытой фазы подготовки может открыть путь к методам лечения, которые остановят печёночные метастазы — главную причину смерти при колоректальном раке — прежде, чем они начнутся.
Незаметная подготовка до появления опухолей
Колоректальный рак часто метастазирует в печень, но агрессивно это делают не все опухоли. Авторы сосредоточились на молекуле KIAA1199, которая в избытке присутствует в опухолях с высоким риском. В моделях на мышах и в образцах пациентов опухоли с высоким уровнем KIAA1199 не только росли быстрее; они также подготавливали печень, превращая её в «предметастатическую нишу» — микроокружение, необычно благоприятное для прибывающих раковых клеток. Даже когда печёночные опухоли засевались экспериментально из отдельного источника, животные с KIAA1199‑высокими опухолями толстой кишки развивали гораздо больше печёночных метастаз и умирали раньше. Это показало, что сигналы от первичной опухоли, а не только блуждающие раковые клетки, заранее меняют печень.
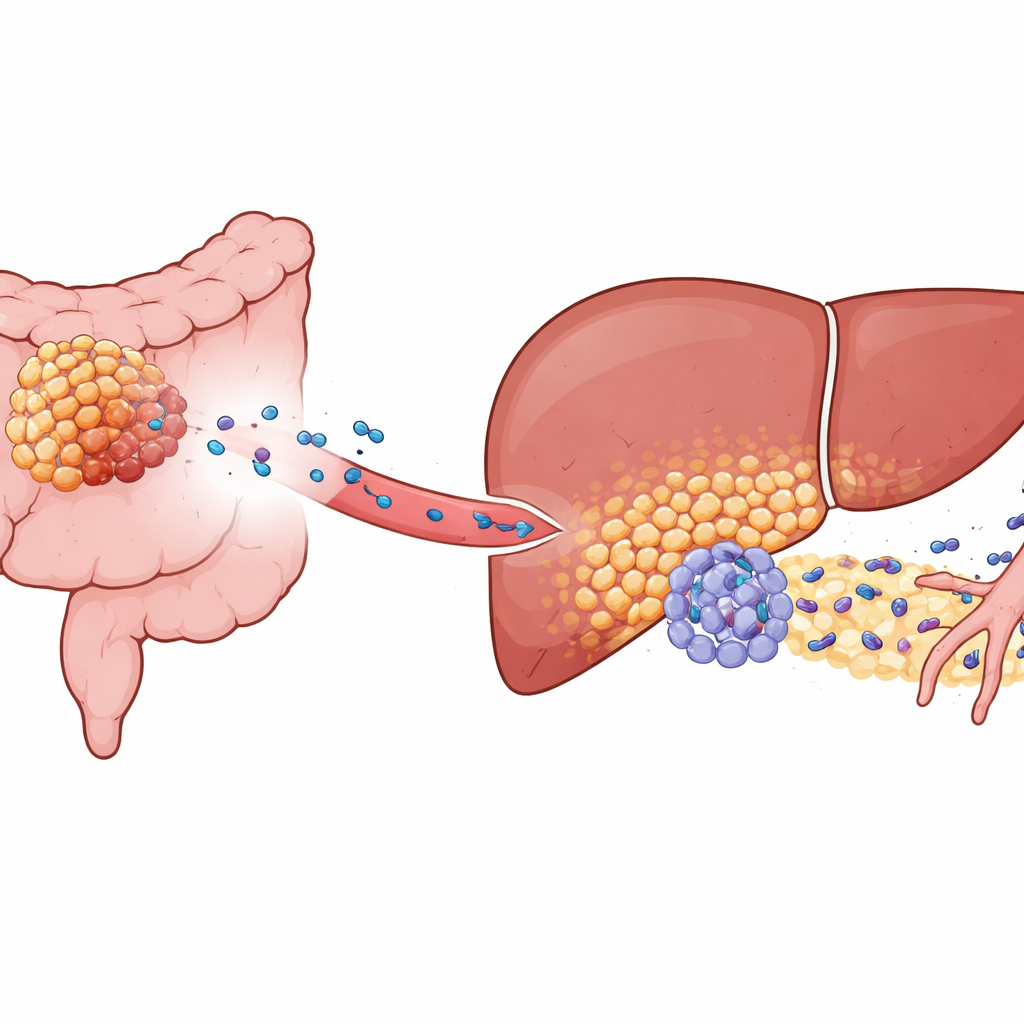
Клетки печени перепрограммируются в помощников опухоли
Углублённый анализ с использованием секвенирования отдельных клеток и пространственного картирования позволил исследователям изучить ткань печени с высоким разрешением. Они обнаружили отдельный подтип гепатоцитов — обычно функциональных рабочих клеток печени — который был «функционально перепрограммирован». Эти клетки появлялись только при наличии KIAA1199‑высоких опухолей. Вместо того чтобы тихо заниматься обменом веществ, изменённые гепатоциты переключались на более злокачественный метаболический профиль и снижали активность защитного регулятора PPARγ, который обычно контролирует воспаление и стрессовые ответы. При подавлении PPARγ эти гепатоциты начали вырабатывать высокие уровни белка SAA2 и выделять его в окружающую среду, особенно на границе, где печёночная ткань встречается с внедряющимися опухолевыми клетками.
Превращение обычных защитников в про‑метастатические нейтрофилы
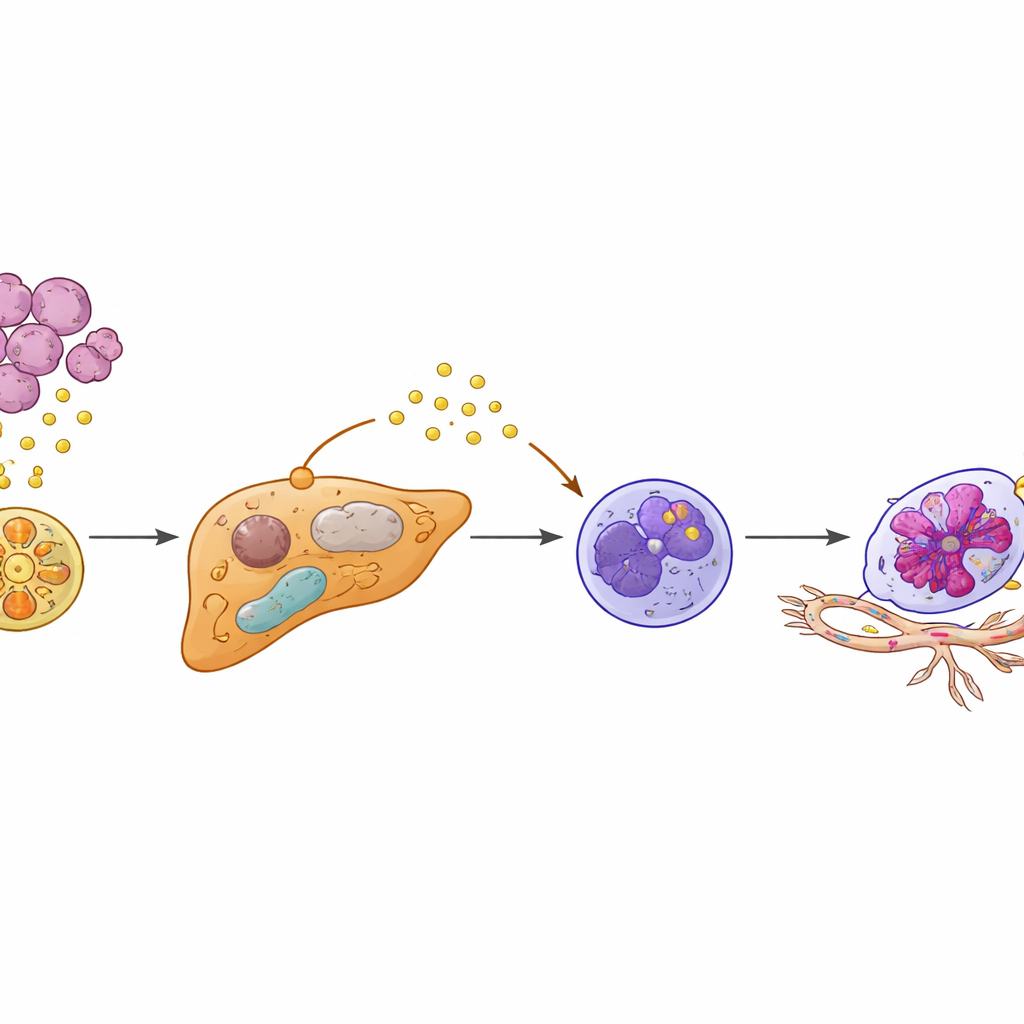
Нейтрофилы — лейкоциты, наиболее известные борьбой с инфекциями — также вели себя необычно в этой подготовленной печени. Авторы обнаружили особый подтип, несущий «Egr1+» подпись, названную по транскрипционному фактору, который перенастраивает функции этих клеток. Похоже, нейтрофилы не приходили из крови уже изменёнными, а переобучались локально перепрограммированными гепатоцитами. SAA2, выделяемый гепатоцитами, связывался с рецептором FPR2 на соседних нейтрофилах и включал внутриклеточную сигнальную цепь PI3K‑AKT, что стабилизировало активность Egr1. В результате появлялись более долго живущие, высокоактивные нейтрофилы, выделяющие большие количества VEGFA — мощного фактора, стимулирующего рост новых сосудов. Эти Egr1+ нейтрофилы группировались на границе «опухоль–печень», именно там, где прорастали новые, хрупкие сосуды.
Формирование сосудов, приветствующих опухолевые клетки
Исследование демонстрирует, что эти переобученные нейтрофилы не просто наблюдатели — они активно перестраивают сосудистую сеть печени. В культуре клеток факторы, выделяемые Egr1+ нейтрофилами, заставляли эндотелиальные клетки пролиферировать, мигрировать и формировать трубчатые структуры, напоминающие новые сосуды. У мышей введение Egr1+ нейтрофилов усиливало печёночные метастазы и ускоряло летальный исход. Блокирование ключевых звеньев этой цепочки — либо сигнала SAA2–FPR2 к нейтрофилам, либо последующего пути PI3K‑AKT — лишало нейтрофилы выживания и продукции VEGFA, снижая рост сосудов и распространение метастазов. Аналогично восстановление активности PPARγ в гепатоцитах с помощью противодиабетического препарата розиглитазона уменьшало уровни SAA2, подавляло появление Egr1+ нейтрофилов и резко снижало печёночную метастазирование в доклинических моделях.
От механизма к прогнозированию и предупреждению
Поскольку KIAA1199 в опухолях и SAA2 в печени занимают центральные позиции в этой цепи, авторы проверили, могут ли эти белки помочь определить пациентов с высоким риском печёночных метастазов. В нескольких когортах пациентов люди с повышенным уровнем обоих маркёров в крови значительно чаще и раньше развивали печёночные метастазы. Простая комбинированная шкала KIAA1199–SAA2 превзошла каждый маркер в отдельности по прогностической способности и была оформлена в клиническую «номограмму», оценивающую вероятность печёночного распространения у конкретного пациента в течение следующих двух лет. В совокупности результаты рисуют наглядную картину: KIAA1199‑высокие опухоли толстой кишки отправляют везикуло‑содержащие сигналы, которые перенастраивают гепатоциты, а те, в свою очередь, превращают соседние нейтрофилы в долго живущих, сосудостроительных соучастников. Ориентируясь на эту ось KIAA1199–PPARγ/SAA2–Egr1 — с помощью метаболических препаратов, иммуномодулирующих средств или их сочетания — возможно не только лечить уже существующие печёночные метастазы, но и предотвратить их установление изначально.
Цитирование: Li, L., Zhao, L., Cao, K. et al. Hepatocytes functionally reprogrammed by KIAA1199-high colorectal cancer cells favour the accumulation of pro-metastatic Egr1+ neutrophils. Nat Commun 17, 2462 (2026). https://doi.org/10.1038/s41467-026-69250-1
Ключевые слова: метастазирование колоректального рака в печень, предметастатическая ниша, нейтрофилы, перепрограммирование гепатоцитов, опухолевое микроокружение