Clear Sky Science · ru
Снижение метилирования лизина 4 гистона 3.3 в медиальном ганглиозном эминенце и гипоталамусе воспроизводит фенотипы нейроразвитийных расстройств
Как крошечные химические метки формируют мозг и тело
Почему некоторые генетические изменения вызывают одновременно проблемы с обучением и необычное развитие тела — например, очень малый размер в детстве и ожирение во взрослом возрасте? В этом исследовании рассматриваются крошечные химические метки на белках, упаковывающих ДНК в мозге, и показано, как их нарушение в всего двух ключевых областях может отдавать волной припадками, поведением, похожим на тревожность, проблемами памяти и резкими изменениями массы тела у мышей.
Выключатели на регуляторах активности генома
Внутри каждой клетки мозга ДНК намотана на катушкообразные белки, называемые гистонами. Химические метки, нанесённые на эти гистоны, действуют как регуляторы яркости, повышая или понижая активность групп генов. Одна из таких меток, нанесённая на место, именуемое H3K4, тесно связана с включением генов. Исследования на людях показали, что люди с дефектами в ферментах, добавляющих или снимающих эту метку, часто имеют нейроразвитийные расстройства, сочетающие интеллектуальную недостаточность, эпилепсию и аномальный рост тела. Однако оставалось неясным, какие именно клетки мозга наиболее чувствительны к такому нарушению и как их дисфункция может объединять возбудимость мозга и метаболизм всего организма.
Тригер на двух критических узлах мозга
Исследователи создали мышей, в которых мутантная версия гистонового белка (H3.3K4M) активировалась только в клетках, происходящих из двух эмбриональных областей мозга: медиального ганглиозного эминенса, который даёт многие тормозные «тормозящие» клетки мозга, и развивающегося гипоталамуса, отвечающего за аппетит, гормоны и энергетику. Эта мутация специально блокирует метилирование H3K4, не уничтожая сами гистоны. Тесты подтвердили широкое присутствие мутантного белка в целевых областях и сильное снижение нормальных меток H3K4 при сохранении общего уровня гистонов. Такая конструкция имитирует многие человеческие состояния, где повреждён только один аллель гена, связанного с H3K4, а не полное его отсутствие.
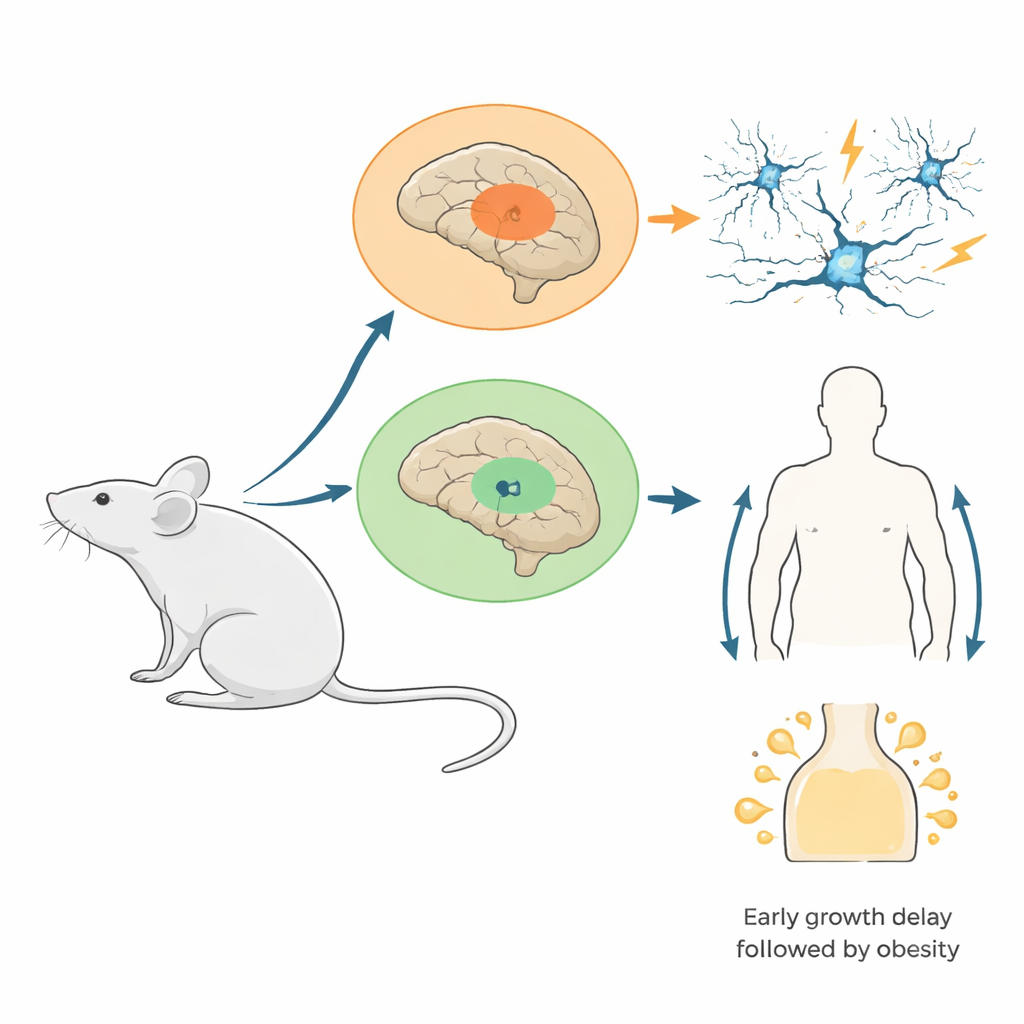
От исчезающих тормозных клеток к цепям, склонным к припадкам
По мере роста мышей последствия для мозговых сетей становились очевидны. У молодых мутантов было меньше тормозных интернейронов в коре и гиппокампе, особенно одного быстрого типа, который обычно строго синхронизирует нейронные ритмы. Подробные записи показали, что оставшиеся интернейроны присутствовали, но их электрические свойства стали более вариабельными, что указывает на нарушение созревания. При стимуляции гиппокампа в срезах мозга обычно наблюдаемые высокочастотные «гамма»-осцилляции — электрические ритмы, связанные с обработкой информации — были слабее и медленнее, и появлялись аномальные схожие на вспышки события. В живых животных многие мутанты, особенно самки, развивали спонтанные припадки и были гораздо чувствительнее к индуцированным препаратами припадкам. Ранняя стадия развития показала, что потеря клеток в основном связана с плохой миграцией интернейронов в кору, а не с повышенной гибелью или снижением деления клеток.
Перепрограммирование активности генов в клетках, связанных с припадками
Чтобы связать эти физические изменения с регуляцией генов, команда использовала одноядерное секвенирование, которое читает как активность генов, так и доступность ДНК в отдельных клетках. В эмбриональном медиальном ганглиозном эминенсе большинство генов, изменившихся у мутантов, были подавлены, в том числе ключевые регуляторы, направляющие клетки к специфическим тормозным судьбам. У взрослых интернейронов баланс между подтипами сместился, и группы генов, участвующих в образовании связей и контроле потоков калия — токов, которые задают скорость возбуждения — оказались нарушены. Сетевой анализ выделил координированное нарушение генов калиевых каналов, которые уже известны как влияющие на эпилепсию и мозговые ритмы, что даёт прямую молекулярную связь между потерей гистоновой метки, изменённой идентичностью интернейронов и восприимчивостью к припадкам.
Дисбаланс гипоталамуса и двухфазная кривая роста
Гипоталамус рассказал дополнительную историю, сосредоточенную на росте тела. В раннем возрасте мутантные мышата были мельче, и заметная часть погибала в раннем возрасте. Выжившие, однако, позже ели больше, накапливали жир и развили высокие уровни гормона лептина, что указывает на ожирение и вероятную резистентность к лептину. Анализ отдельных клеток эмбрионального гипоталамуса выявил больше делящихся предшественников, но меньше клеток, направленных в ключевые ядра, связанные с регуляцией питания, особенно областей, которые обычно чувствуют питание и регулируют гормон роста. В взрослом гипоталамусе клеточный состав изменился: резко увеличилось число астроцитов, уменьшилось число олигодендроцитов, а специализированные барьерные клетки — танициты и соседние глии — утратили упорядоченное расположение на границе мозга с циркулирующими гормонами и питательными веществами. Эти структурные и изменения в экспрессии генов, вероятно, искажают способность мозга оценивать энергетические запасы и контролировать аппетит.
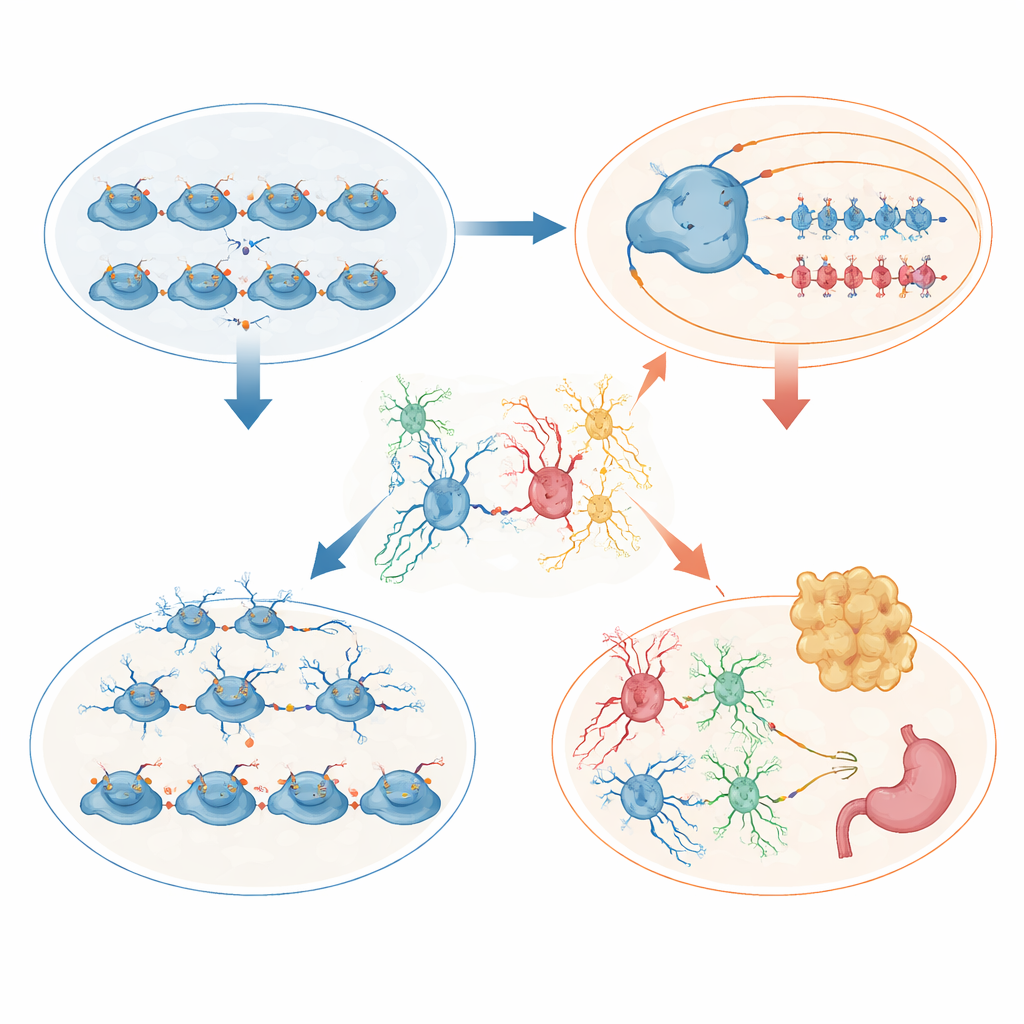
Поведенческие отголоски человеческих нейроразвитийных расстройств
Поведение мышей отзеркаливало симптомы, наблюдаемые при многих нейроразвитийных состояниях. Они проявляли усиленное поведение, похожее на тревожность, изменённую походку, сниженную спонтанную активность дома и плохую производительность в задачах, исследующих память, распознавание объектов и фильтрацию пугающих звуков. В некоторых тестах отмечались повышенные импульсивные действия. По нескольким показателям самки, как правило, были более тяжело затронуты, чем самцы, что указывает на возможное взаимодействие половых гормональных систем и регуляции генов с гистоновыми метками, формирующее уязвимость.
Что это значит для здоровья человека
Вместе эти результаты показывают, что ослабление одного набора гистоновых меток всего в двух эмбриональных узлах мозга достаточно, чтобы воспроизвести широкий спектр проблем: меньше тормозных «тормозов», нестабильные мозговые сети, припадки, нарушенные цепи питания и аномальный рост тела. Для неспециалистов ключевое послание таково: эпигенетические метки, такие как метилирование H3K4, — это не абстрактные добавления, а точные регуляторы, которые помогают развивающимся клеткам мозга стать нужным типом в нужном месте и в нужное время. Когда эти регуляторы сбиваются, как в ряде редких генетических синдромов, результатом может быть тесно связанная комбинация когнитивных, поведенческих и метаболических симптомов. Понимание этих общих корней в конечном счёте может привести к терапии, корректирующей не только один симптом, например припадки или ожирение, но и взаимосвязанную систему, которая их порождает.
Цитирование: Li, J., Tanzillo, A.F., Pizzirusso, G. et al. Reducing methylation of histone 3.3 lysine 4 in the medial ganglionic eminence and hypothalamus recapitulates neurodevelopmental disorder phenotypes. Nat Commun 17, 2984 (2026). https://doi.org/10.1038/s41467-026-69248-9
Ключевые слова: эпигенетика, внутренние нейроны, гипоталамус, припадки, ожирение