Clear Sky Science · ru
Разъединение фазового разделения и фибриллизации сохраняет активность биомолекулярных конденсатов
Почему это важно для здоровья мозга
Во многих заболеваниях головного мозга, включая болезнь Альцгеймера, белки со временем скапливаются в плотные волокнистые клубки. Те же белки могут также формировать более мягкие, похожие на капли структуры внутри клеток, которые помогают организовывать химические процессы — как крошечные жидкие рабочие станции. В этом исследовании поставлен ключевой вопрос: можно ли остановить вредную отвердение этих капель в волокна, не разрушив их полезную повседневную функцию? Авторы показывают, что распространённый клеточный метаболит — аминокислота L-аргинин — способен делать именно это для ключевого белка, связанного с Альцгеймером, называемого тау.
От свободно плавающего белка к крошечным каплям
Внутри клеток некоторые белки не всегда остаются равномерно растворёнными в жидкости. Вместо этого они могут собираться в капли — биомолекулярные конденсаты, — которые ведут себя как очень мягкие гели или вязкие жидкости. Исследователи сосредоточились на тау — белке, который обычно помогает строить и стабилизировать микротрубочки, полые нити, выступающие в роли «дорог» внутри нервных клеток. Тау также печально известен способностью формировать амилоидные фибриллы — жёсткие волокна, обнаруживаемые в клубках при многих нейродегенеративных заболеваниях. Чтобы проследить, как капли тау меняются со временем, учёные создали модифицированную версию белка под названием SynTag-Tau, которая образует активные конденсаты, стареющие в амилоидные фибриллы на удобном для эксперимента временном масштабе, без агрессивных добавок.
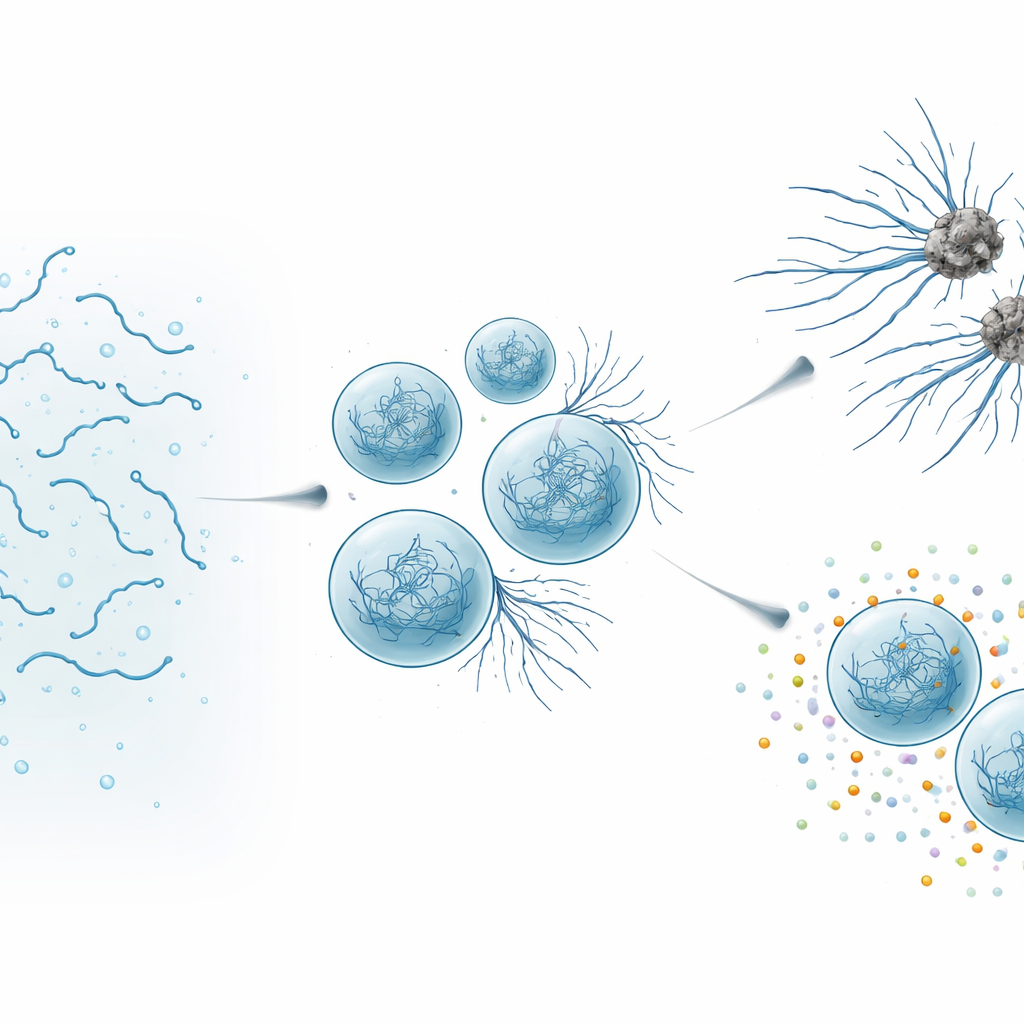
Когда полезные капли становятся вредными
С помощью высокоразрешающей микроскопии и биофизических измерений авторы наблюдали за изменениями капель SynTag-Tau в течение нескольких часов. Свежие капли вели себя как жидкости: они легко сливались, молекулы внутри быстро перемещались, и не было признаков упорядоченной структуры. Со временем капли замедлялись и затвердевали, и тонкие волокна начали прорастать от их поверхности в окружающий раствор. Чувствительные оптические методы показали, что эти волокна содержат плотно упакованную «cross–beta» архитектуру, типичную для амилоида. Важно, что интерфейс — граница между плотной каплей и окружающей жидкостью — выступал как горячая точка, где фибриллы появлялись первыми. По мере старения капель и появления большего числа волокон нормальная функция тау ухудшалась: конденсаты становились менее способными привлекать тубулин, строительный блок микротрубочек, и в конечном итоге полностью теряли способность поддерживать сборку микротрубочек.
Малые молекулы, смещающие равновесие
Затем исследователи спросили, могут ли простые метаболиты замедлить или предотвратить переход из жидкого состояния в волокнистое, не разрушая сами капли. Проверив несколько естественно встречающихся малых молекул, они обнаружили, что положительно заряженные аминокислоты L-аргинин и L-лизин сильно замедляют или блокируют образование амилоидных фибрилл из капель SynTag-Tau, при этом не подавляя образование самих конденсатов при реалистичных низкомиллимолярных концентрациях. Напротив, отрицательно заряженные аминокислоты, такие как глутамат и аспартат, ускоряли формирование фибрилл, а общие химические агенты, разрушающие белки, либо не помогали, либо нарушали сами капли. Флуоресцентный аналог L-аргинина показал, что эта молекула предпочитает находиться внутри конденсатов тау, а не снаружи, что указывает на её действие там, где это наиболее необходимо.
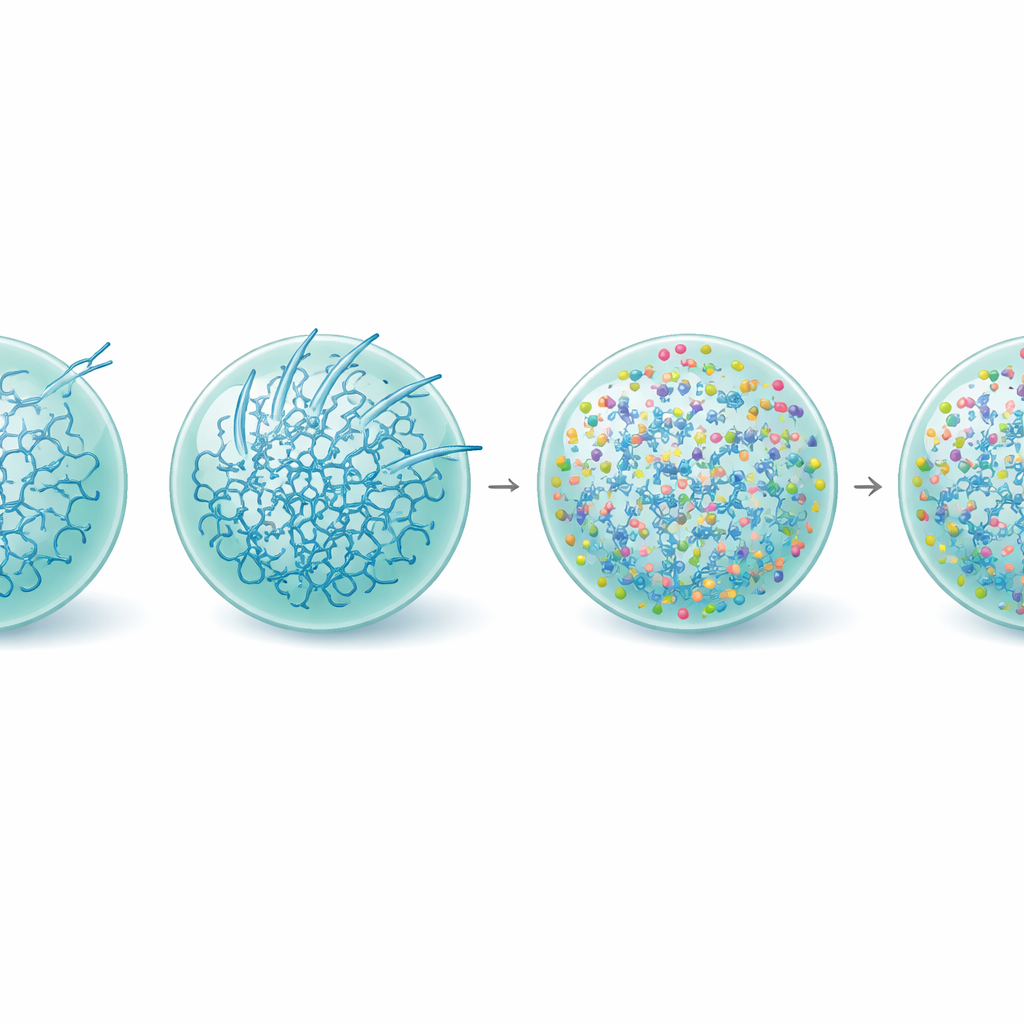
Укрепление капли, сохранение функции
Углубив исследование, команда изучила, как L-аргинин меняет внутреннюю организацию капель тау. Измерения структуры белка показали, что при наличии L-аргинина доля молекул тау, принимающих жёсткие бета-обогащённые формы, связанные с амилоидом, уменьшалась, даже в старых каплях. Видеонасилеметрия наноревологии — отслеживание движения крошечных частиц внутри конденсатов — показала, что L-аргинин фактически делает капли тау более вязкоупругими: их внутренняя сеть становится прочнее и более взаимосвязанной, оставаясь при этом похожей на жидкость. Это усиление, по-видимому, удерживает систему в метастабильном функциональном состоянии и повышает энергетический барьер для образования фибрилл, особенно на поверхности капли. Согласуясь с этим, обработанные L-аргинином конденсаты продолжали равномерно привлекать тубулин и поддерживать рост микротрубочек долгое время после того, как необработанные капли утратили активность.
Что это означает для будущих терапий
Работа показывает, что силы, приводящие к образованию белковых капель, и силы, приводящие к образованию вредных волокон, связаны, но могут быть разобщены. Настраивая химию внутри конденсатов с помощью метаболита, такого как L-аргинин, возможно сохранить полезное, жидкоподобное состояние и одновременно задержать или предотвратить переход к амилоидным волокнам, связанным с болезнью. Хотя в этом исследовании использована специально сконструированная система тау in vitro, оно служит доказательством принципа: малые молекулы, избирательно укрепляющие стабильность конденсатов, однажды могут помочь защитить клетки от постепенного накопления токсичных белковых агрегатов, не блокируя при этом нормальные организующие функции биомолекулярных конденсатов.
Цитирование: Mahendran, T.S., Singh, A., Srinivasan, S. et al. Decoupling phase separation and fibrillization preserves activity of biomolecular condensates. Nat Commun 17, 2841 (2026). https://doi.org/10.1038/s41467-026-69244-z
Ключевые слова: Белок тау, биомолекулярные конденсаты, амилоидные фибриллы, L-аргинин, нейродегенерация