Clear Sky Science · ru
Варианты FOXJ3, связанные с эпилепсией, связывают транскрипционную программу пути PTEN–mTOR с нейронной спецификацией и ламинацией коры
Когда проводящие пути мозга идут немного не по плану
Эпилепсия часто начинается в детстве, но у многих молодых пациентов на снимках мозга врачи не видят ничего очевидно патологического. В этом исследовании изучается одна скрытая причина: крошечные изменения в гене FOXJ3, которые тихо меняют процесс построения внешнего слоя мозга — коры. Проследив действие этого гена в семьях с фокальной эпилепсией и в развивающемся мозге мышей, исследователи показывают, как ранние сбои в рождении клеток, их миграции и слоярной укладке в конце концов могут привести к припадкам.
Тонкая дисплазия, стоящая за трудноизлечимыми припадками
У многих детей с фармакорезистентной фокальной эпилепсией обнаруживают состояние, называемое фокальной кортикальной дисплазией (ФКД), при котором участки коры сформированы неправильно. В таких зонах есть смещённые и аномально крупные нейроны, и именно они часто объясняют неэффективность лекарств. Тем не менее молекулярные причины ФКД нередко остаются неизвестными, а рутинная МРТ может пропустить мелкие или поверхностные дефекты. Авторы начали с семьи, у нескольких членов которой была фокальная эпилепсия и признаки ФКД. Тщательный анализ генома указал на редкие варианты в FOXJ3 — гене, ранее не связанном с эпилепсией. Дополнительные случаи из больших генетических баз данных выявили больше людей с необычными вариантами FOXJ3 и фокальными припадками, что указывает на возможную повторяющуюся роль этого гена в подобных расстройствах.
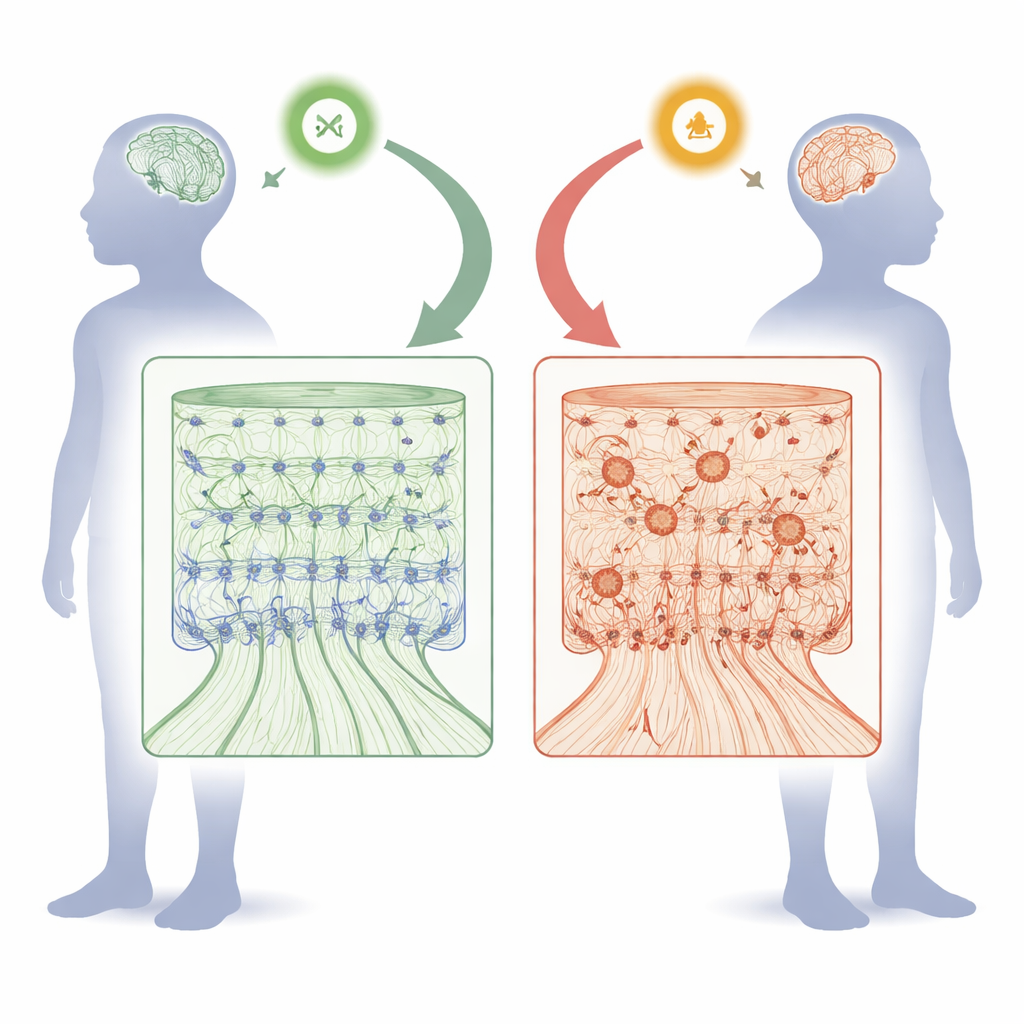
Как FOXJ3 помогает формировать мыслительную поверхность мозга
Во время внутриутробного развития кора собирается как многоэтажное здание. Клетки-предшественницы, выстилающие внутреннюю поверхность мозга, делятся, затем отправляют новорожденные нейроны по радиальным «строительным лесам», чтобы сформировать шесть упорядоченных слоев. Команда обнаружила, что FOXJ3 активен как в этих предшественниках, так и в молодых нейронах, но его активность в предшественниках естественно падает после определённого момента в среднем периоде беременности. Применив инструменты генной инактивации в эмбрионах мышей, исследователи снижали уровни Foxj3 на разных этапах и наблюдали последствия. Раннее подавление Foxj3 замедляло миграцию новорождённых нейронов и заставляло их оседать в неправильных слоях. Клетки, которые должны были стать глубокослойными нейронами, вместо этого приобретали черты верхних слоёв, а числа коллозально проецирующих нейронов, связывающих два полушария, увеличивались. Однако при снижении Foxj3 на поздних этапах развития эффекты были значительно слабее, что показывает высокую чувствительность его роли ко времени действия.
Баланс деления клеток и роста
Чтобы понять, почему FOXJ3 оказывает такое влияние, исследователи объединили несколько крупномасштабных подходов. Они сопоставили места связывания FOXJ3 с ДНК и определили, какие гены активны в тысячах отдельных корковых клеток. Анализ ясно указал на гены, управляющие клеточным циклом и ростом мозга, особенно на PTEN — главный тормоз пути роста mTOR. В предшественниках связывание FOXJ3 усиливало активность PTEN, что в свою очередь помогало клеткам выходить из цикла деления, превращаться в нейроны и мигрировать наружу упорядоченно. При подавлении Foxj3 больше предшественников оставалось в состоянии деления, меньше клеток своевременно выходило из цикла, и миграция задерживалась в промежуточных зонах. Критически важно, что восстановление уровней PTEN в мозгах с дефицитом Foxj3 в значительной мере обращало нарушения миграции, стратификации и судьбы клеток, тогда как усиление другого регулятора роста, TSC1, этого не делало. Это помещает PTEN в центр контроля FOXJ3 над строительством коры.
От нарушенных путей к увеличенным нейронам
Далее команда изучила, как ведут себя варианты FOXJ3, похожие на пациентские. Болезнетворная версия FOXJ3 не смогла повысить уровни PTEN и позволила пути mTOR стать сверхактивным, что проявлялось повышенной фосфорилированием ключевого белка, связанного с ростом. У подростковых мышей, генетически модифицированных так, чтобы экспрессировать эту мутантную форму в развивающейся коре, нейроны позднее выглядели заметно вздутыми, с большими телами и периметрами клеток, воспроизводя дизморфные клетки, наблюдаемые при человеческой ФКД. При этом мутантный белок всё ещё правильно попадал в ядро, что указывает на то, что проблема заключается в нарушении регуляции генов, а не в неверной локализации. В совокупности эти данные связывают мутации FOXJ3 с каскадом событий — снижение PTEN, усиление сигнальности mTOR, задержка выхода из клеточного цикла, спутанная миграция и гипертрофия нейронов — которые могут заложить основу для эпилептических сетей.
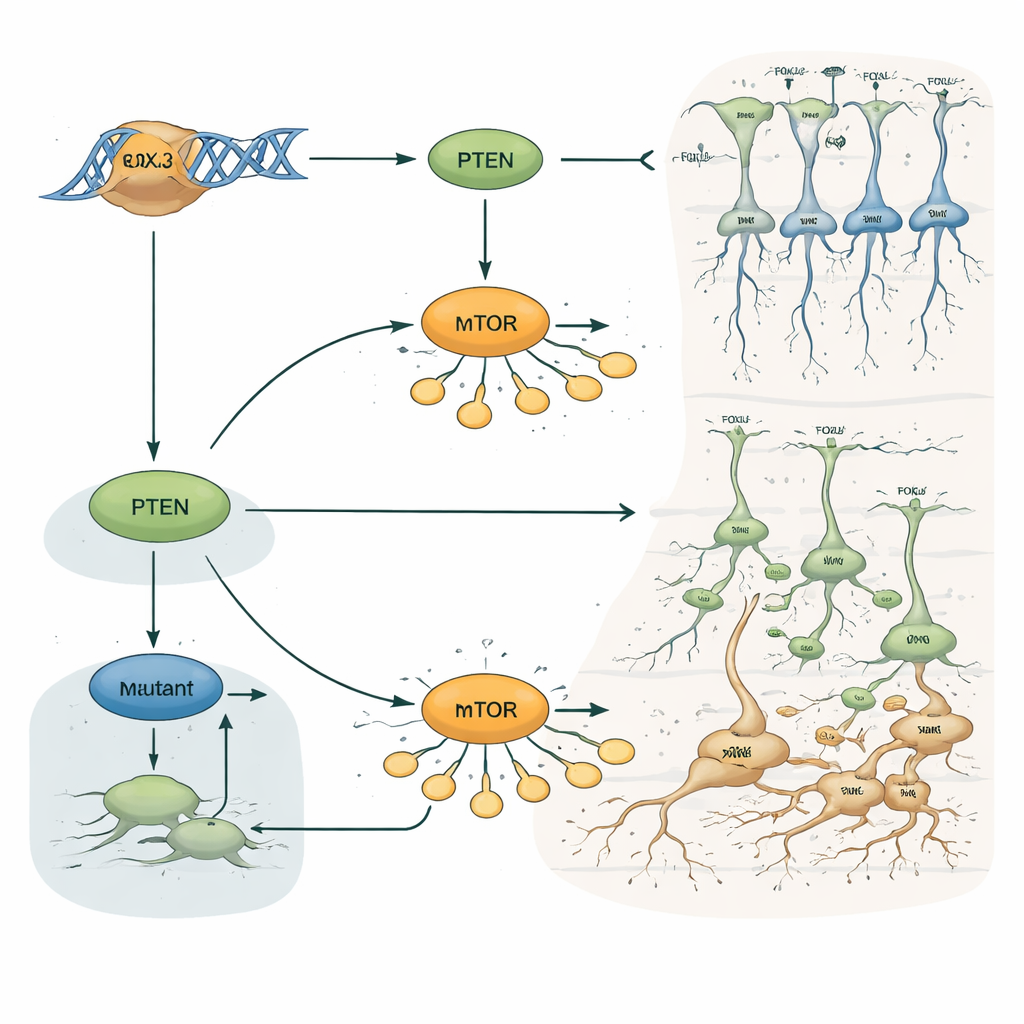
Почему это важно для эпилепсии и скрытых повреждений мозга
Для неспециалиста ключевое послание таково: один транскрипционный фактор, FOXJ3, помогает определить, когда и где рождаются корковые нейроны, как они перемещаются и в какой слой в итоге попадают. Через путь роста PTEN–mTOR FOXJ3 поддерживает «строительный» график мозга. Редкие изменения в этом гене могут нарушить этот баланс, вызывая небольшие участки коры с неправильной проводкой и стратификацией, даже если МРТ выглядит нормальной. Эта работа не только выдвигает FOXJ3 в качестве новой генетической причины фокальной кортикальной дисплазии и эпилепсии, но и иллюстрирует, как тонкие сдвиги в раннем развитии мозга могут отозваться десятилетиями позже в виде трудно поддающихся лечению припадков.
Цитирование: Cheng, HY., Liu, C., Nien, CW. et al. Epilepsy-associated FOXJ3 variants link a transcriptional program of the PTEN-mTOR pathway to neuronal specification and cortical lamination. Nat Commun 17, 1815 (2026). https://doi.org/10.1038/s41467-026-69241-2
Ключевые слова: фокальная кортикальная дисплазия, ген FOXJ3, путь PTEN mTOR, развитие коры, фокальная эпилепсия