Clear Sky Science · ru
Молекулярная основа галактозилирования коллагена ферментом GLT25D1
Как крошечные сахарные метки помогают создавать прочные ткани
Коллаген — самый распространённый белок в организме, он образует каркас для кожи, костей, кровеносных сосудов и многих других тканей. Но коллаген не действует в одиночку: ему нужно «надеяться» небольшими молекулами сахара в строго определённых местах, чтобы он приобрёл нужную прочность и гибкость. В этом исследовании в атомных подробностях показано, как один ключевой фермент, GLT25D1, присоединяет определённый сахар к коллагену и каким образом нарушения в этом процессе могут приводить к хрупкости сосудов, проблемам с мышцами и, возможно, к раку.
Взгляд поближе на скрытую «макияжную» правку коллагена
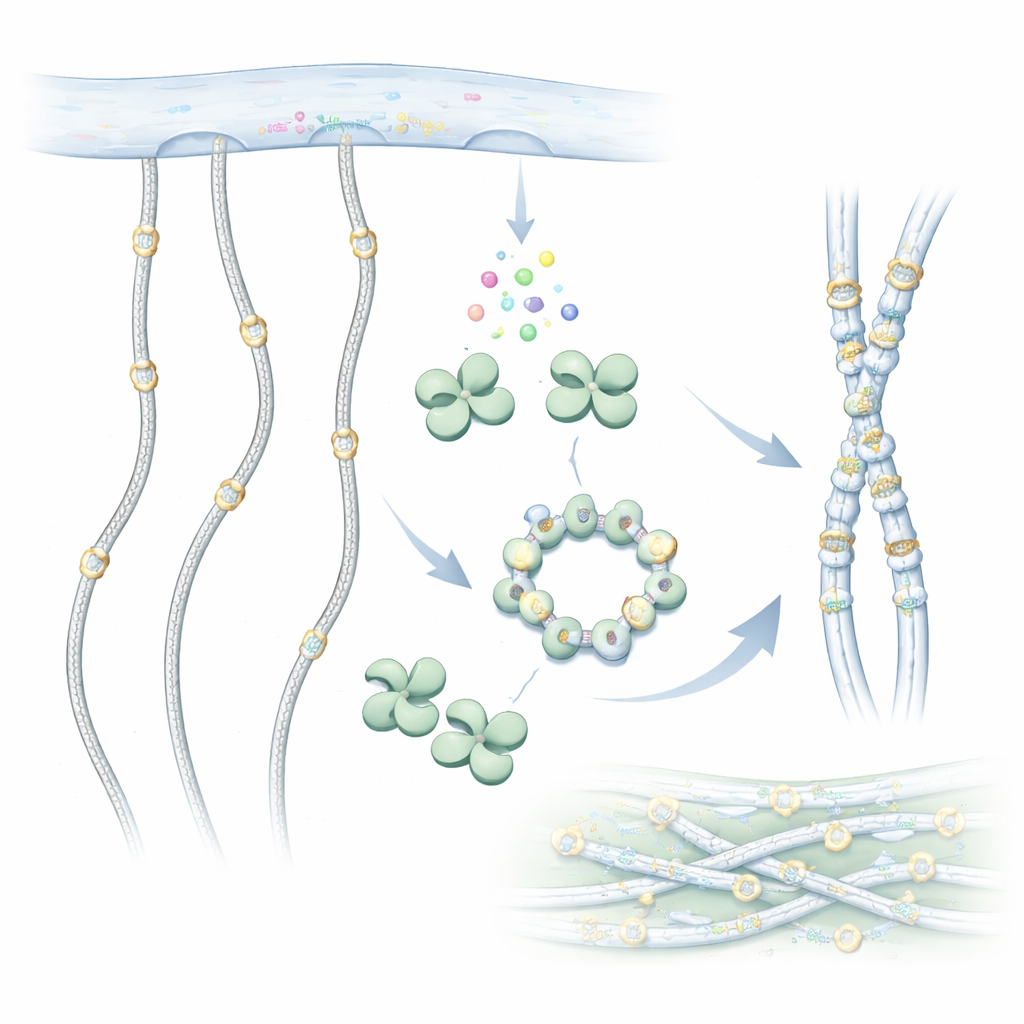
Молекулы коллагена длинные, верёвкообразные цепи, которые собираются во внеклеточные прочные волокна. Однако прежде чем покинуть клетку, они подвергаются химической «редакции». Одно из важных изменений — добавление сахарных групп к особым строительным блокам, называемым гидроксилизинами, вдоль цепи коллагена. GLT25D1 выполняет первый шаг этой сахарной пометки, переносит галактозу с донорной молекулы на гидроксизин. Эта модификация сохраняется от простых животных до человека и помогает коллагену правильно сворачиваться, взаимодействовать с клетками и сопротивляться износу.
Раскрытие формы «декоратора» коллагена
Чтобы понять, как работает GLT25D1, исследователи использовали крио‑электронную микроскопию для визуализации человеческого фермента с почти атомным разрешением. Они обнаружили, что каждая молекула GLT25D1 имеет две похожие доли, обе связанные с общим ферментным фолдом, характерным для белков‑переносчиков сахаров. Эти доли объединяются в продолговатые димеры, а три димера могут далее собираться в гексамер в форме кольца. В таких сборках истинные «трудяги» — каталитические центры — располагаются далеко друг от друга; такая организация может позволять нескольким сайтам добавлять сахар одновременно вдоль натянутой цепи коллагена.
Рабочие части: где на самом деле происходит перенос сахара
Команда решила структуры GLT25D1, связанную как с донором сахара, так и с коротким пептидом, похожим на участки коллагена и содержащим гидроксилизин. Этот тернарный комплекс показал, что только вторая доля, называемая С‑концевым доменом, действительно осуществляет химическую реакцию. Там донорная молекула располагается в кармане, стабилизированном ионным металлом, в то время как пептид лежит в узкой борозде, которая обеспечивает специфический локальный мотив: гидроксилизин сразу за которым следует маленькая глицин. Один остаток аспарагата действует как химическая основа, активируя гидроксильную группу гидроксизина, чтобы она могла атаковать сахар и завершить перенос. Изменения в любом из этих ключевых аминокислотных остатков резко снижают или полностью уничтожают активность, подтверждая их жизненно важные роли.
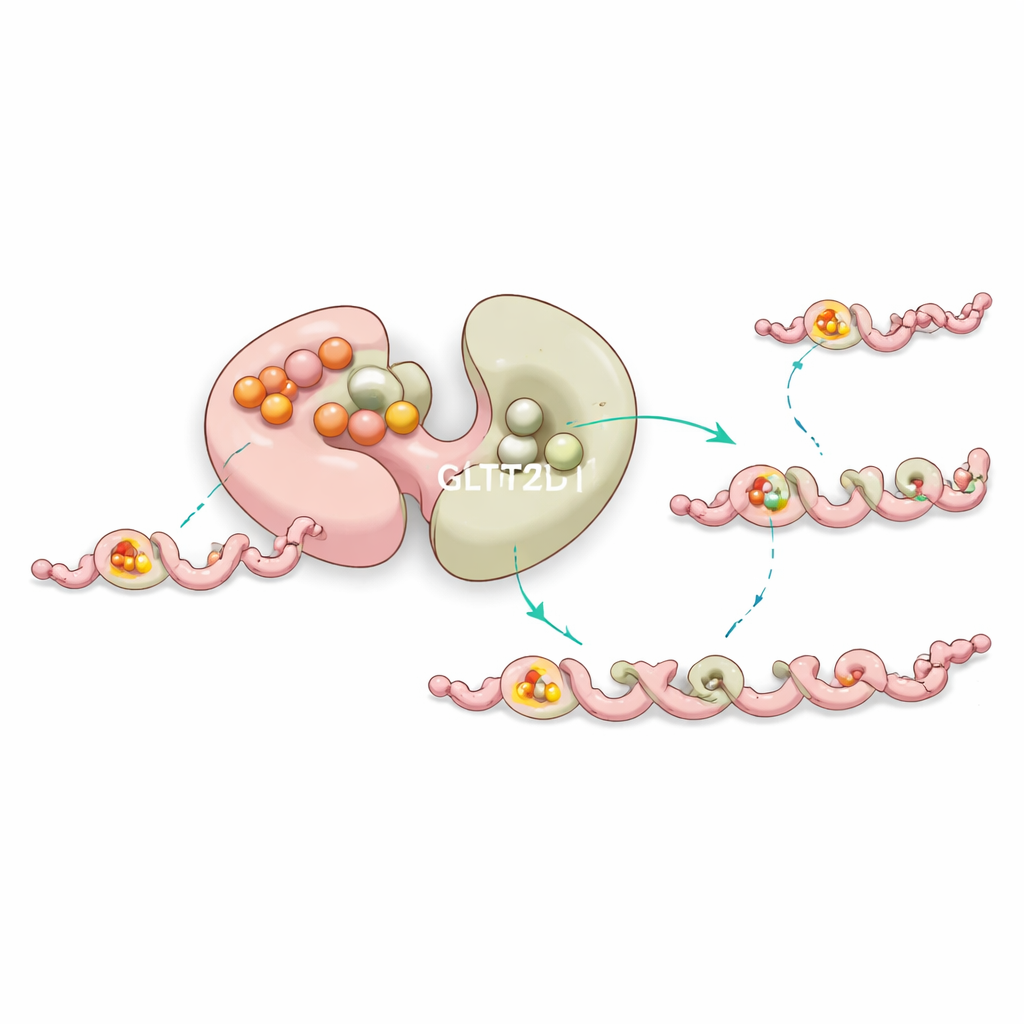
Встроенный стабилизатор и дальнодействующий контроль
Любопытно, что первая доля GLT25D1 очень плотно связывает донор сахара, но не осуществляет перенос. Вместо этого эксперименты и компьютерные симуляции показывают, что этот «немой» сайт помогает стабилизировать фермент и тонко настраивает поведение активной доли через дальнодействующую связь внутри белка. Мутации рядом с этим не‑каталитическим карманом часто дестабилизируют фермент или изменяют его эффективность, что намекает на то, что природа использует этот дополнительный сайт связывания как форму внутреннего контроля качества, чтобы модификация коллагена шла гладко.
Когда «декоратор» даёт сбой: связи с болезнями
Нанесение на структурную модель мутаций, найденных у пациентов, позволило авторам объяснить, как ошибки в GLT25D1 приводят к заболеваниям человека. Некоторые мутации отрезают каталитическую долю полностью, другие дестабилизируют белковое ядро, а третьи поражают сами сайты связывания сахара или коллагена. Эти дефекты уменьшают или устраняют добавление сахара к коллагену и связываются с болезнями малых сосудов мозга, когнитивными нарушениями и дефектами мышц и скелета. Мутации, связанные с раком, также сосредоточены в критических регионах, что предполагает: изменённая «украшенность» коллагена может влиять на рост и распространение опухолей.
Почему это важно для здоровья и будущих терапий
Представив детальную трёхмерную «схему» GLT25D1 в действии, эта работа объясняет, как точечные сахарные метки добавляются к коллагену и почему этот шаг так важен для целостности тканей. Для неспециалистов ключевая мысль такова: крошечные химические изменения на коллагене могут иметь непропорционально большие последствия для состояния сосудов, костей и, возможно, риска рака. Структурная карта GLT25D1 теперь служит проводником для диагностики вредных вариантов и для разработки терапий — будь то малые молекулы, стабилизирующие дефектные ферменты, или генетические подходы — которые однажды смогут исправлять дефекты «сахарной» маркировки коллагена у их истока.
Цитирование: Sun, H., Zhang, M., Shi, Y. et al. Molecular basis of collagen galactosylation by GLT25D1. Nat Commun 17, 2426 (2026). https://doi.org/10.1038/s41467-026-69234-1
Ключевые слова: гликозилирование коллагена, GLT25D1, внеклеточный матрикс, сосудистые заболевания, структура крио-ЭМ