Clear Sky Science · ru
Дефицит склеростина повышает чувствительность белых адипоцитов к термогенным сигналам, индуцирующим беигинг у мышей
Почему разогрев жира может охладить болезни
Большинство из нас считает кость и жировую ткань разными мирами: одна даёт опору, другая хранит энергию. Исследование на мышах показывает, что кость и жир постоянно обмениваются химическими сигналами, и что белок, вырабатываемый клетками кости, может решать, будет ли наш «белый» жир просто запасать калории или превратится в более активную, сжигающую калории «бежевая» ткань. Понимание этого скрытого диалога может открыть новые пути борьбы с ожирением, диабетом и потерей костной массы одновременно.
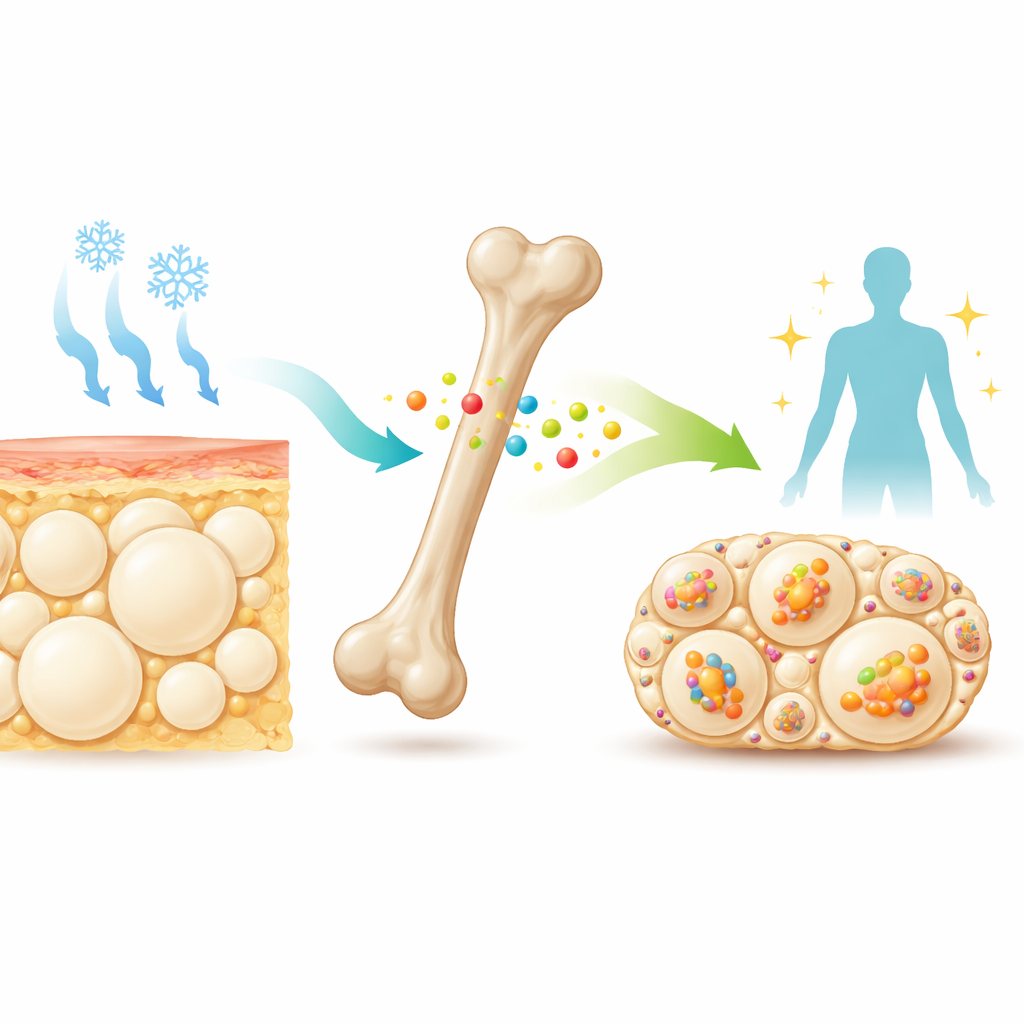
Тихий вестник из кости
Глубоко в костях специализированные клетки выделяют в кровь небольшой белок — склеростин. Врачи уже нацеливаются на склеростин при лечениe пациентов с повышенным риском переломов, чтобы укрепить кости. Ранние работы показали, что мыши, лишённые склеростина, не только имеют крепкие кости, но и более худые и более чувствительны к инсулину. Их подкожный жир, особенно в области бёдер (паховый белый жир), содержит мелкие многокамерные адипоциты, напоминающие бежевая ткань, которая может сжигать топливо для выработки тепла. Эти подсказки натолкнули исследователей на вопрос: действует ли склеростин как тормоз, мешающий организму превращать белый жир в бежевая при воздействии холода или препаратов, имитирующих нервные сигналы к жиру.
Холодовые сигналы, костные сигналы и зажигание жира
Команда подвергла обычных мышей и мышей, лишённых гена склеростина (Sost-/-), действию препарата, активирующего специфический рецептор адипоцитов (β3-адренергический рецептор), или мягкому холоду. У нормальных животных эти термогенные сигналы увеличивали производство склеростина в кости и повышали его уровень в крови. Этот рост связывали с потерей губчатой кости, но лишь с незначительными изменениями подкожного жира. Напротив, у мышей без склеростина ответ был гораздо сильнее: их паховый жир поглощал больше глюкозы, выделял больше жирных кислот, уменьшался в размере и заполнялся беже-подобными клетками, богатыми митохондриями — энергетическими станциями клетки. Ключевые термогенные гены включались сильнее в этих мышах, особенно в подкожном жире, тогда как классическая буроватая ткань оставалась в значительной степени неизменной.
Тонкая настройка сжигания жира через общий переключатель
Чтобы понять, как склеростин реализует этот контроль, исследователи сосредоточились на β-катенине — белке, участвующем в Wnt-сигнальном пути, который склеростин обычно подавляет в кости. В жировой ткани активация β-катенина после рождения направляла белые клетки в беже-подобное состояние и усиливала их ответ на β3-адренергические сигналы, но этот эффект исчезал, когда мышей содержали в тёплом, термонейтральном окружении, где организму больше не требуется дополнительное тепло. И наоборот, удаление β-катенина специально в адипоцитах мышей без склеростина уничтожало их бежевая ткань, восстанавливало большие белые адипоциты и отменяло улучшения в уровнях инсулина и жирных кислот. Эти эксперименты указывают на то, что при низком уровне склеростина β-катенин в жировых клетках становится важным внутренним рычагом, делающим белый жир более отзывчивым на термогенные сигналы.
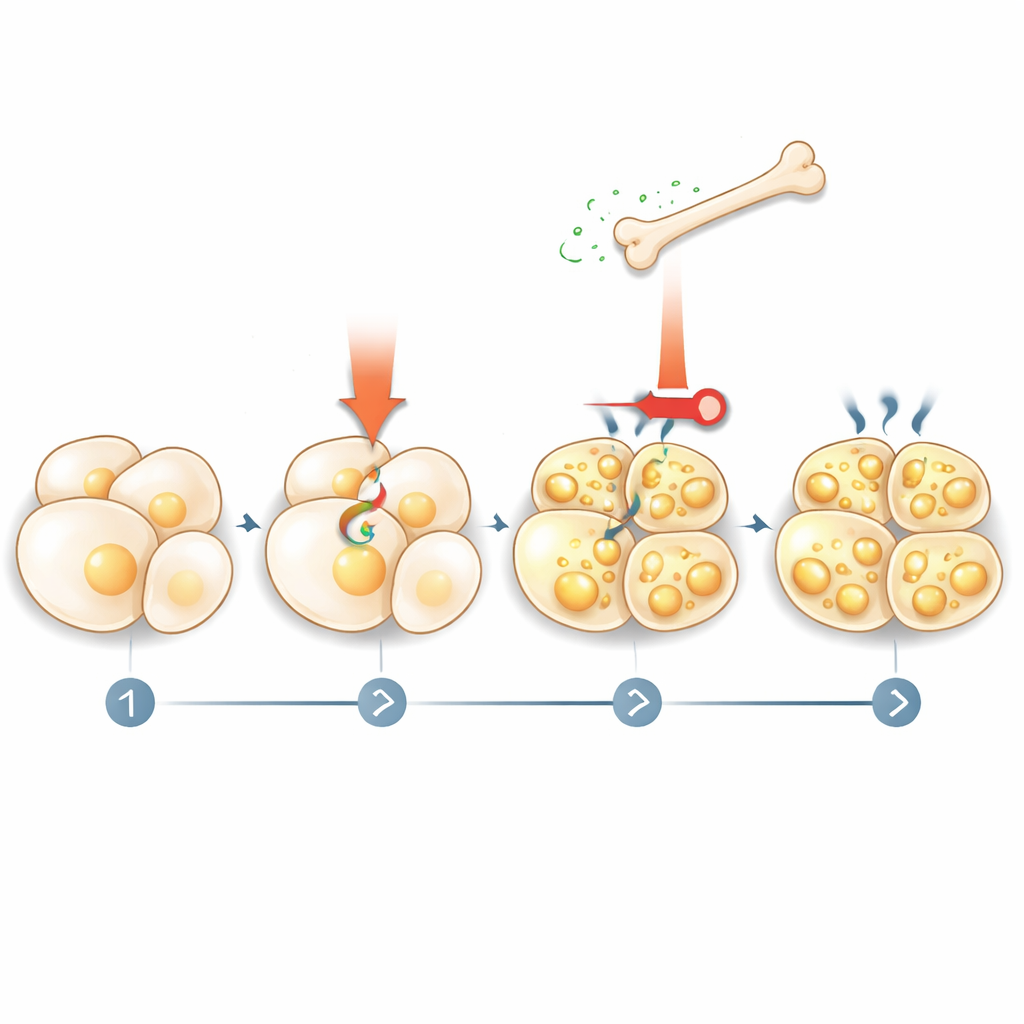
Как жир отвечает кости
История не закончилась тем, что кость приказывала жиру, что делать. Команда обнаружила, что термогенная стимуляция активирует распад жира (липолиз), высвобождая жирные кислоты в кровь. Эти жирные кислоты, в свою очередь, действуют на клетки кости через ядерный рецептор PPARγ, повышая производство склеростина. Когда исследователи блокировали липолиз в жировых клетках или удаляли PPARγ из клеток кости, препараты, имитирующие холод, больше не могли повышать уровни склеростина. Это выявляет петлю обратной связи: термогенные сигналы заставляют жир высвободить топливо, это топливо инструктирует кость секретировать больше склеростина, а склеростин затем сдерживает дальнейшую активацию жира и беигинг.
Комбинирование препаратов для кости и жира ради метаболического здоровья
Наконец, исследователи проверили, поможет ли прерывание этой петли в условиях, похожих на заболевание. Ожиревшим мышам на высокожировой диете давали низкую дозу мирабегрона (β3-адренергический препарат, уже используемый при проблемах с мочевым пузырём), антитело, нейтрализующее склеростин (ромосозумаб, одобренный для лечения остеопороза), или оба препарата. Хотя каждый препарат по отдельности давал скромный эффект, комбинация уменьшала массу жира в ключевых депо, смещала его в сторону меньших, более активных клеток, снижала уровни инсулина, триглицеридов и холестерина и сохраняла прочность костей. Тёплое содержание, которое уменьшает потребность организма в тепле, в значительной мере стирало метаболические преимущества потери склеростина, подчёркивая, что этот путь наиболее важен в присутствии термогенных сигналов.
Что это значит для будущих методов лечения
Проще говоря, работа показывает, что кость — это не просто пассивный каркас, а активный регулятор того, сколько энергии сжигают жировые клетки. Склеростин действует как регулятор громкости, который держит термогенную активность жира, а значит и расход топлива, под контролем. Понижение этой «громкости» — генетически или с помощью лекарств — делает некоторые запасы белого жира более охотно переключаться в режим выработки тепла, когда организм стимулируют холодом или определёнными препаратами. Поскольку тот же подход может укреплять кости и улучшать метаболическое здоровье у мышей, тщательно продуманные комбинации препаратов, направленных на кость и жир, однажды могут помочь лечить ожирение, диабет и остеопороз одновременно, а не по отдельности.
Цитирование: Choquette, G.M., Kim, S.P., Wilkinson, K.J. et al. Sclerostin deficiency sensitizes white adipocytes to thermogenic signals that induce beiging in mice. Nat Commun 17, 2394 (2026). https://doi.org/10.1038/s41467-026-69227-0
Ключевые слова: склеростин, бежевая ткань, взаимодействие кости и жира, термогенез, метаболическое заболевание