Clear Sky Science · ru
Локальный синтез PI(4,5)P2 изоформами PIPKIγ, ассоциированными с септинами, контролирует связь центральспиндлина с срединным телом во время цитокинеза
Как клетки заканчивают расщепление
Цитокинез — последний этап, в ходе которого одна клетка сжимается и разделяется на две — легко воспринимается как должное, но при сбоях он может способствовать развитию рака и других заболеваний. В этом исследовании показано, как определённый набор молекул действует подобно прорабам на узком мостике, соединяющем две новорожденные клетки, обеспечивая аккуратное завершение расщепления вместо отката или застоя процесса.
Последний мостик между дочерними клетками
После удвоения генетического материала и разделения хромосом клетке нужно физически разделиться. Контрактильное кольцо из белковых филаментов стягивается вокруг экватора клетки, формируя глубокую борозду — борозду деления. По мере её вдавления дочерние клетки остаются связанными тонким межклеточным мостиком, в котором расположен плотный центр — срединное тело. Срединное тело — крошечная, но сложная структура из связанных микротрубочек, белковых каркасов и сигнальных липидов; оно служит как связующим, так и центром управления, координирующим последние шаги деления и окончательный разрыв между клетками. 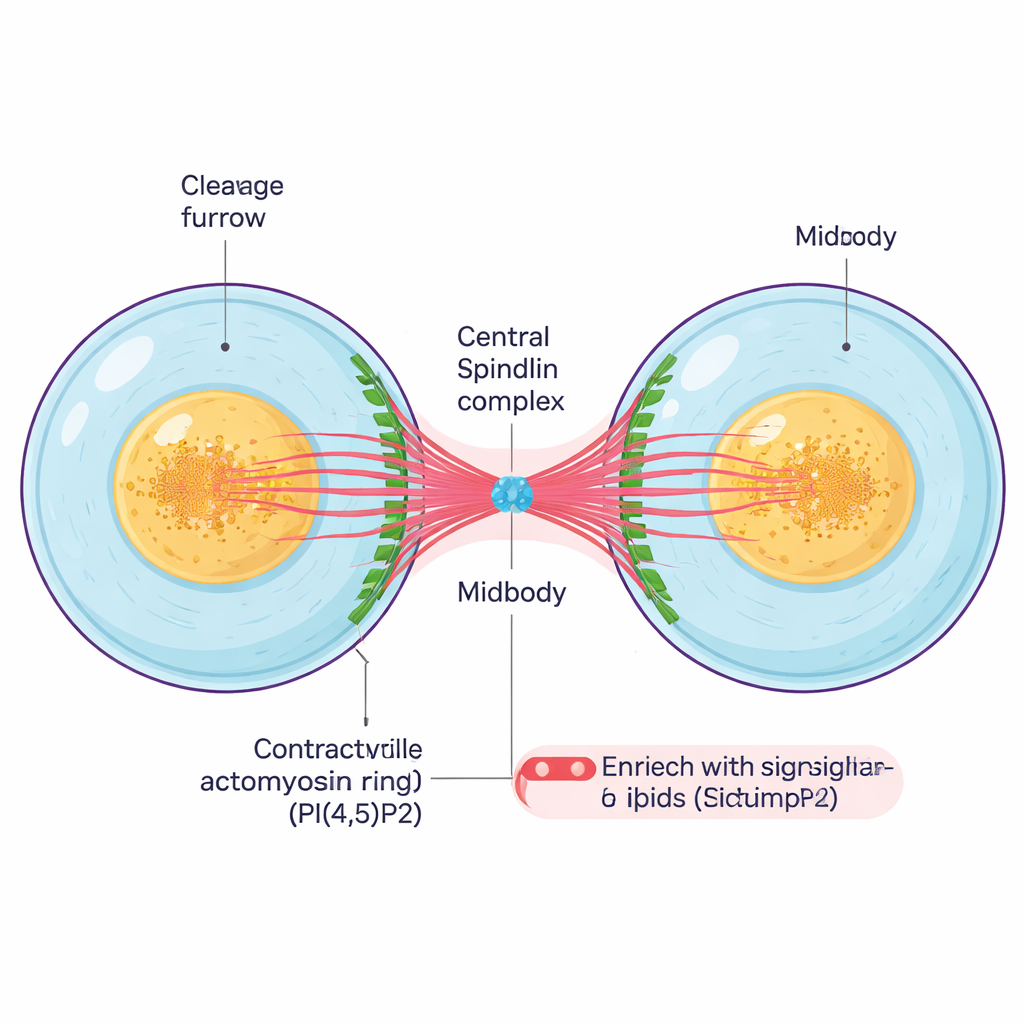
Липидный сигнал, который должен находиться в нужном месте
Ключевой участник процесса — сигнальная жировая молекула в клеточной мембране, называемая PI(4,5)P2. Этот липид помогает закреплять множество белков, формирующих и стесняющих контрактильное кольцо и стабилизирующих мостик. Загадка заключалась в том, как клетки контролируют где и когда появляется PI(4,5)P2, учитывая, что он может диффундировать в мембране. Авторы сосредоточились на ферментах типа I PIP-киназ, которые синтезируют PI(4,5)P2, и в частности на гене PIPKIγ, который существует в нескольких тонко различающихся сплайс-формах. Селективно уменьшая выражение отдельных киназ в человеческих клетках и наблюдая эффекты с помощью продвинутой микроскопии, они обнаружили, что PIPKIγ играет особую роль на позднем этапе цитокинеза, когда формируются мостик и срединное тело, хотя при этом он не сильно изменяет общий уровень PI(4,5)P2 на поверхности клетки.
Септиновые каркасы привлекают специализированный фермент
Группа выяснила, что две сплайс-версии PIPKIγ, обозначенные i3 и i5, действуют как точные инструменты, которые доставляют в нужное место структурные белки, известные как септины. Септины формируют филаменты и кольца, помогая формировать мостик и организовывать другие компоненты. Биохимические вытяжки и визуализация в клетках показали, что PIPKIγ-i3 и PIPKIγ-i5 физически связываются с комплексами септинов и покрывают септиновые филаменты, тогда как другие варианты PIPKIγ этого не делают. Когда исследователи мутировали две специфические аминокислоты в этих вставках сплайсов, ферменты перестали связываться с септинами. В делящихся клетках нормальные PIPKIγ-i3/i5 переходят от рассеянной мембранной локализации к концентрации в борозде деления, затем обозначают межклеточный мостик и срединное тело синхронно с септинами и другим каркасным белком — аниллином. Удаление только вариантов i3 и i5 рассеивало аниллин и септины вдоль мостика, отдаляя их от срединного тела, и у многих клеток цитокинез завершался неудачно, приводя к многоплодным ядрам.
Локальное производство липида фиксирует деловой аппарат
Чтобы проверить, зависят ли эти эффекты от локального образования PI(4,5)P2, авторы измеряли PI(4,5)P2 вокруг срединного тела и манипулировали ферментами, добавляющими или удаляющими этот липид. Обезличивание PIPKIγ-i3/i5 снизило уровень PI(4,5)P2 в срединном теле, тогда как блокировка фермента, разрушающего PI(4,5)P2, дала противоположный эффект. Важно, что восстановление нормальной сплайс-формы PIPKIγ, способной связываться с септинами и обладающей каталитической активностью, вернуло правильную кластеризацию аниллина и септинов на мостике; кинезо-неактивные или неспособные связываться с септинами мутанты такого эффекта не давали. С помощью живой визуализации и метода экспансионной микроскопии, который физически «надувает» образец для выявления тонких деталей, команда показала, что без PIPKIγ-i3/i5 септины перестают перемещаться на микротрубочки мостика, сам мостик становится короче и менее пучковым, а важный комплекс centralspindlin не удерживается прочно в срединном теле.
Построение контрольно-пропускного механизма для аккуратного разрыва
Centralspindlin помогает связывать микротрубочки срединного тела с окружающей мембраной и регулирует маленькие молекулярные переключатели, контролирующие форму клетки. Исследование показывает, что centralspindlin ассоциируется как с септинами, так и с PIPKIγ, и что потеря любого из партнёров схожа по эффекту — ослабляет его присутствие в срединном теле. Авторы предлагают, что септины привлекают PIPKIγ-i3/i5 к вдавленной борозде, где эти ферменты создают сконцентрированное пятно PI(4,5)P2. Этот локальный пул липида, в свою очередь, стабилизирует аниллин, centralspindlin и септины рядом со срединным телом, способствует пучкованию и стабилизации микротрубочек мостика и позволяет межклеточному мостику созревать до момента окончательного рассечения. При нарушении этой системы PI(4,5)P2 появляется не там, где нужно, каркасные белки рассеиваются, микротрубочки слабо пучкуются, и цитокинез часто завершается неудачно.
Почему это важно помимо базовой клеточной биологии
Выявив, как конкретные варианты сплайсинга PIPKIγ и септины взаимодействуют для генерации локального липидного сигнала в срединном теле, эта работа объясняет, как клетки придают пространственную точность высокодвижимой сигнальной молекуле. Эта точность критична для безопасного завершения деления клетки, помогая предотвращать неправильное распределение хромосом и аномальные числа клеток, что может способствовать развитию опухолей. Те же структуры срединного тела влияют и на судьбу клетки и её пролиферацию после деления, поэтому понимание их сборки открывает новые направления для изучения того, как ошибки в этих наноразмерных каркасах могут способствовать раку и, возможно, для манипуляции стволовыми клетками.
Цитирование: Russo, G., Hümpfer, N., Jaensch, N. et al. Local PI(4,5)P2 synthesis by septin-associated PIPKIγ isoforms controls centralspindlin association with the midbody during cytokinesis. Nat Commun 17, 1482 (2026). https://doi.org/10.1038/s41467-026-69224-3
Ключевые слова: деление клетки, цитокинез, сигнальные липиды, септины, онкобиология