Clear Sky Science · ru
Пан-ингибитор RAF эксарафениб нацелен на BRAF класса II/III при НМРЛ и выявляет устойчивость через ARAF–KSR1 и стратегию комбинаций
Почему это исследование важно для пациентов с раком легкого
Большинство людей слышали о таргетных противораковых препаратах, которые нацелены на конкретные генетические изменения. Но для многих пациентов с раком легкого, особенно у тех, чьи опухоли несут менее распространенные мутации в гене BRAF, существующие таргетные препараты часто не эффективны. В этом исследовании представлен новый экспериментальный препарат — эксарафениб, разработанный для воздействия на более широкий набор опухолей, управляемых BRAF, и показано, как клетки рака пытаются уйти от его действия — что позволяет выявить комбинационные схемы лечения, способные дольше контролировать эти опухоли.
Скрытое большинство забытых мутаций
Исследователи начали с простого вопроса: насколько распространены разные типы мутаций BRAF в продвинутых опухолях, и в частности при немелкоклеточном раке легкого (НМРЛ)? Используя очень большую базу данных жидкостной биопсии более чем 160 000 пациентов, они проанализировали фрагменты опухолевой ДНК, циркулирующей в крови. Они обнаружили, что при раке легкого мутации BRAF встречаются примерно у 4–5 % пациентов, что в абсолютных числах означает несколько тысяч людей во всем мире. Важно, что около двух третей этих легочных опухолей несли так называемые мутации BRAF класса II и класса III — типы, на которые одобренные в настоящее время препараты против BRAF не действуют эффективно. Пациенты с одной из этих групп, особенно с мутациями класса II, в целом жили меньше, чем пациенты с более знакомой мутацией класса I, вероятно потому, что для класса I доступны проверенные таргетные терапии, тогда как пациенты с классом II/III в основном получают стандартную химио- или иммунотерапию.
Следующее поколение препарата, нацеленного на весь путь
BRAF является частью каскада белков (MAPK-пути), который передает сигналы роста от поверхности клетки в ядро. Многие существующие препараты против BRAF были разработаны для блокирования только одного мутантного варианта и иногда непреднамеренно активируют родственные белки в нормальных клетках. Эксарафениб создан иначе: это «пан‑RAF» ингибитор, спроектированный для подавления нескольких членов семейства RAF (ARAF, BRAF и CRAF) как в единичной, так и в парной формах, при этом он по возможности не затрагивает большинство других клеточных ферментов. В биохимических тестах на сотнях человеческих киназ эксарафениб сильно блокировал все три белка RAF и имел мало внецелевых эффектов, что указывает на более чистый профиль безопасности по сравнению с ранними пан‑RAF соединениями.
Мощные эффекты в моделях трудноизлечимых опухолей
Команда проверила эксарафениб в батарее клеточных линий и мышиных моделей с различными мутациями BRAF и RAS, включая реалистичные опухоли, полученные от пациентов. В культурах клеток эксарафениб замедлял рост и подавлял MAPK-сигнализацию не только в классических клетках с мутацией BRAF V600E, но и в клетках с мутациями класса II и III, а также во многих RAS-мутационных клетках, для которых в настоящее время нет хороших таргетных опций. У мышей с легочными опухолями с этими изменениями эксарафениб уменьшал или замедлял рост опухолей в дозозависимом режиме и демонстрировал четкие связи между уровнями препарата, подавлением пути и ответом опухоли. Ранние клинические данные от двух пациентов с прогрессирующим раком легкого с мутантным BRAF — одного с редким фузионным вариантом BRAF и другого с точечной мутацией класса II — показали частичные ответы и значительное облегчение симптомов, подтверждая применимость доклинических результатов.
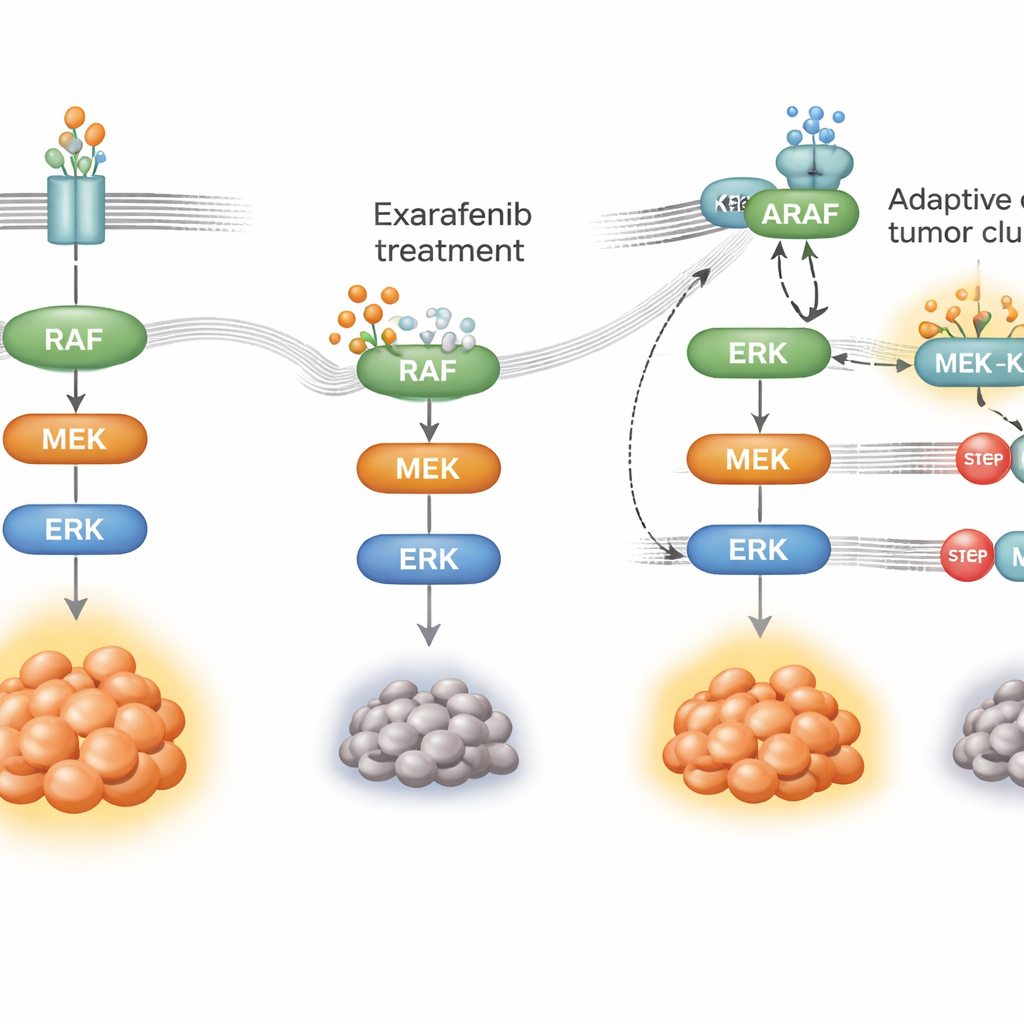
Как рак учится обходить препарат
Ни одна таргетная терапия не действует вечно: клетки рака адаптируются. Чтобы понять, как опухоли могут стать устойчивыми к эксарафенибу, исследователи подвергали клетки рака легкого с мутантным BRAF воздействию препарата в течение месяцев, пока не возникли резистентные популяции. Эти клетки по-прежнему зависели от того же пути роста, но перенастроили способы его использования. Вместо того чтобы в основном полагаться на мутантный BRAF, они усилили активность вышестоящего переключателя RAS и сместились в сторону использования другого члена семейства — ARAF — вместе со строительным белком-‘каркасом’ KSR1. Под давлением препарата ARAF и KSR1 образовывали плотные комплексы, которые помогали поддерживать передачу сигнала по MAPK, несмотря на наличие эксарафениба. Когда ученые селективно отключали ARAF или KSR1 либо снижали активность RAS, резистентные клетки снова становились чувствительными к эксарафенибу, и сигналы выживания разрушались.
Комбинационные стратегии, чтобы опережать сопротивление
Имея эту механистическую карту, команда искала препараты‑партнеры, которые могли бы блокировать путь в «узких местах», общих для исходного и обходного маршрутов. Они обнаружили, что сочетание эксарафениба с ингибиторами MEK или ERK — ключевых нижестоящих звеньев MAPK-каскада — давало сильный синергетический эффект во многих клеточных и мышиных моделях, включая опухоли, которые изначально были менее чувствительны или приобрели резистентность. Эти комбинации дольше удерживали путь в отключенном состоянии, вызывали больше клеточной гибели и в животных часто работали так же хорошо или лучше, чем более высокие дозы эксарафениба в монотерапии, без очевидного дополнительного токсического эффекта. Препараты, нацеленные непосредственно на RAS, также усиливали действие эксарафениба в моделях, где RAS явно управлял резистентностью, что предлагает ещё одну перспективную клиническую тактику.
Что это означает для пациентов
Для людей с НМРЛ, несущих мутации BRAF класса II или III — либо сложные фузии BRAF и сопутствующие мутации RAS — в настоящее время нет одобренных таргетных терапий, и их результаты отстают от исходов у пациентов с более распространёнными изменениями. Это исследование даёт веские научные основания полагать, что эксарафениб может помочь восполнить этот пробел, обеспечив широкое подавление RAF‑опосредованной сигнализации. Оно также объясняет, как опухоли могут адаптироваться через обходной путь ARAF–KSR1, и показывает, что блокирование пути на нескольких уровнях, особенно сочетание ингибиторов RAF и MEK или добавление ингибиторов RAS, может обеспечить более глубокий и длительный контроль над опухолью. В совокупности эти выводы пролагают путь к клиническим испытаниям, направленным на предоставление таргетных комбинационных терапий большой и ранее недостаточно обслуживаемой группе пациентов с раком легкого.
Цитирование: Manabe, T., Bergo, H.C., Li, Q. et al. Pan-RAF inhibitor exarafenib targets BRAF class II/III NSCLC and reveals ARAF-KSR1 resistance and combination strategies. Nat Commun 17, 2484 (2026). https://doi.org/10.1038/s41467-026-69216-3
Ключевые слова: рак легкого с мутантным BRAF, пан-ингибитор RAF, MAPK-сигнализация, лекарственная резистентность, комбинации таргетной терапии