Clear Sky Science · ru
Создание цитохрома P450 как пероксигеназы для селективного гидроксилирования стероидов
Создание лекарств из труднонастраиваемых молекул
Стероидные препараты — от противовоспалительных таблеток до гормональной терапии — входят в число самых широко используемых лекарств в мире. Однако точечная доработка этих молекул, например внесение единственного атома кислорода в строго определённое место, традиционной химией даётся крайне тяжело. В этом исследовании показано, как учёные перепроектировали природный фермент так, чтобы он мог точно «полировать» стероидные молекулы с помощью простой перекиси водорода, что потенциально открывает более экологичные и дешёвые пути получения важных лекарств.
Почему стероиды трудно модифицировать
Стероиды состоят из плотной стопки углеродных колец с множеством практически идентичных связей углерод–водород. Обычные химические методы с трудом нацеливаются только на одну такую связь, не затрагивая остальные, часто требуя жёстких реагентов, высоких температур и множества защитных этапов, которые создают отходы. Между тем даже небольшие изменения — например добавление одной гидроксильной группы (–OH) в конкретную позицию — могут кардинально изменить поведение стероида в организме. Ферменты семейства цитохромов P450 — природные специалисты по такому точному активированию связей C–H, но в своей естественной форме они обычно нуждаются в дорогих вспомогательных молекулах и белках, перерабатывающих кислород, что ограничивает их прямое применение в промышленных масштабах.
Поиск перспективного исходного фермента
С помощью майнинга геномов исследователи выделили автономный фермент P450, названный P450stri, из почвенной бактерии. В отличие от классической «рабочей лошадки» P450BM3, предпочитающей небольшие жирные кислоты, P450stri естественным образом принимает громоздкие стероидные молекулы, такие как тестостерон. В своих родных условиях, используя клеточный кофактор NADH, P450stri добавляет гидроксильные группы в три позиции тестостерона, давая смесь продуктов. Эта врождённая способность распознавать стероиды сделала P450stri привлекательной «исходной платформой» для проектирования более селективного и удобного для промышленности катализатора.
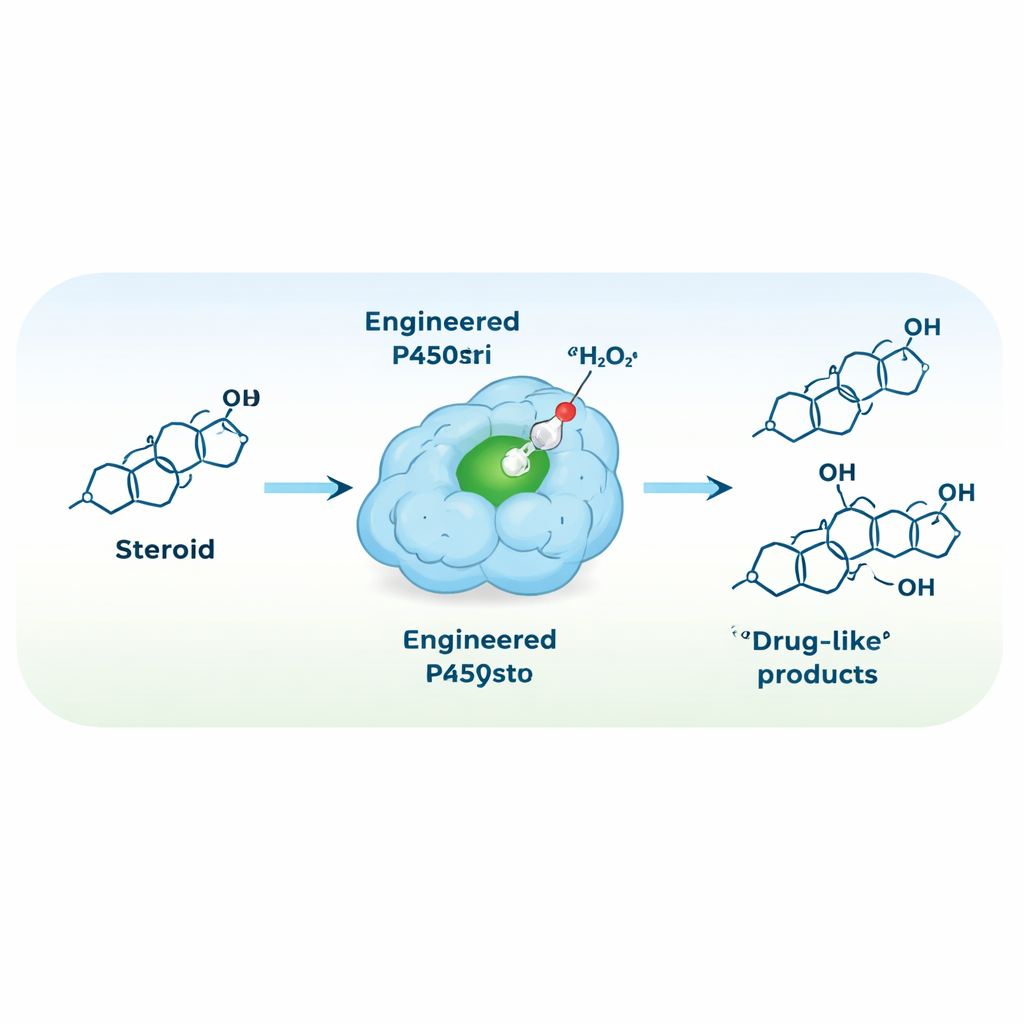
Перенастройка фермента для работы на перекиси водорода
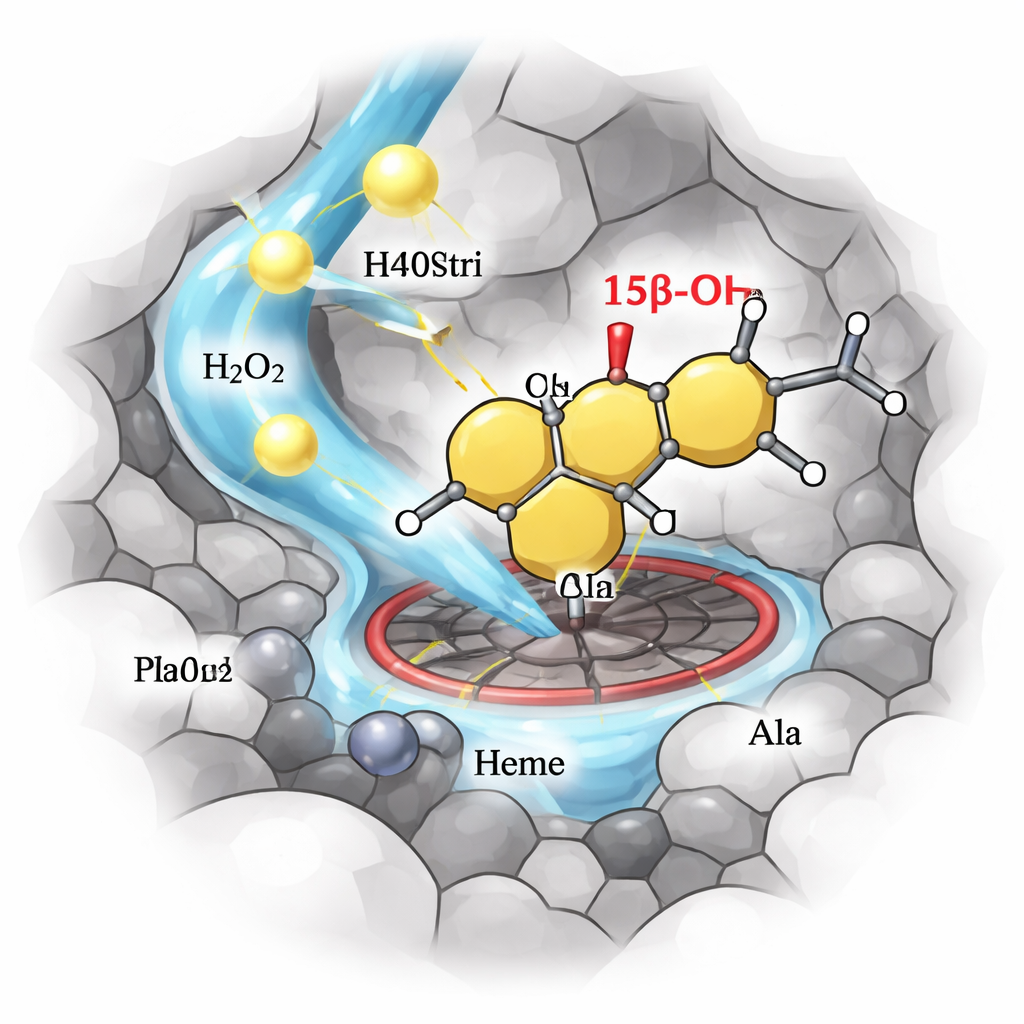
Чтобы упростить реакционную схему, команда поставила задачу превратить P450stri в пероксигеназу — фермент, который использует перекись водорода напрямую в качестве окислителя, исключая необходимость в дорогих кофакторах и вспомогательных белках. Одна стратегическая замена — замена объёмного фенилаланина прямо над гем-центром на более мелкую аланин — дала вариант, названный M1. Это изменение освободило пространство вокруг реактивного железного центра и, что удивительно, сделало фермент более устойчивым к высоким концентрациям перекиси водорода и значительно более селективным. В новом режиме, работающем на перекиси, M1 превращал тестостерон в основном в один продукт — гидроксилированный в позиции 15β — с приблизительно 94% селективностью против 35% у исходного фермента.
Модель «Круглой колбы» для более разумного проектирования ферментов
Чтобы увеличить эффективность, авторы предложили концепцию дизайна, которую называют моделью «Круглой колбы». Они рассматривают активный сайт, где происходит химия, как закруглённое дно, а узкие туннели доступа — как горловину и пробку. Дно определяет, какая позиция в стероиде будет модифицирована, тогда как горловина контролирует, насколько легко стероид и перекись водорода достигают реактивного центра. Руководствуясь компьютерными симуляциями и программами для картирования туннелей, они систематически меняли небольшой набор аминокислот, выстилающих эти туннели, подбирая их размер и гидрофобность. Эта двумерная стратегия привела к выдающемуся варианту, M4, который сохранил высокую селективность по 15β и одновременно значительно увеличил скорость реакции и выдерживал концентрации перекиси водорода до нескольких сотен миллимоляров.
От лаборатории к масштабируемому улучшению стероидов
Инженерный фермент M4 затем протестировали в реакциях большего масштаба с тестостероном и близким стероидом, применяемым в контексте, связанном с повышением производительности. В простых водных смесях при комнатной температуре и при наличии только перекиси водорода M4 превратил более 90% исходного вещества и дал изолированные 15β-гидроксилированные продукты в выходах около 75–80%. Эти условия намного мягче и чище по сравнению с типичными химическими маршрутами. Наконец, команда показала, что при переносе ключевых мутаций в несколько родственных P450 из той же эволюционной «ветви» их можно надёжно превратить в аналогично селективные и эффективные пероксигеназы, подчёркивая общность их правил проектирования.
Что это значит для будущих лекарств
Для неспециалиста суть в том, что исследователи научили природный фермент действовать как весьма точная, работающая на перекиси «микрофабрика» для модификации стероидных препаратов. Объединив простую концептуальную модель с целевыми мутациями, они создали фермент, который способен добавить группу OH в нужное место при мягких и масштабируемых условиях, а затем перенесли эту стратегию на родственные белки. Этот подход может упростить производство существующих стероидов, открыть пути к новым кандидатам в лекарства и послужить схемой для проектирования других ферментов, которые чисто активируют стойкие C–H связи в сложных молекулах.
Цитирование: Tang, T., Wang, R. & Chen, Y. Engineering a cytochrome P450 enzyme as a peroxygenase for selective hydroxylation of steroids. Nat Commun 17, 1996 (2026). https://doi.org/10.1038/s41467-026-69211-8
Ключевые слова: биотехнология стероидов, инжиниринг цитохрома P450, пероксигеназа, катализ перекисью водорода, селективное гидроксилирование