Clear Sky Science · ru
14-3-3ζ взаимодействует с доменом, связывающим ДНК, белка FOXO3a и конкурирующе отрывает его от ДНК посредством двойного привязывания по мотивам
Как раковые клетки отключают свой собственный выключатель самоуничтожения
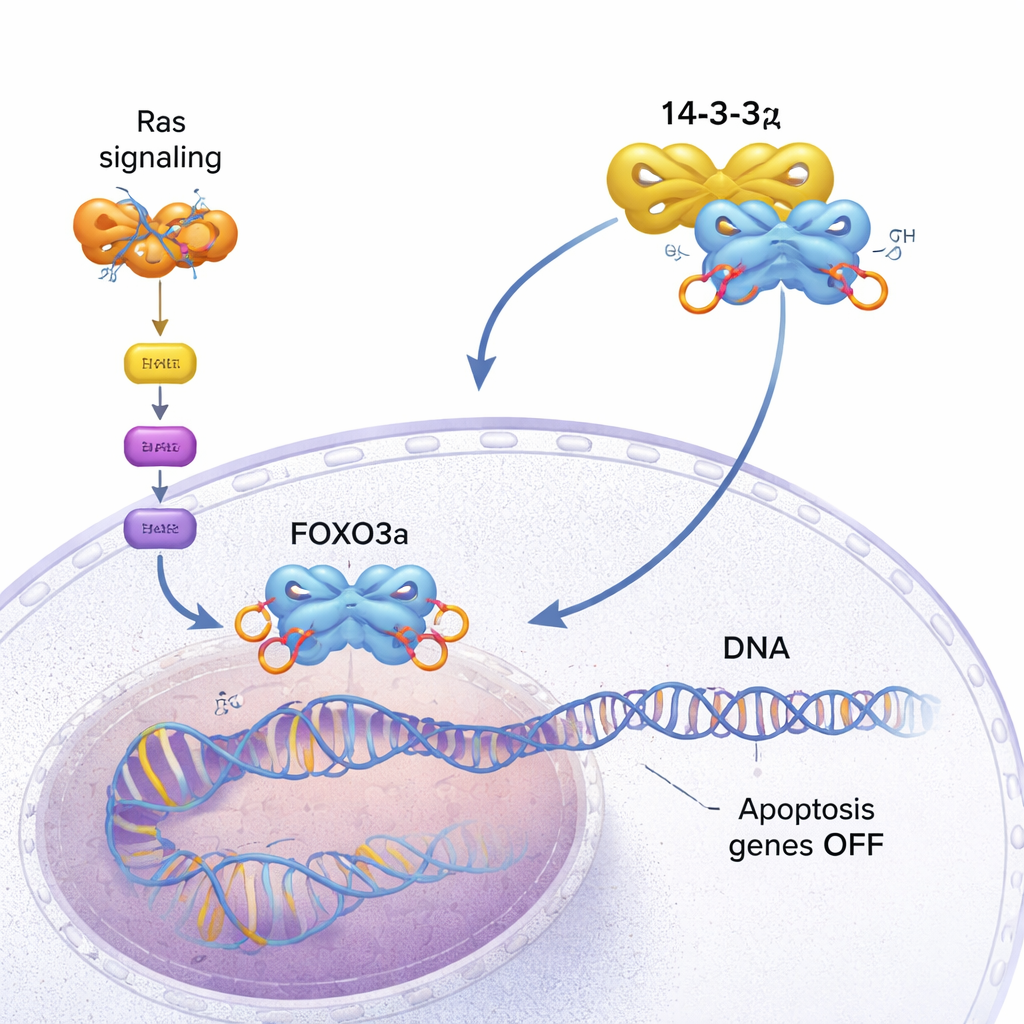
В наших клетках есть встроенные предохранители, которые могут запустить их гибель, если они становятся слишком повреждёнными или опасными. Одна из таких систем управляется белком FOXO3a, который включает гены, заставляющие сбившиеся с пути клетки погибать. Однако многие опухоли находят способы заглушить FOXO3a и продолжать расти. В этом исследовании подробно разобраны молекулярные механизмы, с помощью которых другой белок, 14-3-3ζ, помогает раковым клеткам отрывать FOXO3a от ДНК и отключать этот механизм самоуничтожения.
Белок‑страж, который противодействует раку
FOXO3a действует как инспектор безопасности клетки. Он связывается с определёнными участками ДНК и активирует гены, замедляющие рост или запускающие запрограммированную гибель клетки (апоптоз), когда что‑то идёт не так. В здоровых клетках это помогает предотвращать образование опухолей. Однако во многих раках путь, стимулирующий рост и управляемый мутантными белками Ras, постоянно остаётся включённым. Этот путь активирует киназу AKT, которая химически помечает FOXO3a фосфатными группами в нескольких сайтах. Эти метки создают посадочные места для 14-3-3ζ — димерного «адаптерного» белка, распознающего фосфорилированные мотивы у различных мишеней. Когда 14-3-3ζ прикрепляется к FOXO3a, внутренние тормоза клетки начинают давать сбой.
Почему простая сила связывания не объясняла эффект
Ранее, при работе с родственным белком FOXO4, предполагали, что 14-3-3 белки отрывают факторы FOXO от ДНК просто потому, что связываются крепче. Но FOXO3a предпочитает свои естественные ДНК‑мишени сильнее, чем предполагала старая модель. В этом исследовании учёные получили версию FOXO3a, включающую домен, связывающий ДНК, и две ключевые фосфорилируемые позиции. Они измерили, насколько прочно этот белок связывается либо с ДНК, либо с 14-3-3ζ, и обнаружили, что различия в прочности связывания были скромными: 14-3-3ζ был лишь примерно в два раза сильнее партнёра, чем ДНК. Тем не менее в экспериментах‑смесах, отслеживающих миграцию молекул через хроматографическую колонку, 14-3-3ζ вызывал почти полное высвобождение ДНК из FOXO3a, как будто он был приблизительно в 100 раз более конкурентоспособен, чем ожидалось. Это несоответствие подсказало наличие дополнительного механизма.
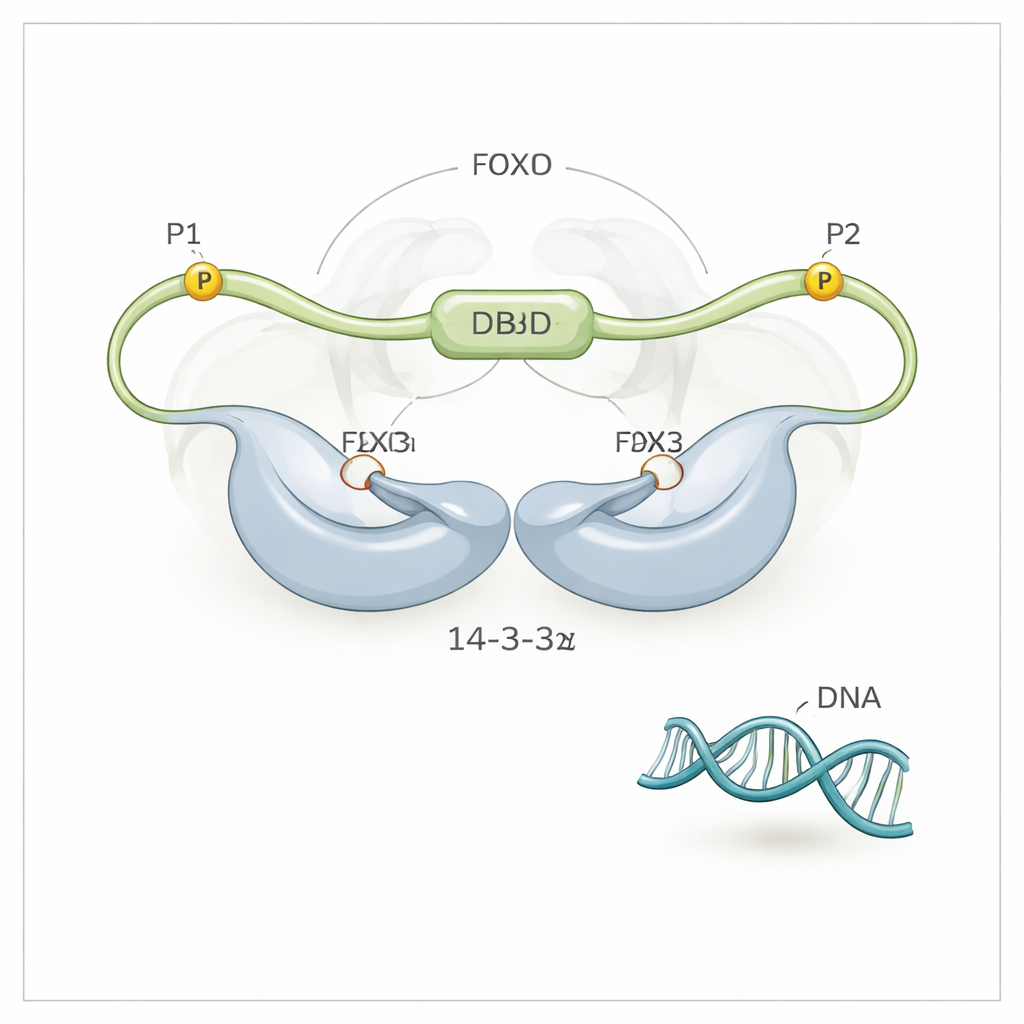
Трёхточечный захват, вытесняющий ДНК
С помощью высокоразрешающей МРТ‑спектроскопии команда обнаружила, что 14-3-3ζ делает больше, чем просто захватывает FOXO3a за два фосфорилированных мотива (обозначаемые P1 и P2). Он также устанавливает прямой, хотя и более слабый контакт с самим доменом, связывающим ДНК (DBD) FOXO3a — той самой поверхностью, которая обычно облегает ДНК. Белок 14-3-3ζ образует симметричный димер с двумя бороздками. Каждая бороздка зажимает один из фосфорилированных мотивов FOXO3a, закрепляя FOXO3a за два пункта на 14-3-3ζ. Поскольку один из этих мотивов (P2) находится очень близко по цепи к DBD, это «двойное привязывание по мотивам» фактически держит 14-3-3ζ рядом с DBD, сильно повышая вероятность того, что DBD столкнётся и свяжется с поверхностью 14-3-3ζ вместо ДНК. Исследователи даже наблюдали, что DBD переливается с одной стороны димера 14-3-3ζ на другую, проводя большую часть времени экранированным от ДНК.
Какие фосфатные метки имеют наибольшее значение
Чтобы отделить роли двух фосфорилируемых сайтов, команда создала варианты FOXO3a, в которых мог быть фосфорилирован только один сайт за раз. Когда был активен только сайт P2, расположенный рядом с DBD, 14-3-3ζ мог частично вытеснить ДНК, но не полностью. Когда активным был только более удалённый сайт P1, 14-3-3ζ мог связываться с FOXO3a, но почти не влияло на его захват ДНК. Полное высвобождение ДНК требовало совместной работы обоих сайтов: P1 обеспечивает высокоаффинную начальную точку прикрепления для 14-3-3ζ, а P2 позиционирует димер достаточно близко к DBD, делая локальную концентрацию 14-3-3ζ на этом участке по сути огромной. Это многоступенчатое привязывание усиливает скромное предпочтение связывания в мощную способность вытеснять ДНК.
От молекулярной перетягивания каната к новым идеям для лекарств
Для неспециалиста главное вывод — раковые клетки эксплуатируют хитрую геометрию молекул, а не только грубую силу связывания, чтобы заглушить важный белок‑супрессор опухолей. 14-3-3ζ использует два небольших фосфатзависимых анкера на FOXO3a как точки опоры, затем накрывает поверхность, захватывающую ДНК в основном домене FOXO3a, препятствуя ему включать гены, ответственные за гибель клетки. Поскольку семейства FOXO и 14-3-3 широко представлены во многих тканях, эта стратегия двойного привязывания, вероятно, распространена и в других раках. Нарушение либо фосфатзависимых анкеров, либо более слабого контакта с поверхностью домена, связывающего ДНК, может восстановить способность FOXO3a активировать программы самоуничтожения в опухолевых клетках, что открывает перспективные новые подходы для разработки противораковых лекарств.
Цитирование: Enomoto, S., Kuwayama, T., Nakatsuka, S. et al. 14-3-3ζ interacts with DNA-binding domain of FOXO3a and competitively dissociates DNA by dual-motif tethering. Nat Commun 17, 1503 (2026). https://doi.org/10.1038/s41467-026-69203-8
Ключевые слова: FOXO3a, белки 14-3-3, апоптоз, сигналинг Ras–AKT, противораковая терапия